Samenvatting
Verwekker: Mazelenvirus
Incubatieperiode: Van expositie tot begin van prodromale fase gemiddeld 10 dagen (spreiding 7 tot 14 dagen) en gemiddeld 14 dagen tot het begin van het exantheem (spreiding 7 tot 18 dagen)
Besmettingsweg: Uitscheiding van het mazelenvirus vindt plaats vanuit de neus- en keelholte door bijvoorbeeld niezen, hoesten en praten door een persoon met mazelen in de besmettelijke periode
Besmettelijke periode: 4 dagen vóór tot en met 4 dagen na het begin van het exantheem
Maatregelen: Bron- en contactonderzoek, contact vermijden met personen uit risicogroepen gedurende besmettelijke periode, immunisatie contacten. Meldingsplichtige ziekte groep B2 en artikel 26.
Symptomen: Koorts, hoesten, neusverkoudheid, oor- of oogontsteking, Koplikse vlekjes en grofvlekkig exantheem. In ernstige gevallen longontsteking of hersenontsteking
Zie ook Wie is beschermd tegen mazelen en Stroomschema maatregelen.
blok
Deze richtlijn is ontwikkeld voor zorgprofessionals werkzaam binnen de infectieziektebestrijding. De primaire doelgroepen zijn GGD- en LCI-professionals. Deze richtlijn bevat adviezen, taken en verantwoordelijkheden en vormt een basis voor het nemen van geïnformeerde beslissingen en het maken van beleid in de praktijk. Voor meer informatie zie Ontwikkeling LCI-richtlijnen.
Vastgesteld (Landelijk Overleg Infectieziektebestrijding): 24 juni 2025. Publicatie: 7 juli 2025.
Diagnostiek vastgesteld: 12 november 2025. Publicatie: 20 januari 2026.
Wijzigingen sinds de publicatie
- 20 januari 2026: Het op 12 november 2025 vastgestelde hoofdstuk Diagnostiek is gepubliceerd. In de hoofdstukken Diagnostiek, Preventie (Immunisatie) en Maatregelen is informatie over diagnostiek en het beleid bij mazelenverschijnselen na vaccinatie opgenomen. Onder Diagnostiek en Maatregelen (Contactonderzoek) is informatie toegevoegd over de inzet van een aviditeitstest.
- 5 september 2025: de drie onderbouwingsbijlagen (Beperkt contactonderzoek bij een doorbraakinfectie, Afweging (bof, mazelen, rodehond)-vaccinatie en PEP zuigelingen zijn samengebracht in Onderbouwing mazelen. In dit nieuwe document is de onderbouwing van het PEP-beleid bij personen ≥ 14 maanden die niet zwanger of immuungecompromitteerd zijn en het PEP-beleid bij zwangeren nieuw toegevoegd.
- 13 augustus 2025: de uiterste spreiding rondom exantheem is van 21 dagen terug gebracht naar 18 dagen, conform de voorgaande versie van de richtlijn.
- 14 juli 2025: de bijlage Mazelen in de huisartsenpraktijk is herzien in samenwerking met het (Nederlands Huisartsen Genootschap).
Herziening 2025
De richtlijn is herzien onder leiding van dr. C.J.G. Kampman, arts M+G izb, auteur richtlijnen bij de LCI. De wijzigingen ten opzichte van de vorige versie (2019) zijn:
- De achtergrondinformatie (verwekker, epidemiologie, pathogenese, ziekteverschijnselen, immuniteit, transmissie, risicogroepen) zijn geüpdatet met recente literatuur. Sommige delen en/of paragrafen zijn verplaatst voor een logischer vindbaarheid (kader Wie is beschermd tegen mazelen is verplaatst van Verhoogde kans op infectie naar Maatregelen; het herhaaldelijk toedienen van immunoglobuline is verplaatst van Passieve immunisatie naar Postexpositieprofylaxe). Ook zijn dubbelingen zoveel mogelijk opgeheven.
- Het PBM-advies bij diagnostiekafname is aangepast. In de vorige versie was er geen PBM-advies bij een immune werknemer in de extramurale setting die diagnostiek afneemt. In de herziene versie wordt wel een FFP2-masker en eventueel spatbril geadviseerd bij het afnemen van een keelwat, i.v.m. het risico op spatten.
- Er zijn twee nieuwe zwangerschapsparagrafen toegevoegd: immuniteit en transmissie.
- De besmettelijke periode in een klinische setting is aangepast conform SRI-richtlijn Isolatie naar 'tot en met 4 dagen' na het ontstaan van exantheem.
- Het verzoek om bij ziekenhuisopname of bij overlijden t.g.v. mazelen te melden aan de GGD is opgenomen in de paragraaf Meldingsplicht.
- Onder Immunoglobulinen extra informatie de beschikbaarheid van Beriglobin P aangepast en is Cuvitru toegevoegd. Interval tussen immunoglobuline en BMR-vaccin aangepast van > 6 weken naar minimaal 3 maanden.
- Beleid voor specifieke groepen is uitgewerkt in nieuwe bijlagen, zie hieronder. In de twee bijlagen voor werknemers wordt voor dubbele informatie verwezen naar de hoofdrichtlijn: Wie is beschermd en Wettelijk kader.
- De onderbouwingen BMR-0 en PEP zuigelingen zijn samengevoegd met de onderbouwing BCO bij doorbraakinfecties. Dit samengestelde document is gepubliceerd op 5 september 2025. In dit nieuwe samengevoegde document is de onderbouwing van het PEP-beleid bij personen ≥ 14 maanden die niet zwanger of immuungecompromitteerd zijn en het PEP-beleid bij zwangeren nieuw toegevoegd.
Bijlagen
- Bescherming tegen mazelen in de gezondheidszorg is geactualiseerd, vastgesteld.
- Bescherming tegen mazelen voor werknemers in de kinderopvang is nieuw, vastgesteld.
- Handreiking kinderopvang is nieuw, vastgesteld.
- De informatiebrieven en vertalingen worden later in 2025 bijgewerkt.
- Mazelen bij arbeidsmigranten is ongewijzigd vastgesteld.
- Mazelen in de huisartsenpraktijk is vastgesteld door het LOI, nieuwe versie in samenwerking met het NHG gepubliceerd op 14 juli 2025.
- Postexpositiebeleid immuungecompromitteerde contacten bij mazelen is 4 april 2025 geaccordeerd door de wetenschappelijke verenigingen en is nu bij de publicatie van de herziene richtlijn een apart product geworden, te vinden onder 'Zie ook'.
- Stroomschema maatregelen contacten is geactualiseerd en opgenomen in de richtlijn zelf, en daarmee vervallen als aparte bijlage.
- Bijlage Laboratoriumonderzoek bij een mazelenepidemie is vervallen. De informatie wordt opgenomen in het nieuwe hoofdstuk Diagnostiek (volgt).
- Toedienen immunoglobuline bij zuigelingen is nieuw en vastgesteld
- Wachtkamercontacten is nieuw en met een kleine verduidelijking vastgesteld
Achtergronden
Verwekker
Mazelenvirus behoort tot de familie van de paramyxoviridae, genus morbillivirus. Het mazelenvirus bestaat uit een enkelstrengs RNA-genoom dat wordt beschermd door virale eiwitten en omhuld door een lipidenmembraan. Het virus is antigeen-stabiel, waardoor het vaccinvirus geïsoleerd in 1950 nog steeds een goede bescherming geeft tegen alle circulerende wildtype-stammen. Totaal zijn er 24 genotypen van het mazelenvirus bekend. In Nederland circuleren sinds 2021 nog 2 genotypen (B3 en D8). Verondersteld wordt dat dit een gevolg is van grootschalige vaccinatie-inspanningen om mazelen te elimineren. Het mazelenvirus genotype B3 heeft een hoger transmissierisico, een hogere incidentie van vaccinfalen, ziekenhuisopname en complicaties, vergeleken met D8 (Gershon 2021, Moss 2024, Strebel 2019).
Epidemiologie
Verspreiding in de wereld
Mazelen komt voor over de hele wereld. Zonder vaccinatie kwamen epidemieën elke 2 tot 5 jaar voor, die gemiddeld 3 tot 4 maanden duurden (Gershon 2021). Vaccinatiecampagnes hebben ertoe geleid dat zowel het totaal aantal infecties als het aantal overlijdens aan mazelen wereldwijd gedaald is. Naar schatting heeft mazelenvaccinatie 60 miljoen doden voorkomen tussen 2000 en 2023 (Minta 2024).
In 2022 waren er wereldwijd naar schatting 9 miljoen mensen met mazelen, dit is een toename van 18 procent ten opzichte van 2021 (CDC 2024). De meeste gevallen van mazelen doen zich voor in Irak en Pakistan met in beide landen meer dan 16.000 gevallen tussen maart en augustus van 2024 (CDC 2024). In 2022 waren er nog 136.000 geschatte overlijdens ten gevolge van mazelen (dit was 761.000 in 2000). De overlijdens doen zich met name voor in lage inkomenslanden, onder ongevaccineerden en bij kinderen die jonger zijn dan 5 jaar (Minta 2023).
In 2023 had 83 procent van de kinderen wereldwijd ten minste één vaccinatie tegen mazelen gehad, in 2019 was dit nog 86 procent (WHO 2024). Deze daling in de vaccinatiegraad is waarschijnlijk het gevolg van de COVID-19 pandemie, die leidde tot het opschorten van vaccinatiecampagnes, waardoor en naar schatting 61 miljoen vaccinaties wereldwijd zijn gemist. In 2023 zijn er nog steeds bijna 35 miljoen doses gemist, mogelijk door logistieke uitdagingen, vaccinatietwijfel en geen goede toegang tot zorg (CDC 2024, eClinicalMedicine 2024, (World Health Organization) 2024).
Tussen februari 2024 en januari 2025 zijn er totaal 32.265 mensen in Europa gediagnosticeerd met mazelen. De meeste personen werden gediagnosticeerd in Roemenië (27.568), Italië (1.097) en Duitsland (637). In Roemenië overleden 18 personen aan mazelen in die periode (ECDC 2025). Voor actuele cijfers wereldwijd zie de Wereldgezondheidsorganisatie Global Update.
Voorkomen in Nederland
Voor de invoering van mazelenvaccinatie was er om het jaar was een grote, landelijke epidemie. Vanaf 1945 was de sterfte aan mazelen tijdens de epidemieën gemiddeld 16 per 100.000 gevallen. Ongeveer 5 procent kreeg complicaties zoals pneumonie en andere ernstige respiratoire aandoeningen. Na invoering van landelijke vaccinatie tegen mazelen in 1976 nam de incidentie snel af. In dat jaar werden 2500 gevallen van mazelen bij de Inspectie voor de Volksgezondheid gemeld, 3 jaar later nog maar 56 (Beersma 1988).
Buiten de epidemieën worden er in Nederland 10 tot 20 mazelengevallen per jaar gemeld, meestal betreft dit infecties die in het buitenland zijn opgelopen. In uitbraaksituaties loopt het aantal gevallen op. In 1983, 1987-1988 en 1992-1993 waren er uitbraken onder ongevaccineerden.
In 1999-2000 was er een landelijke epidemie die bijna een jaar duurde. Er werden 3300 gevallen met mazelen gemeld van wie 95 procent niet gevaccineerd was, en vier personen overleden (van Binnendijk 2003, van den Hof 2002). In 2008 was er een uitbraak in de regio Den Haag, met circa 100 ziektegevallen zonder sterfgevallen, rond mensen die om antroposofische redenen niet gevaccineerd waren (Hahne 2010).
In 2013-2014 was er een landelijke epidemie, vooral onder ongevaccineerden uit de biblebelt. Er werden 2700 gevallen met mazelen gemeld. De meeste personen met mazelen waren tussen de 4-17 jaar (Opstelten 2013, Woudenberg 2017). Belangrijk om te vermelden is dat er bij epidemieën een aanzienlijke onderrapportage is van het daadwerkelijke aantal personen met mazelen. In de epidemie van 2013-2014 werden er ruim 11-maal meer personen met mazelen geschat dan dat er werden gemeld (Woudenberg 2018). In 2024 en 2025 is er een verheffing te zien van het aantal personen met mazelen in Nederland. Tot april 2025 zijn er 347 personen met mazelen gemeld in verschillende (Gemeentelijke gezondheidsdienst)-regio's, zie ook de Actuele cijfers mazelen op RIVM.nl.
Pathogenese
Mazelen kent een bifasisch verloop. In de eerste fase infecteert het mazelenvirus de mens via het respiratoire epitheel. Lokale vermeerdering van het virus vindt plaats in de lymfoïde weefsels in de luchtwegen.
In de tweede fase volgt viremie als gevolg van het circuleren van virusgeïnfecteerde lymfocyten in het bloed. De viremie resulteert in een gegeneraliseerde infectie waarbij het virus repliceert in lymfocyten van alle lymfoïde weefsels en organen en zich verspreidt naar endotheelcellen, epitheelcellen, dendritische cellen en keratinocyten. Infectie van de luchtwegen kan zorgen voor oedeem en verlies van trilharen (cilia), waardoor de luchtwegen gevoelig worden voor een secundaire bacteriële infectie, zoals een otitis media of een pneumonie. Het exantheem ontstaat waarschijnlijk door infectie van het vasculaire endotheel, waarbij vasodilatatie en verhoogde permeabiliteit optreedt (Gershon 2021, Laksono 2020, Moss 2024).
Incubatieperiode
De incubatieperiode van expositie tot begin van de prodromale fase duurt gemiddeld 10 dagen met een spreiding van 7 tot 14 dagen en is vaak iets langer bij volwassenen dan bij kinderen. De incubatieperiode van expositie tot begin van het exantheem is gemiddeld 14 dagen, met een spreiding van 7 tot 18 dagen (Gastanaduy 2024, Lessler 2009, Moss 2012).
Ziekteverschijnselen
Mazelen begint plotseling met algehele malaise, koorts, conjunctivitis, verkoudheid en hoesten. De koorts neemt in de loop van 2 tot 3 dagen geleidelijk toe tot meer dan 39 graden Celsius (prodromale fase). Aan het einde van de prodromale fase, net voor het ontstaan van het exantheem, kunnen bij 50-70 procent van de gevallen Koplikse vlekjes (kleine witte vlekjes op het mondslijmvlies) ontstaan die kenmerkend zijn voor mazelen (Gershon 2021, Jain 2024).
3-7 dagen na ontstaan van de klachten ontwikkelt zich een gegeneraliseerd grofvlekkig exantheem dat ruw aanvoelt (als schuurpapier). Het begint achter de oren en langs de haargrens en breidt zich in 3 dagen uit via gezicht, nek, borst, romp naar de ledematen. Na enkele dagen verbleekt het exantheem weer. In totaal duurt deze exanthemateuze fase meestal 7-10 dagen. Hoesten is vaak het laatste symptoom dat verdwijnt (Gershon 2021).
Na het doormaken van mazelen is men enkele maanden tot jaren verhoogd vatbaar voor andere infecties. Dit is waarschijnlijk het gevolg van infectie en depletie van geheugenlymfocyten met het mazelenvirus en heet ook wel immuun-amnesie (Gadroen 2018, Laksono 2018).
Mild verloop bij partiële immuniteit
Een zeer milde vorm van mazelen kan zich voordoen bij de volgende personen:
- Baby’s die nog gedeeltelijk beschermd zijn door maternale antistoffen;
- Personen die laat of onvoldoende immunoglobuline hebben gekregen na contact met een mazelengeval;
- Gevaccineerde personen met een doorbraakinfectie door secundair vaccinfalen. Bij mensen met primair vaccinfalen verloopt mazelen zoals bij een immuun-naïef persoon, zie voor verdere uitleg paragraaf Immunisatie.
De typische ziekteverschijnselen kunnen afwezig of minimaal zijn, ook is de incubatietijd verlengd. Bij een mild verlopende mazelenvirusinfectie kunnen exantheem, koorts, hoesten, verkoudheid en conjunctivitis minimaal of afwezig zijn. Ook Koplikse vlekjes zijn gering in aantal of afwezig. Het exantheem kan daarnaast een atypisch patroon volgen en de vlekken conflueren meestal niet (Gershon 2021).
Mazelen bij personen met een afweerstoornis
Bij personen met een afweerstoornis kan de initiële presentatie ook afwijken. Bij hen kan het exantheem afwezig zijn, terwijl het risico op complicaties (pneumonie, encefalitis) en overlijden verhoogd is (Gershon 2021).
Complicaties
De complicaties die bij mazelen optreden hangen samen met het effect van het mazelenvirus op de luchtwegen en op het immuunsysteem. De meest voorkomende complicaties zijn de volgende:
- Complicaties van de luchtwegen: gedacht moet worden aan otitis media, laryngotracheobronchitis, bronchiolititis en pneumonie. Deze complicaties kunnen veroorzaakt worden door het mazelenvirus zelf of door een bacteriële superinfectie. Een otitis media kan ontstaan als gevolg van een ontsteking en verstopping van de buis van Eustachius. Een zeldzame en zeer ernstige vorm van pneumonie is de reuscelpneumonie (of Hecht-pneumonie). Deze komt met name voor bij kinderen met mazelen en immuunsuppressie en is klinisch niet te onderscheiden van andere interstitiële pneumonieën, behalve op basis van histologie (Gershon 2021, Griffin 2020, Moussallem 2007).
- Complicaties van het zenuwstelsel: verschillende vormen van encefalitis kunnen zich voordoen. Bij een acute gedissemineerde encefalomyelitis (1 per 1000 mazelengevallen) treedt demyelinisatie op als gevolg van een auto-immuunreactie. Subacute scleroserende panencefalitis (SSPE) (10 per 100.000 mazelengevallen) is een progressieve dodelijke aandoening. De klinische symptomen manifesteren zich meestal pas een aantal jaren (gemiddeld 4-10 jaar) na de acute infectie. De precieze pathogenese van SSPE is onduidelijk, mogelijk is persisterende virusreplicatie in de hersenen de oorzaak (Lebon 2021, Moss 2024). Het risico op SSPE is hoger wanneer mazelen op jonge leeftijd wordt opgelopen (< 1 jaar) (Miller 1992).
In lage-inkomenslanden en conflictgebieden heeft mazelen in combinatie met ondervoeding vaak een ernstig verloop, waarbij de ziekte naast de gebruikelijke complicaties kan leiden tot hemorragisch exantheem, huidinfecties, diarree, dehydratie, keratitis en blindheid (Portnoy 2019).
Sterfte
In lage-inkomenslanden en conflictgebieden bedraagt de mortaliteit tussen de 5-10 procent, in sommige gebieden nog hoger (Moss 2024, Portnoy 2019). In hoge-inkomenslanden, waaronder Nederland, is de kans om aan mazelen te overlijden erg klein (ECDC 2024). Tijdens de Nederlandse mazelenuitbraak van 2013-2014 zijn er ruim 2700 gevallen van mazelen gemeld en is er één persoon overleden. Waarschijnlijk is er een onderrapportage van het aantal gevallen en overlijdens, mede door gevallen van subacute scleroserende panencefalitis (SSPE) die soms pas jaren later gekoppeld kunnen worden aan de uitbraak (Woudenberg 2017).
Natuurlijke immuniteit
Het aangeboren immuunsysteem wordt onderdrukt door het mazelenvirus, waardoor het virus zich kan verspreiden, voordat het verworven immuunsysteem wordt geactiveerd. T-lymfocyten zijn van belang bij het opruimen van de infectie, terwijl de antistofrespons van belang is bij de bescherming tegen herinfectie. Hierdoor kunnen personen met ernstige humorale afweerstoornissen de infectie gewoon opruimen, terwijl personen met een ernstige T-lymfocytendysfunctie vaak ernstige progressieve ziekte ontwikkelen. Het doormaken van mazelen geeft doorgaans levenslange immuniteit (Gershon 2021, Moss 2024).
Vanaf het moment dat het exantheem verschijnt, zijn er veelal virusspecifieke (immunoglobuline G)- en (immunoglobuline M)-antistoffen aantoonbaar. De IgM-titer stijgt tot een maximum op de 7e tot 10e dag en daalt vervolgens snel. Na 6 tot 8 weken is IgM niet meer te detecteren. De IgG-titer stijgt tot de 30e dag en blijft dan levenslang aantoonbaar (Tipples 2003, WHO 2007). De concentratie mazelenvirus-specifieke neutraliserende antilichamen in serum is een goede graadmeter voor bescherming tegen ziekte en herinfectie: concentraties van meer dan 120 mIU/ml beschermen tegen ziekte, maar hogere concentraties zijn nodig om te beschermen tegen infectie (Moss 2024).
Immuniteit foetus en/of pasgeborene
De bescherming door maternale antistoffen is beperkt. Zuigelingen van gevaccineerde moeders zijn nauwelijks beschermd, omdat maternale antistoffen snel verdwijnen (Leuridan 2007, Waaijenborg 2013). Zuigelingen van moeders die mazelen hebben doorgemaakt, hebben wel enige mate van bescherming door maternale antistoffen. In dat geval kan de zuigeling tot en met 2 maanden na de geboorte als beschermd beschouwd worden door maternale antistoffen. Zie voor meer informatie de Onderbouwing (Resultaten literatuur uitgangsvraag 2).
Reservoir
De mens is de enige natuurlijke gastheer van het mazelenvirus. Apen kunnen ook met het virus besmet worden (Gershon 2021).
Transmissie
Besmettingsweg
Mazelenvirus wordt uitgescheiden tijdens hoesten, niezen, praten en ademen, door een persoon met mazelen. Overdracht door de lucht vindt met name plaats dichtbij de persoon die het virus uitscheidt, doordat het virus op de slijmvliezen (ogen, neus, mond) terechtkomt of wordt ingeademd door iemand anders (WHO 2024).
Het virus kan enkele uren overleven in de lucht en op oppervlakken (ECDC 2023, WHO 2024). Hierdoor is indirecte transmissie mogelijk, ook nadat de persoon die het virus uitscheidt de ruimte heeft verlaten, via oppervlakken en door het inademen van virusdeeltjes die in de ruimte zweven. Hoe lang overdracht via de lucht mogelijk is hangt af van diverse factoren, zoals de hoeveelheid virusdeeltjes in de lucht en ventilatie. Via luchtstromen kan mazelenvirus ook worden verspreid naar andere ruimtes (Li 2007).
Perinatale transmissie
Bij congenitale mazelen is er sprake van transmissie van mazelen van de zwangere naar de foetus. Als er bij de pasgeborene exantheem wordt geconstateerd binnen 10 dagen post-partum, spreekt men van congenitale mazelen. Tevens is bekend dat zwangeren met een mazelenvirusinfectie langer virus uitscheiden dan niet-zwangeren, wat kan leiden tot perinatale transmissie. Het is niet bekend of er transmissie van het mazelenvirus naar de foetus op kan treden in eerdere trimesters (Charlier 2021, Rasmussen 2015, Shperling 2022).
Besmettelijke periode
De besmettelijke periode is 4 dagen vóór tot en met 4 dagen na het begin van het exantheem (Klinkenberg 2011, Moss 2024).
Besmettelijkheid
Mazelen is een van de meest besmettelijke infectieziekten. Het aantal secundaire ziektegevallen dat een persoon met mazelen in een volledig vatbare populatie veroorzaakt (basale reproductiegetal R0) is 12 tot 18 (Guerra 2017). Het risico op secundaire transmissie naar niet-beschermde contacten is meer dan 90% (ECDC 2023). De virusuitscheiding en daarmee de besmettelijkheid van de persoon met mazelen is het hoogst rondom het begin van het exantheem (of de late prodromale fase) (Gershon 2021).
De besmettelijkheid van mensen met een doorbraakinfectie bij secundair vaccinfalen is zeer gering, omdat de symptomen over het algemeen milder zijn en de virale lading in de nasofarynx lager is dan bij primaire infectie (Fappani 2022, Sundell 2019, Tranter 2024). Zie ook de Onderbouwing BCO bij doorbraakinfecties.
Het mazelenvirus kan enkele uren op oppervlakken en in de lucht overleven (WHO 2024). Het mazelenvirus is echter niet stabiel; het is gevoelig voor alcohol 70%, zuur, (ultraviolet) licht, hitte en uitdroging. Als het virus hieraan wordt blootgesteld blijft het virus niet lang infectieus op oppervlakken en in de lucht. Bij een lage luchtvochtigheid kan het virus langer infectieus blijven (Beggs 2010, Gershon 2021, Moss 2024, Strebel 2018).
Risicogroepen
Verhoogde kans op infectie
Iedereen die niet beschermd is door vaccinatie of geen mazelen heeft doorgemaakt, kan mazelen krijgen. Dat zijn de volgende personen:
- kinderen die hun eerste BMR-vaccinatie (op 14 maanden) nog niet hebben gekregen en bij wie maternale antistoffen niet of niet meer aanwezig zijn (wat geldt voor de meerderheid van deze kinderen);
- ongevaccineerde personen die bijvoorbeeld vanwege een medische contra-indicatie of een andere reden (bijvoorbeeld om religieuze of antroposofische redenen) niet gevaccineerd zijn.
De kans op infectie is groter bij sociale of geografische clustering van niet-beschermde personen: clustering op scholen, kinderopvang, kerk of andere instellingen waar mensen die niet gevaccineerd zijn samenkomen. Zie ook de Arbeidsgerelateerde risicogroepen.
Verhoogde kans op ernstig beloop
De volgende personen hebben een verhoogde kans op ernstig beloop (CDC 2024, Gershon 2021):
- pasgeborenen en jonge kinderen (< 1 jaar): vooral pasgeborenen van niet-beschermde moeders hebben een verhoogde kans op ernstige complicaties en sterfte (zie ook Verhoogde kans op ernstig beloop bij zwangerschap);
- volwassenen: met de toename van de leeftijd (vanaf 20 jaar) is er een verhoogde kans op complicaties door een mazelenvirusinfectie (Hübschen 2022);
- immuungecompromitteerde personen: vooral bij personen met een verminderde cellulaire afweer; maar bij elke afweerstoornis is er een grotere kans op een ernstige progressieve mazelenvirusinfectie, mogelijk met fatale afloop;
- Zie ook Verhoogde kans op ernstig beloop bij zwangerschap.
In lage-inkomenslanden en conflictgebieden kan er sprake zijn van ondervoeding, dit kan leiden tot een afname van de cellulaire immuniteit. Bij ondervoeding in combinatie met ‘crowding’, waarbij er mogelijk een verhoogde blootststelling is aan het virus, is er kans op een ernstig beloop (CDC 2024, Gershon 2021).
Verhoogde kans op ernstig beloop bij zwangerschap
Risico voor de zwangere
Zwangeren met een mazelenvirusinfectie hebben een verhoogde kans op een ernstig beloop. Zij worden vaker opgenomen in het ziekenhuis en ontwikkelen vaker een pneumonie (10 tot 40 procent van de geïnfecteerde zwangeren) in vergelijking met niet-zwangeren. Hoewel de reden van opname vaak een pneumonie was, is in overige gevallen de reden van ziekenhuisopname niet gespecificeerd. Ook is de mortaliteit verhoogd bij zwangeren (3-15%), vergeleken met niet-zwangeren (Charlier 2021, Khalil 2024, Rasmussen 2015).
Risico voor het ongeboren kind
Mazelen veroorzaakt bij de foetus waarschijnlijk geen aangeboren afwijkingen. Enkele studies vinden wel een associatie tussen mazelen en een spontane abortus of vroeggeboorte (Khalil 2024, Rasmussen 2015).
Risico pasgeborene
Na intra-uteriene expositie kent mazelen bij de pasgeborene een kortere incubatieperiode; het klinische beeld kan variëren van mild tot ernstig en kan fataal verlopen (Orenstein 2023). Vanwege de verhoogde kans op vroeggeboorte heeft de pasgeborene een grotere kans op een laag geboortegewicht. Bij een perinatale infectie van de pasgeborene is er een grotere kans op een subacute scleroserende panencefalitis (SSPE) met een korte latentietijd en fulminant beloop (Khalil 2024, Rasmussen 2015).
Behandeling
Er zijn geen geneesmiddelen geregistreerd voor de behandeling van mazelen. Symptomatische behandeling bestaat uit bestrijding van koorts en dehydratie en het behandelen van bacteriële superinfecties. In lage-inkomenslanden en conflictgebieden wordt, gezien de vaak aanwezige pre-existente deficiëntie, vitamine A toegediend aan kinderen om de ernst van de ziekte te verminderen. Het exacte werkingsmechanisme van vitamine A op het verloop van mazelen is niet bekend (Gershon 2021, Hübschen 2022).
Diagnostiek
Zie mazelenvirus in het Diagnostisch vademecum (RIVM.nl).
Door een arts die ervaring heeft met mazelen is een klassiek mazelenbeeld met hoge koorts, hoesten, conjunctivitis, Koplikse vlekjes en een grofvlekkig exantheem beginnend achter de oren en in het gezicht te herkennen. Mazelen is echter een zeldzame ziekte geworden en verloopt lang niet altijd volgens het klassieke patroon, waardoor mazelen klinisch gemakkelijk verward kan worden met andere exantheemziekten. Bij patiënten met een donkere huidkleur is het exantheem vooral voelbaar. Daarom is bij het vermoeden van mazelen laboratoriumbevestiging geïndiceerd. Er kan in overleg met de GGD in geval van een uitbraak of epidemie van diagnostiek worden afgezien indien er een direct epidemiologisch verband is met een persoon waarbij de mazeleninfectie is bevestigd en er sprake is van milde klachten.
Microbiologische diagnostiek
Directe diagnostiek
Moleculaire diagnostiek (RT-PCR) is geschikt voor keeluitstrijk, speeksel, urine (bij voorkeur sedimenteren) en eventueel bloedmonsters (bij voorkeur (ethyleendiaminetetra-azijnzuur)-volbloed om witte bloedcellen te verkrijgen). De sensitiviteit van de RT-PCR is bij materiaal verkregen binnen 3 dagen na het optreden van exantheem hoger dan 80%. Bij later verkregen materiaal daalt de sensitiviteit snel (50% na 2 weken en lager dan 20% na 3 weken) (WHO 2008). In sommige gevallen kan viraal RNA worden gedetecteerd tot wel 5 (urine) en 7 (speeksel) weken na optreden van exantheem (Van Binnendijk 2003).
Aantonen mazelenvaccinvirus
Na vaccinatie met BMR (levend verzwakt virus) kan in urine en speeksel mazelenvirus-RNA worden gedetecteerd. Als een persoon recent een BMR-vaccinatie heeft gekregen, (mogelijk) ook is blootgesteld aan het mazelenvirus en daarna klachten krijgt die passen bij mazelen, kan onderzocht worden of de klachten komen door wildtype mazelenvirus of het mazelenvaccinvirus. Met een specifieke PCR is het mogelijk onderscheid te maken tussen het wildtype virus en de vaccinstam (na telefonisch overleg beschikbaar bij RIVM-IDS, zie Diagnostisch Vademecum).
Virusisolatie door middel van kweek wordt niet routinematig voor diagnostiek uitgevoerd. Detectie van virus door kweek is minder gevoelig dan RT-PCR (WHO 2008, Van Binnendijk 2003).
Indirecte diagnostiek
Recente infecties met mazelenvirus kunnen worden aangetoond door de aanwezigheid van mazelenvirus-specifieke IgM-antistoffen. Mazelenvirus-specifieke IgM-antistoffen uit serum, vingerprikbloed of speeksel kunnen tot 6 weken na ontstaan van exantheem worden aangetoond.
De sensitiviteit van IgM is > 60-70% bij monsters verzameld binnen 0-3 dagen na optreden exantheem en > 90% bij monsters verzameld tussen 4 en 28 dagen (WHO 2008). Foutpositieve IgM-uitslagen zijn mogelijk, onder andere door de aanwezigheid van reumafactor (WHO 2017). Bij enkel positieve serologie, zonder duidelijke epidemiologische link met een mazelenuitbraak, is bevestiging middels RT-PCR daarom zeer raadzaam. Bij combinatie van directe (RT-PCR) en indirecte (serologie) diagnostiek is mazelen in meer dan 99% van de gevallen te diagnosticeren. Confirmatie van laboratoriumuitslagen kan plaatsvinden bij het mazelen- en rodehondreferentielaboratorium van de wereldgezondheidsorganisatie (WHO) in Nederland, te weten RIVM-IDS en Erasmus (Medisch Centrum)-Viroscience.
Een recente mazelenvirusinfectie kan ook bewezen worden door een seroconversie of een significante stijging van mazelen-specifieke IgG-antistoffen in gepaarde acute en convalescente serummonsters. Ook hier geldt dat wanneer er geen epidemiologische link is met een bevestigde mazelenpatiënt of een uitbraak, aanvullende diagnostiek middels RT-PCR raadzaam is.
IgG aviditeitstest
Een anti-mazelen IgG aviditeitstest kan bij een (in het verleden) gevaccineerd persoon met een vastgestelde mazeleninfectie ingezet worden om onderscheid te maken tussen primair of secundair vaccinfalen (na telefonisch overleg beschikbaar bij RIVM-IDS). De aviditeit (sterkte van de binding aan het mazelenvirus) van IgG is laag tot 6 weken na primaire blootstelling of vaccinatie, daarom moet het onderzoek zo snel mogelijk na het optreden van klachten worden uitgevoerd (WHO 2018).
Typering voor bron- en contactonderzoek
Genotypering is mogelijk via het RIVM-IDS en Erasmus MC-Viroscience. Genotypering wordt in combinatie met epidemiologische gegevens gebruikt om transmissieketens te identificeren, en zo vast te stellen of er sprake is van een geïmporteerde of import-gerelateerde infectie, danwel of er endemische transmissie is van het virus (Rota 2009).
Bij alle solitaire gevallen, en voor ten minste twee gevallen in ieder epidemiologisch cluster, wordt daarom gevraagd aan de GGD om te zorgen dat materialen voor PCR (urine, speeksel en keeluitstrijk) worden ingestuurd naar het RIVM-IDS of Erasmus MC-Viroscience.
Niet-microbiologische diagnostiek
Niet van toepassing.
PBM-advies bij diagnostiekafname mazelen buiten het ziekenhuis
Diagnostiekafname buiten het ziekenhuis gebeurt in principe door beschermde zorgverleners. Zie hiervoor ook het kader Wie is beschermd? en de Bijlage Bescherming in de gezondheidszorg. Als de zorgverlener niet weet of hij/zij beschermd is (door vaccinatie of door mazelen doorgemaakt te hebben), dan wordt deze als niet beschermd beschouwd. Zorgverleners die niet beschermd zijn, nemen alleen bij hoge uitzondering diagnostiek af. Zorgverleners met een verhoogd risico op ernstig beloop van mazelen worden hiervoor nooit ingezet.
- Extramurale zorgverleners die beschermd zijn dragen bij afname van een keelwat een FFP2-masker en bij risico op spatten (hoesten, niezen) ook een spatbril.
- Niet-beschermde extramurale zorgverleners voeren diagnostiekafname uit met handschoenen, schort, FFP2-masker en bij risico op spatten een spatbril.
Preventie
Immunisatie
Vaccinatie
De BMR-vaccinatie wordt programmatisch aangeboden in het Rijksvaccinatieprogramma. Voor de indicaties, de geregistreerde vaccins, eigenschappen, doseringsschema, contra-indicaties, veiligheid, effectiviteit en beschermingsduur, zie Factsheet BMR-vaccinatie.
Als een kind voor de leeftijd van 14 maanden op reis gaat naar een land waar mazelen voorkomt, wordt geadviseerd een extra of vervroegde BMR-vaccinatie (een zogenaamde BMR-0) te geven. Zie voor BMR-vaccinatieadvies per land de BMR-landenlijst. In Nederland wordt er vervroegd gevaccineerd vanaf de leeftijd van 6 maanden. Vervroegd vaccineren heeft echter gevolgen voor de bescherming van het kind op langer termijn, zie hiervoor de Onderbouwing vervroegd vaccineren.
Vaccinfalen
Ook bij mazelenvaccinatie kan er sprake zijn van vaccinfalen, hierbij kan er sprake zijn van primair en secundair vaccinfalen. Bij primair vaccinfalen treedt er geen adequate immuunrespons op na vaccinatie(s). Secundair vaccinfalen wil zeggen dat er na vaccinatie(s) een adequate immuunrespons is opgetreden, desondanks wordt er toch mazelen opgelopen (Fappani 2022, Hahné 2016).
Indien er sprake is van secundair vaccinfalen heeft de geïnfecteerde persoon vaccin-geïnduceerde immuniteit opgebouwd. Er worden dan snel nieuwe antistoffen aangemaakt door memory B-cellen waardoor het virus ook sneller wordt geklaard. Door middel van de IgG-aviditeitstest kan onderzocht worden of er sprake is van secundair vaccinfalen. De antistoffen die opgewekt worden bij infectie hebben een relatief hoge aviditeit. Deze test is bij het RIVM beschikbaar en wordt op indicatie ingezet.
Mazelenverschijnselen na BMR-vaccinatie
Tussen 5 en 12 dagen na toediening van het BMR-vaccin kan de gevaccineerde symptomen ontwikkelen die lijken op de symptomen van mazelen, zoals koorts, exantheem en soms milde luchtwegklachten. Deze reactie wordt veroorzaakt door de verzwakte mazelenstam in het vaccin. Het onderscheid tussen bijwerkingen van het vaccin, eerder ook wel ‘vaccinitis’ genoemd, en een wildtype mazeleninfectie is klinisch vaak lastig te maken. Moleculair diagnostisch onderzoek kan in dergelijke gevallen uitsluitsel bieden, zie ook Directe diagnostiek. Mazelenverschijnselen die optreden als bijwerkingen van het vaccin zijn zelflimiterend en verlopen over het algemeen mild, en zonder complicaties. Er is geen sprake van transmissie naar anderen (Moorer 2011, Di Pietrantonj 2021, EMA 2025).
Passieve immunisatie
Mazelenimmunoglobuline heeft een specifieke immuniserende werking tegen het mazelenvirus. De antistoffen neutraliseren het virus, waardoor het niet meer kan binden aan de targetcellen. In Nederland is echter geen specifiek mazelenimmunoglobuline verkrijgbaar. Daarom wordt ter voorkoming van mazelen in bijzondere gevallen humaan gammaglobuline gegeven (Follin 2008, UKHSA 2024).
Buiten het ziekenhuis wordt dit humaan gammaglobuline intramusculair toegediend. Intramusculaire toediening geeft een snellere absorptie van de immunoglobulinen in vergelijking met subcutane toediening en wordt daarom verkozen boven subcutane toediening (UKHSA 2024). De beschikbare producten worden hieronder beschreven.
- Bij niet-beschermde immuungecompromitteerde contacten worden intraveneuze immunoglobulinen (IVIg) geadviseerd; bij intramusculaire toediening is de dosering te laag om ziekte te voorkomen. De indicatie voor intraveneus immunoglobuline (IVIg) wordt altijd gesteld door de behandelend arts en is afhankelijk van de ernst van immuunsuppressie en van de immuunstatus van het contact. Toediening van IVIg gebeurt in het ziekenhuis. Voor meer informatie zie Postexpositieprofylaxe, en voor de specificatie bij welke immuungecompromitteerde personen IVIg nodig kan zijn zie Postexpositieprofylaxebeleid mazelen bij immuungecompromitteerde contacten.
- Bij zuigelingen met afweerstoornissen en/of ander ernstig onderliggend lijden, is overleg met een kinderarts geïndiceerd. De indicatie voor intraveneus immunoglobuline (IVIg) wordt altijd gesteld door de kinderarts en gebeurt in het ziekenhuis. Meer informatie is te lezen in de Onderbouwing PEP zuigelingen (resultaten uitgangsvraag 3). De Bijlage Toedienen immunoglobuline bij zuigelingen bevat praktische adviezen die ondersteunend kunnen zijn bij de voorbereiding op en het uitvoeren van het toedienen van immunoglobuline bij zuigelingen.
Voor meer informatie over de indicaties van immunoglobuline, tijdsinterval tussen blootstelling en toediening en dosering, zie Postexpositieprofylaxe.
Beriglobin P
Beriglobin P heeft geen officiële indicatie voor mazelen-postexpositieprofylaxe en het gebruik hiervoor is off-label. De minimale beschermende dosis is 11 IU/kg (UKHSA 2024). Op basis van uitgevoerde anti-mazelentiterbepalingen in Beriglobin P is het volgende doseringsschema opgesteld:
- Zuigelingen: 0,7 ml/kg met een maximum van 6 ml, intramusculair. Eventueel in meerdere bovenbeenspieren toedienen. Het is te overwegen om de volledige dosis in de voorgevulde spuit (2 of 5 ml) toe te dienen. De toegediende dosis kan dan hoger liggen dan de aanbevolen dosering. Dit is niet schadelijk: er is geen risico op overdosering bij dit product. Zie ook de Bijlage Toedienen immunoglobuline bij zuigelingen.
- Niet-beschermde zwangeren: 15 ml intramusculair in 3 giften van 5 ml in meerdere bovenarm- of bovenbeenspieren. De maximale hoeveelheid van 15 ml zorgt voor volledige bescherming bij personen tot 21 kg. Bij zwangeren zal de toegediende dosis daarom niet compleet beschermend zijn, maar zal de ziekte-ernst verminderen.
Levering Beriglobin P
Beriglobin P (CSL Behring) kan bij twee groothandels besteld worden, namelijk Orly Pharma en Europort Pharmaceuticals. Beide groothandels verwerken alleen tijdens kantoortijden bestellingen; binnen dit kader kan wel met spoed/snel en ook buiten kantoortijden geleverd worden, tegen extra kosten. Omdat Beriglobin P niet in Nederland is geregistreerd, is de procedure van bestellen met artsenverklaring van toepassing. Bij Europort Pharmaceuticals kan Beriglobin P daarom alleen per e-mail besteld worden. De verwachting begin april 2025 is dat Beriglobin P op korte termijn niet meer in Nederland verkrijgbaar is, omdat CSL Behring gestopt is met de productie ervan.
Beriglobin P heeft ook een indicatie hepatitis A-profylaxe. Of er alternatieve producten hiervoor zijn, is nog niet duidelijk. Er zijn wel vervangende producten voor mazelen postexpositieprofylaxe beschikbaar (zie hierna). De (Gemeentelijke gezondheidsdienst)’en wordt daarom geadviseerd om de aanwezige Beriglobin P zo mogelijk te reserveren voor hepatitis A postexpositieprofylaxe en voor mazelenpostexpositieprofylaxe onderstaande producten te gebruiken.
Cutaquig
Cutaquig 165 mg/ml (Octapharma), verkrijgbaar in flacons van verschillende hoeveelheden, is in Nederland geregistreerd en beschikbaar. Net als Beriglobin P en Cuvitru kent het geen officiële indicatie voor mazelen-postexpositieprofylaxe en is het geregistreerd voor subcutane toediening. Intramusculaire toepassing voor mazelen-postexpositieprofylaxe is dan ook off-label.
De anti-mazelentiter van in Nederland beschikbare batches van 6 en 12 ml Cutaquig is door het (Rijksinstituut voor Volksgezondheid en Milieu) bepaald. Op basis daarvan is het volgende doseringsschema opgesteld, uitgaande van een minimale beschermende dosis van 11 IU/kg (UKHSA 2024):
- Zuigelingen: 0,6 ml/kg met een maximum van 6 ml. Eventueel in meerdere bovenbeenspieren toedienen. Het is te overwegen om de volledige inhoud van de flacon van 6 ml toe te dienen. De toegediende dosis kan dan hoger liggen dan de aanbevolen dosering. Dit is niet schadelijk: er is geen risico op overdosering bij dit product. Zie ook de Bijlage Toedienen immunoglobuline bij zuigelingen.
- Niet-beschermde zwangeren: 18 ml (6 en 12 ml) intramusculair toegediend in meerdere giften in meerdere bovenarm- of bovenbeenspieren. De maximale hoeveelheid van 18 ml zorgt voor volledige bescherming bij personen tot 30 kg. Bij zwangeren zal de toegediende dosis daarom niet compleet beschermend zijn, maar zal de ziekte-ernst verminderen.
Cuvitru
Cuvitru 200 mg/ml (Takeda), verkrijgbaar in flacons van verschillende hoeveelheden, is in Nederland geregistreerd en beschikbaar. Net als Beriglobin P en Cutaquig kent het geen officiële indicatie voor mazelen-postexpositieprofylaxe en is het geregistreerd voor subcutane toediening. Intramusculaire toepassing voor mazelen-postexpositieprofylaxe is dan ook off-label.
De anti-mazelentiter van in Nederland beschikbare batches van 5 en 10 ml Cuvitru is door het RIVM(Rijksinstituut voor Volksgezondheid en Milieu ) bepaald. Op basis daarvan is het volgende doseringsschema opgesteld, uitgaande van een minimale beschermende dosis van 11 IU/kg (UKHSA 2024):
- Zuigelingen: 0,6 ml/kg met een maximum van 5 ml. Eventueel in meerdere bovenbeenspieren toedienen. Het is te overwegen om de volledige inhoud van de flacon van 5 ml toe te dienen. De toegediende dosis kan dan hoger liggen dan de aanbevolen dosering. Dit is niet schadelijk: er is geen risico op overdosering bij dit product. Zie ook de Bijlage Toedienen immunoglobuline bij zuigelingen.
- Niet-beschermde zwangeren: 20 ml intramusculair toegediend in meerdere giften in meerdere bovenarm- of bovenbeenspieren. De maximale hoeveelheid van 20 ml zorgt voor volledige bescherming bij personen tot 33 kg. Bij zwangeren zal de toegediende dosis daarom niet compleet beschermend zijn, maar zal de ziekte-ernst verminderen.
Levering Cutaquig en Cuvitru
Voor Cutaquig en Cuvitru is geen artsenverklaring nodig, waardoor een (kleine) voorraad bij de GGD mogelijk is. Voor Cutaquig is Eurocept Pharmaceuticals de distributeur; Cuvitru wordt geproduceerd en gedistribueerd naar groothandels door Takeda. Voor beide producten geldt dat er niet direct aan GGD’en kan worden geleverd, maar dat de bestelling en levering via apotheken loopt.
Algemene preventieve maatregelen
Aangezien mazelen zeer besmettelijk is, zijn algemene hygiënemaatregelen zoals handen wassen en hoesthygiëne niet voldoende om transmissie te voorkomen. Personen met een verhoogd risico op ernstig beloop van mazelen, met name (nog) ongevaccineerde jonge kinderen, niet-beschermde zwangeren en immuungecompromitteerden, wordt geadviseerd contact met personen die mogelijk mazelen hebben te vermijden.
Reiniging, desinfectie en sterilisatie
Conform de LCI-richtlijn Reiniging, desinfectie en sterilisatie in de openbare gezondheidszorg.
Maatregelen
Meldingsplicht
Mazelen is een meldingsplichtige ziekte groep B2. Artsen en hoofden van laboratoria moeten bij vaststelling van de infectieziekte dit binnen 1 werkdag melden aan de (Gemeentelijke gezondheidsdienst). De GGD meldt gepseudonimiseerd conform de Wet publieke gezondheid binnen 24 uur aan het CIb en levert gegevens voor de landelijke surveillance van meldingsplichtige ziekten.
Als zich in een instelling, zoals een school of kinderopvang, twee of meerdere gevallen met overeenkomstige huidafwijkingen, zoals vlekjes die bij mazelen optreden, voordoen, is er sprake van de meldingsplicht op basis van artikel 26 van de Wet publieke gezondheid. Hoofden van instellingen waar voor infectieziekten kwetsbare populaties verblijven, dienen binnen 1 werkdag te melden bij de GGD, conform artikel 26 van de Wet publieke gezondheid. Zie het Draaiboek artikel 26 meldingen in Wpg-instellingen.
Meldingscriteria:
Een persoon met een herkenbaar begin van symptomen:
- koorts én een verheven maculopapuleuze uitslag
én ten minste 1 van de volgende 3 symptomen:
- hoesten
- neusverkoudheid
- conjunctivitis
én ten minste 1 van de volgende criteria:
- detectie van nucleïnezuur (RNA) van het mazelenvirus in een klinisch monster (PCR);
- detectie van mazelenspecifieke (immunoglobuline M)-antistoffen in serum, vingerprikbloed of speeksel;
- detectie van een significante stijging van mazelen specifieke (immunoglobuline G)-antistoffen in serum of vingerprikbloed;
- contact (< 3 weken) met een persoon bij wie de infectie is vastgesteld met behulp van laboratoriumdiagnostiek (epidemiologische link).
Extra verzoek bij ernstige complicaties en overlijden: Het verzoek aan behandelend artsen is om (1) ernstige complicaties waarvoor een opname nodig is en (2) overlijden ten gevolge van mazelen aanvullend te melden aan de GGD. Het verzoek aan de GGD’en is om deze informatie aan te vullen in de oorspronkelijke Osirismelding. Dit is belangrijk om de ziektelast door mazelen te kunnen monitoren in het kader van landelijke surveillance.
Bron- en contactonderzoek
Bronopsporing
Bronopsporing is de verantwoordelijkheid van de GGD nadat deze een melding van mazelen heeft ontvangen, waarbij vooral nagegaan moet worden of er sprake is van mogelijke import van de ziekte uit het buitenland.
Bij alle solitaire gevallen, en voor ten minste 2 gevallen in ieder epidemiologisch cluster, wordt gevraagd aan de GGD om te zorgen dat materialen voor PCR (urine, speeksel en keeluitstrijk) worden ingestuurd (zie Diagnostiek moleculaire typering) naar het (Rijksinstituut voor Volksgezondheid en Milieu)-IDS of Erasmus (Medisch Centrum)-Viroscience. Duidelijkheid over de mondiale transmissieroutes is van belang in het kader van het eliminatiestreven van de (World Health Organization).
Contactonderzoek
Naar aanleiding van een geval van mazelen moeten de contacten worden geïnventariseerd. Contacten worden als volgt gedefinieerd, in volgorde van urgentie:
- huishoudcontacten;
- nauwe contacten (anders dan huishoudcontacten) die langer dan 15 minuten dezelfde binnenruimte hebben gedeeld (zoals kinderopvang, school, werk);
- medisch en verzorgend personeel dat in contact is geweest met de indexpatiënt;
- wachtkamercontacten: personen met een verhoogd risico op een ernstig beloop van mazelen, die tot maximaal 2 uur na de index in de wachtkamer gezeten hebben (Beggs 2010, Gastañaduy 2018), zie ook de Bijlage Contactonderzoek wachtkamercontacten.
Bij een éénmaal (bof, mazelen, rodehond)-gevaccineerde index vindt regulier contactonderzoek plaats, omdat de kans op primair vaccinfalen bij personen met mazelen die eenmaal zijn gevaccineerd groter is dan bij tweemaal BMR-gevaccineerde personen met mazelen. In geval van primair vaccinfalen is deze persoon even besmettelijk als iemand die in het geheel niet is gevaccineerd.
Mazelenvirus-doorbraakinfectie
De kans op transmissie vanuit tweemaal gevaccineerde personen met een mazelenvirus-doorbraakinfectie wordt geacht zeer gering te zijn. Diverse studies opgenomen in een review tonen aan dat transmissie vrijwel alleen plaatsvindt bij langdurig en/of intensief contact, zoals in een huishouden of in een zorgsetting (Fappani 2022). Voor meer informatie zie de Onderbouwing BCO bij doorbraakinfecties. Het contactonderzoek bij een mazelen-doorbraakinfectie is als volgt:
- Bij een volledig (tweemaal BMR-) gevaccineerde persoon met een mazelenvirus-doorbraakinfectie kan het contactonderzoek buiten het ziekenhuis beperkt worden tot de huishoudcontacten. In uitzonderingsgevallen waarbij er intensief contact is geweest met een niet-beschermde, kwetsbare groep of persoon kan het contactonderzoek uitgebreid worden. Ook kan overwogen worden om een aviditeitstest te laten uitvoeren om onderscheid te maken tussen primair en secundair vaccinfalen, zie ook Diagnostiek en Preventie (Immunisatie). Bij primair vaccinfalen vindt regulier contactonderzoek plaats.
- Het contactonderzoek bij een mazelenvirusdoorbraakinfectie in het ziekenhuis ligt bij de afdeling infectiepreventie van het ziekenhuis.
Maatregelen ten aanzien van index, contacten en bron
Bij een solitaire patiënt met een klinisch beeld passend bij mazelen, die niet met laboratorium-bevestigde gevallen in verband gebracht kan worden, is het geïndiceerd om de diagnose eerst te laten bevestigen alvorens tot maatregelen over te gaan.
Als in een mazelencluster bij een aantal personen de diagnose via laboratoriumonderzoek is bevestigd, en een epidemiologische link met een nieuwe mazelenpatiënt voldoende waarschijnlijk is, kunnen rondom de nieuwe patiënt direct maatregelen worden genomen zonder te wachten op (aanvullend) laboratoriumonderzoek.
Bij een vermoeden van mazelen bij een persoon die recent een BMR-vaccinatie heeft ontvangen (bijvoorbeeld als postexpositieprofylaxe na blootstelling aan mazelen), moet worden afgewogen hoe groot de kans is dat de klachten door een mazelenvirusinfectie of door bijwerkingen van het vaccin worden veroorzaakt, zie ook Mazelenverschijnselen na BMR-vaccinatie. Overweeg laboratoriumonderzoek in te zetten om te bepalen of het gaat om het wildtype of vaccinstam mazelenvirus alvorens maatregelen te nemen, zie ook Directe diagnostiek. Bij personen met het vaccinstam-mazelenvirus is het niet nodig om maatregelen te nemen omdat er geen verdere transmissie plaatsvindt.
Maatregelen ten aanzien van index
Een persoon met mazelen dient in de besmettelijke periode (dus tot en met 4 dagen na het ontstaan van het exantheem) contact te vermijden met personen met een verhoogd risico op ernstig beloop. Dit betreft met name (nog) ongevaccineerde jonge kinderen, niet-beschermde zwangeren en immuungecompromitteerde personen. In de praktijk houdt dit in dat het wordt aangeraden thuis te blijven. Dit geldt ook voor gevaccineerde gevallen met een mazelen-doorbraakinfectie.
Indien de index of contact een arbeidsmigrant betreft, zie de Bijlage Mazelen bij arbeidsmigranten voor aandachtspunten en adviezen.
In een klinische situatie verblijft de patiënt tot en met 4 dagen na uitbreken van exantheem in isolatie. Zie ook de Bijlage Bescherming tegen mazelen in de gezondheidszorg en de de SRI-richtlijn Isolatie.
Maatregelen ten aanzien van contacten
Voor niet-beschermde contacten zijn er maatregelen nodig in de vorm van vaccinatie of het toedienen van immunoglobuline (zie Postexpositieprofylaxe). Zie onderstaand kader Wie is beschermd voor een overzicht van wie als beschermd tegen mazelen kan worden beschouwd.
Postexpositieprofylaxe
Postexpositieprofylaxe is geïndiceerd bij niet-beschermde contacten. Zie het kader Wie is beschermd tegen mazelen hieronder om de immuniteit te bepalen. Als een contact ooit 1 vaccinatie heeft gehad, is verdere postexpositieprofylaxe niet nodig, tenzij het contact:
- immuungecompromitteerd is;
- opgenomen is in het ziekenhuis of werkt in de gezondheidszorg (zie Bijlage Bescherming tegen mazelen in de gezondheidszorg);
- werkt met kinderen tot 14 maanden (zie Bijlage Bescherming tegen mazelen in de kinderopvang).
In geval van een indicatie voor postexpositieprofylaxe, wordt in principe BMR-vaccinatie gegeven.
Bij de volgende groepen met een verhoogde kans op een ernstig beloop bij wie BMR-vaccinatie gecontra-indiceerd is of niet werkzaam is, wordt immunoglobuline gegeven:
- Zuigelingen tot 6 maanden en indien gezinscontact tot en met 8 maanden;
- Niet-beschermde zwangeren (niet gevaccineerd en geen mazelen doorgemaakt);
- Niet-beschermde immuungecompromitteerden.
Wie is beschermd tegen mazelen?
Wie is beschermd tegen mazelen?
- Personen die mazelen hebben doorgemaakt. Als beschermd worden beschouwd:
- Personen geboren voor 1965 (toen was er uitgebreide circulatie van mazelen)
- Personen geboren tussen 1965 en 1975 die anamnestisch mazelen hebben doorgemaakt*
- Ongevaccineerde kinderen en volwassenen binnen de reformatorische gezindte die anamnestisch mazelen hebben doorgemaakt
- Ongevaccineerde personen met een gedocumenteerde immuniteit tegen mazelen (meestal: (immunoglobuline G) tegen mazelen positief).
- Personen die zijn gevaccineerd. Als beschermd worden beschouwd:
- Personen geboren vanaf 1975 die gevaccineerd zijn volgens het Rijksvaccinatieprogramma:
- 1 mazelen- of BMR-vaccinatie geeft aan 95% van deze personen bescherming;
- 2 mazelen- of BMR-vaccinaties geeft aan 99% van deze personen bescherming.
- Personen die (gedocumenteerd) gevaccineerd zijn buiten het Rijksvaccinatieprogramma, bijvoorbeeld personen die via de huisarts, arbodienst of in het kader van reizen gevaccineerd zijn.
- Personen geboren vanaf 1975 die gevaccineerd zijn volgens het Rijksvaccinatieprogramma:
* Omdat mazelen zeer besmettelijk is, hebben de meeste volwassenen geboren voor 1965 de ziekte doorgemaakt en als gevolg daarvan natuurlijke immuniteit verworven. Volwassenen geboren tussen 1965 en 1975 zijn mogelijk minder goed beschermd omdat er in hun kinderjaren ten gevolge van de vaccinatie minder circulatie van het mazelenvirus was.
Aanvullende indeling voor specifieke groepen werknemers en patiënten die zijn opgenomen in het ziekenhuisVoor werknemers in de kinderopvang die werken met kinderen tot 14 maanden, werknemers in de gezondheidszorg of patiënten die zijn opgenomen in het ziekenhuis wordt een extra onderverdeling gemaakt.
- Voor deze groepen geldt dat alleen het doormaken van mazelen of het gevaccineerd zijn met 2 mazelen- of BMR-vaccinaties als voldoende bescherming wordt beschouwd.
- Een eenmalige vaccinatie bij iemand die geen mazelen heeft doorgemaakt wordt als matig-beschermd beschouwd.
- Geboren na 1-1-1975 en voor 1-1-1978: 1x mazelenvaccin
- Geboren na 1-1-1978 en voor 1-1-1983: 1x mazelenvaccin bij 14 mnd en 1x (bof, mazelen, rodehond) bij 9 jaar
- Geboren na 1-1-1983 en voor 1-1-1986: 2x BMR (inhaalcampagne)
- Geboren na 1-1-1986 en voor 1-1-2016: 2x BMR, bij 14 mnd en 9 jaar
- Geboren na 1-1-2016 en voor 1-1-2022: 2x BMR, bij 14 mnd en voor 2e vaccinatie zie Rijksvaccinatieprogramma
Geboren na 1-1-2022: 2x BMR, bij 14 mnd en rond de 3e verjaardag (huidige reguliere (Rijksvaccinatieprogramma)).
Tijdstip van toediening van postexpositieprofylaxe
Zowel immunoglobuline als BMR-vaccinatie worden bij voorkeur zo snel mogelijk toegediend na eerste blootstelling voor de beste effectiviteit. De berekening van het tijdstip van toediening is afhankelijk van de setting.
- Bij gezinscontacten wordt de periode waarbinnen het zinvol is om postexpositieprofylaxe toe te dienen berekend vanaf de dag dat het exantheem ontstond. De virusuitscheiding en daarmee de besmettelijkheid van een mazelenpatiënt is namelijk het hoogst rondom het begin van het exantheem. Zie ook de Onderbouwing PEP bij contacten (resultaten uitgangsvraag 3).
- Voor settings anders dan binnen het gezin kan gerekend worden vanaf de laatste blootstellingsdag in de besmettelijke periode van de index. Het advies blijft echter, ongeacht type setting, om de postexpositieprofylaxe zo snel mogelijk na eerste blootstelling toe te dienen voor de hoogste effectiviteit.
Tijdstip (bof, mazelen, rodehond)-vaccinatie
- Vaccinatie wordt bij voorkeur zo spoedig mogelijk gegeven, liefst binnen 72 uur na blootstelling.
- Toediening ook binnen 72 uur voorkomt niet altijd ziekte. Mogelijk kan vaccinatie het aantal dagen koorts en de hoogte van de koorts verminderen, dit effect is echter onzeker (Sakuta 2008). Er kunnen geen uitspraken gedaan worden over het effect op het optreden van ernstige ziekte/complicaties.
- Bij voortdurende blootstelling zoals tijdens een uitbraak kan vaccinatie, ook later dan 72 uur na het eerste contact, nog zinvol zijn om tertiaire infecties te voorkomen (UKHSA 2024). Voor gezinscontacten is BMR-vaccinatie na 72 uur niet zinvol.
Tijdstip immunoglobuline
- Immunoglobuline wordt het liefst binnen 72 uur maar uiterlijk tot en met 6 dagen na blootstelling toegediend. Toediening van immunoglobulinen aan niet-immune personen als PEP tot en met dag 6 na mazelenblootstelling is in oudere onderzoeken effectief gebleken tegen mazelenvirusinfectie en ook tegen mortaliteit (Young 2014).
- Bij voortdurende intensieve blootstelling dient de toediening van immunoglobuline elke 3-4 weken herhaald te worden.
- In uitzonderlijke gevallen kan latere toediening overwogen worden bij ernstig immuungecompromitteerde personen (zie Postexpositiebeleid immuungecompromitteerde contacten).
Zie Passieve immunisatie voor het doseringsschema, de beschikbaarheid en de verkrijgbaarheid van immunoglobuline.
PEP bij kinderen tot 14 maanden
- Bij kinderen tot 14 maanden met afweerstoornissen en/of ander ernstig onderliggend lijden is overleg met een kinderarts geïndiceerd. De indicatie voor intraveneus immunoglobuline (IVIg) wordt altijd gesteld door de kinderarts en gebeurt in het ziekenhuis.
- Bij overige kinderen tot 14 maanden gelden de volgende adviezen:
| Type contact | 0 tot 6 maanden | 6 tot en met 8 maanden | 9 tot 14 maanden |
|---|---|---|---|
| Immunoglobuline idealiter < 72 uur, maar tot en met 6 dagen vanaf start exantheem index, tenzij moeder mazelen heeft doorgemaakt en zuigeling < 2 maanden; de zuigeling is dan tot en met 2 maanden beschermd door maternale antistoffen. | Immunoglobuline* idealiter < 72 uur, maar tot en met 6 dagen vanaf start exantheem index, onafhankelijk van bescherming moeder. | BMR-vaccinatie liefst < 72 uur vanaf start exantheem index. Vaccineren mitigeert mogelijk eventuele ziekte. |
| Immunoglobuline < 72 uur tot en met 6 dagen vanaf (laatste) blootstelling, tenzij moeder mazelen heeft doorgemaakt; de zuigeling is dan tot en met 2 maanden beschermd door maternale antistoffen. | BMR-vaccinatie** liefst < 72 uur na (laatste) blootstelling, maar anders ook daarna om herintroductie op de kinderopvang te voorkomen. Vaccineren mitigeert mogelijk eventuele ziekte. | |
Na toediening van immunoglobuline dient BMR-vaccinatie bij voorkeur minimaal 3 maanden te worden uitgesteld. Wanneer direct bescherming tegen mazelen nodig is, bijvoorbeeld bij doorgaande transmissie, kan overwogen worden BMR-vaccinatie eerder toe te dienen, vanaf de leeftijd van 6 maanden (Burgmeijer 2011, UKHSA 2019).
Indien een BMR-vaccinatie wordt toegediend vóór de leeftijd van 1 jaar wordt deze vaccinatie als extra beschouwd. Het kind volgt verder het gebruikelijke schema van het (Rijksvaccinatieprogramma) en krijgt (opnieuw) een BMR-vaccinatie op de leeftijd van 14 maanden. BMR-vaccinatie toegediend na de 1e verjaardag en voor de leeftijd van 14 maanden kan de 1e BMR-vaccinatie in het kader van het RVP vervangen.
overwegingen
Bij het postexpositieprofylaxebeleid bij zuigelingen wordt rekening gehouden met de mate (type en duur) van blootstelling, eventuele bescherming door maternale antistoffen in de eerste levensmaanden, de verminderde vaccineffectiviteit van (bof, mazelen, rodehond)-vaccinatie bij zuigelingen onder de leeftijd van 12 maanden, en het feit dat immunoglobulinen slechts tijdelijke bescherming bieden en herbesmetting en/of herintroductie niet tegen gaan.
Mate van blootstelling
Het besmettingsrisico is het grootst onder gezinscontacten, omdat er sprake is van meerdaagse intensieve blootstelling met een toenemende virale blootstelling. Ook bij mazelen op de kinderopvang is er sprake van een reëel besmettingsrisico als de zuigeling op dezelfde groep 1 of meerdere volle dagen is blootgesteld aan een kind met mazelen. Bij overige nauwe contacten (> 15 minuten in dezelfde ruimte) is het besmettingsrisico lager.
Maternale antistoffen
Alleen indien de moeder een mazelenvirusinfectie heeft doorgemaakt, kan de zuigeling tot en met 2 maanden na de geboorte als beschermd beschouwd worden door maternale antistoffen. Zie Natuurlijke immuniteit Immuniteit foetus en/of pasgeborene.
Vaccineffectiviteit onder de leeftijd van 12 maanden
Indien de eerste mazelenvaccinatie voor de leeftijd van 1 jaar wordt toegediend, is op langere termijn de bescherming mogelijk minder goed. Deze effecten zijn het grootst bij vaccineren op een leeftijd van 6 maanden en nemen af naarmate er op latere leeftijd gevaccineerd wordt. Dit heeft waarschijnlijk te maken met de rijping van het afweersysteem en de aanwezigheid van moederlijke antistoffen.
Geschat wordt dat de bescherming rond 76 procent bij 6 maanden zit en oploopt tot 95 procent bij 9 maanden, met blijvend verminderde antistoftiters op latere leeftijd, ook na vervolgvaccinatie(s).
Bij het aanbieden van een extra vaccinatie moet het risico van het krijgen van mazelen op korte termijn - en dus de noodzaak voor onmiddellijke bescherming - afgewogen worden tegen de mogelijk minder goede bescherming op lange termijn. Voor kinderen met een hoog risico op blootstelling aan mazelen weegt het positieve aspect van snelle bescherming op tegen het negatieve aspect van mogelijk lagere antistoftiters tegen mazelen op de lange termijn. Als er geen direct risico is om mazelen op te lopen, geeft vaccinatie op de leeftijd van 14 maanden optimale bescherming. Zie Onderbouwing.
PEP bij niet-beschermde zwangeren
Er is een contra-indicatie voor (bof, mazelen, rodehond)-vaccinatie bij zwangeren. Bij blootstelling wordt daarom immunoglobuline gegeven. In de paragraaf Passieve immunisatie staat bij de productinformatie van de immunoglobuline het doseringsschema voor niet-beschermde zwangeren beschreven.
PEP bij immuungecompromitteerden
Bij immuungecompromitteerde personen is er een verhoogde kans op een gecompliceerd beloop van mazelen als er geen immuniteit tegen mazelen aanwezig is óf als deze door ziekte of behandeling verdwenen is of onderdrukt wordt. Bij voorkeur is al bekend of de patiënt ooit tegen mazelen is gevaccineerd en of er (nog) een anti-mazelen antistofconcentratie aanwezig is na een behandeling waarbij immuniteit verloren kan gaan (b.v. stamceltransplantatie, leukemiebehandeling). De (Gemeentelijke gezondheidsdienst) kan overleggen met de behandeld arts indien een contact immuungecompromitteerd is. Dit overleg kan betrekking hebben op aspecten als:
- de mate van immuunsuppressie
- de (actuele) dosering en duur van immuunsuppressieve behandeling
- de uitslag van een serologische test tegen mazelen
Bij blootstelling aan mazelen en onduidelijkheid over de immuniteit tegen mazelen, wordt cito een (immunoglobuline G)-antistoftiter bepaald. Als de antistoftiter te laag is, wordt intraveneus immunoglobuline (IVIg) gegeven in het ziekenhuis tot en met dag 6 na blootstelling. Alleen bij ernstig immuungecompromitteerde patiënten zou het tot en met dag 18 na blootstelling nog toegediend kunnen worden. Er is een contra-indicatie voor BMR-vaccinatie bij immuungecompromitteerden. De antistoftiter-bepaling, het toedienen van de immunoglobuline en de instructie tot monitoring op het ontstaan van klachten passend bij een eventuele mazelenvirusinfectie tot 28 dagen na laatste blootstelling, gebeurt, na overleg, in de tweede of derde lijn. Zie voor het beleid bij immuungecompromitteerden de bijlage Postexpositieprofylaxe mazelen bij immuungecompromitteerde contacten.
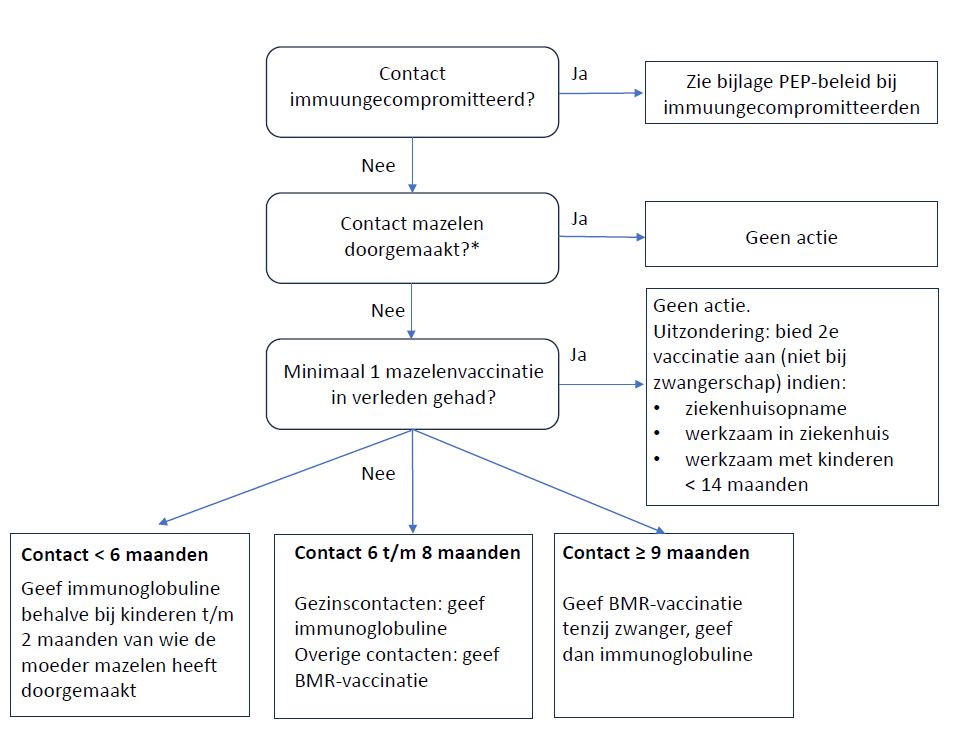
Stroomschema (postexpositieprofylaxe) contacten
Het hierboven beschreven beleid is samengevat in het stroomschema hieronder.
Afbeelding: Stroomschema PEP-contacten
* Zie ook: Wie is beschermd tegen mazelen?
Wering
Wering personen met mazelen van kinderopvang of school
Geadviseerd wordt om kinderen met mazelen te weren van de kinderopvang of school tot en met 4 dagen na het ontstaan van het exantheem (einde besmettelijke periode). Kinderen met mazelen voelen zich vaak te ziek om naar de kinderopvang of school te gaan en zullen in de praktijk vaak pas terugkeren na volledig herstel.
Mazelen is zeer besmettelijk al vanaf 4 dagen voor het ontstaan van het exantheem. Besmetting van mensen in de nabije omgeving heeft dus vaak al plaatsgevonden voordat de diagnose is gesteld. Bij een kinderopvang is weren echter alsnog zinvol vanwege wisselende aanwezigheid van kinderen en/of wanneer er een groot aantal ongevaccineerde kinderen op de groep verblijven. Zeker als het kind gedurende de 4 dagen voorafgaand aan het ontstaan van het exantheem elders verbleef, is wering zinvol om secundaire gevallen te voorkomen. Daarnaast zijn er op de kinderopvang vaak ongevaccineerde kinderen tot 14 maanden aanwezig.
Het weren van kinderen met mazelen op basis- en middelbare scholen is extra van belang als het kind in de besmettelijke periode niet aanwezig is geweest, en als er veel ongevaccineerden op school aanwezig zijn. Het weren van kinderen met mazelen beperkt verdere verspreiding.
Wering van niet-beschermde gezinscontacten van een persoon met mazelen
Geadviseerd wordt om niet-beschermde gezinscontacten te weren van de kinderopvang gedurende 14 dagen, gerekend vanaf de het ontstaan van exantheem bij het gezinslid met mazelen om besmetting van nog niet gevaccineerde kinderen te voorkomen. Daarnaast kan het verdere transmissie beperken. Ook op basis- en middelbare scholen kan dit geadviseerd worden om transmissie te beperken.
Wering niet-beschermde personen gedurende een epidemie
Het weren van niet-beschermde kinderen (ongevaccineerd en geen doorgemaakte mazelen) van de kinderopvang of school ten tijde van een mazelenepidemie wordt niet zinvol geacht. Dit zou een zeer ingrijpende en langdurige maatregel zijn met een twijfelachtig effect. Transmissie van mazelenvirus vindt ook buiten deze instellingen plaats, zoals via familiecontacten, buurtcontacten, kerken en verenigingen.
Wering van werk
Voor werknemers die zijn blootgesteld aan mazelen en matig (eenmaal gevaccineerd) of niet immuun zijn voor mazelen, kunnen maatregelen van toepassing zijn. Voor meer informatie, zie Wering van werk.
Arbeidsrelevante aanvullingen
Deze aanvullingen zijn geschreven voor en door bedrijfsartsen en beschrijven de preventieve maatregelen om het oplopen van infectieziekten tijdens het werk te voorkomen (werknemer als risicoloper) en de maatregelen/aanpassingen die genomen kunnen worden bij vaststelling van de infectieziekte bij de werknemer (werknemer als risicovormer). In de werksituatie gelden de Arbowet, het Arbeidsomstandighedenbesluit (Arbobesluit) en de Europese Richtlijn 2000/54 gericht op preventie. Zie ook biologische agentia in de wet (Arboportaal.nl).
tekst arbo
Ziekteverschijnselen in relatie tot werk
Zie de paragraaf Ziekteverschijnselen. Doorgaans zal er bij een werknemer met een mazelenvirusinfectie sprake zijn van een aanzienlijke ziektelast die tijdelijk zal leiden tot arbeidsongeschiktheid.
Arbeidsgerelateerde risicogroepen
Risicolopers
Beroepsgroepen met een verhoogde kans op beroepsmatige blootstelling zijn:
- werknemers in de gezondheidszorg en (para)medische studenten (Chen 2011, Gohil 2015, Maltezou 2013, Muscat 2011, Steingart 1999)
- werknemers die frequent reizen naar of verblijven in endemische gebieden, zoals arbeidsmigranten (in de Bijlage Mazelen bij arbeidsmigranten staan aandachtspunten en adviezen over mazelen bij arbeidsmigranten), zakenreizigers (ECDC 2019, Jost 2015, Kessler 2009) en werknemers van luchtvaartmaatschappijen of cruiseschepen (Croteau 2009, Kobayashi 2020)
- werknemers betrokken bij de vluchtelingenopvang
- werknemers van scholen en kinderopvang met name in regio’s met lage vaccinatiegraad (Jackson 1996, Kessler 2009).
Blootgestelde werknemers kunnen mazelen oplopen als zij niet beschermd zijn. Raadpleeg hiervoor het overzicht Wie is beschermd tegen mazelen.
Risicovormers
Dit zijn vatbare (niet of onvoldoende beschermde) werknemers die werken met kwetsbare groepen. Dit betreft personen werkzaam:
- in de zorg (met name op de kinder-, neonatologie-, kraam- en verloskundeafdeling en afdelingen met immuungecompromitteerde patiënten)
- in de kinderopvang en op consultatiebureaus (Botelho-Nevers 2011, Chen 2011, Fu 2019, Muscat 2011).
Werknemers met een verhoogde kans op ernstig beloop
Voor (medische) risicogroepen zie Verhoogde kans op beloop en Risico's mazelen tijdens de zwangerschap. In de (Risico-inventaristie en evaluatie) moet rekening gehouden zijn met de medische risicogroepen en de demografie van de werknemerspopulatie.
Preventieve maatregelen op het werk
Volg de Algemene preventieve maatregelen. Volg bij de preventieve maatregelen op het werk de bio-arbeidshygiënische strategie op Arboportaal. Mazelen valt onder categorie 2 van de biologische agentia van de EU-richtlijn 2019. De combinatie van onderstaande preventieve maatregelen op het werk heeft het doel het risico op besmetting van werknemer te minimaliseren.
- Bij een verhoogd risico op beroepsmatige blootstelling aan mazelen (risicoloper), of als de kans op beroepsmatige overdracht naar kwetsbare derden aanwezig is (risicovormer) dient de werkgever:
- Bij herhaling goede voorlichting te geven over infectierisico’s, wijze van transmissie, hygiënemaatregelen en bescherming door vaccinatie.
- Vaccinatie aan te bieden. Dit is een effectieve preventieve maatregel. Zie onder Vaccinatie werknemers.
- Erop toe te zien dat algemene hygiënische maatregelen consequent worden nageleefd.
- Bij verzorging of verpleging van een patiënt met bekende of vermoedelijke mazelen geldt daarnaast dat:
- Infectiepreventie- en beschermende maatregelen worden toegepast, persoonlijke beschermingsmiddelen op de juiste wijze worden gedragen en van toepassing zijnde isolatiemaatregelen consequent worden gevolgd. Zie SRI-richtlijn Isolatie.
- Onbeschermde werknemers een patiënt niet behandelen/verzorgen (UKHSA 2024, CDC 2025). Als hier in noodsituaties van wordt afgeweken dienen goed passende persoonlijke beschermingsmaatregelen strikt te worden gebruikt. Hierbij moet op correct gebruik te worden toegezien en dient werknemer zorgvuldig te zijn voorgelicht over het risico om mazelen op te lopen en over de mogelijkheid tot vaccinatie. Onbeschermde werknemers met een verhoogd persoonlijk risico, zoals zwangere en immuungecompromitteerde werknemers, dienen ook in noodsituaties niet te worden ingezet bij de verzorging of behandeling van een mazelenpatiënt.
- Bij afname van diagnostiek moeten beschermende maatregelen worden genomen: zie PBM-advies bij diagnostiekafname buiten het ziekenhuis.
Vaccinatie werknemers
Bij een verhoogd risico op beroepsmatige blootstelling aan mazelen (risicoloper), of als de kans op beroepsmatige overdracht naar kwetsbare derden aanwezig is (risicovormer), dient bij indiensttreding de immuun- en vaccinatiestatus te worden vastgelegd. Werkgever kan zich hierbij laten bijstaan door de arbodienst of bedrijfsarts bij de implementatie hiervan in lijn met de wet Algemene Verordening Gegevensbescherming (AVG).
Bij onvoldoende bescherming moet, na goede voorlichting hierover en bij ontbreken van contra-indicaties, vaccinatie worden aangeboden. Daarbij is extra aandacht nodig voor zwangere en immuungecompromitteerde werknemers binnen deze groep. Zie ook Factsheet BMR-vaccinatie.
- Onbeschermde werknemers krijgen een volledige vaccinatie aangeboden, bestaande uit 2 BMR-vaccinaties met een tussenpoos van ten minste 1 maand.
- Werknemers die in het verleden éénmaal zijn gevaccineerd tegen mazelen worden als voldoende beschermd beschouwd, tenzij zij werken in de gezondheidszorg of in de kinderopvang met kinderen jonger dan 14 maanden. Hen wordt een 2e BMR-vaccinatie geboden.
- Voor gezondheidszorgwerkers: zie Bijlage Bescherming tegen mazelen in de gezondheidszorg. Zie ook het Arbo-infact Gezondheidszorgmedewerkers en mazelen (2024).
- Voor de kinderopvang: zie Bijlage Bescherming tegen mazelen voor werknemers in de kinderopvang.
Preventieve maatregelen bij kinderwens, zwangerschap of lactatie
De werkgever is in het kader van het Arbeidsomstandighedenbesluit 4.85 verantwoordelijk voor de bescherming van werknemers in het algemeen en zwangere medewerkers in het bijzonder (Arbobesluit 4.107). Zie ook het HSE-artikel Zwangerschap en werk.
Werkgevers actief in de zorg, vluchtelingenopvang, kinderopvang, onderwijs en met werknemers die beroepsmatig reizen naar endemische gebieden dienen, bij voorkeur bij aanstelling, werknemers te wijzen op het anonieme (preventieve) arbeidsomstandighedenspreekuur bij de bedrijfsarts. Werknemers kunnen hier terecht met vragen over arbeidsomstandigheden in relatie tot o.a. zwangerschapswens, zwangerschap of lactatie.
Maatregelen en wering van werk
Postexpositieprofylaxe na blootstelling op werk
- Voor werknemers in de gezondheidszorg zie Bijlage Bescherming tegen mazelen in de gezondheidszorg.
- Voor werknemers in de kinderopvang zie Bijlage Bescherming tegen mazelen voor werknemers in de kinderopvang.
- Voor overige werknemers: volg het postexpositieprofylaxebeleid in settings anders dan gezinscontacten.
Wering van werk
Wering van werk na blootstelling is van toepassing. Hierbij wordt onderscheid gemaakt tussen wering van werk van 1) werknemers in de gezondheidszorg die werken met kwetsbare groepen en 2) andere werknemers met beroepsmatig contact met anderen.
1. Werknemers in de gezondheidszorg die werken met kwetsbare groepen
Matig of niet-beschermde werknemers in de gezondheidszorg werkend op risicoafdelingen in het ziekenhuis worden geweerd van dit werk vanaf dag 5 tot 18 dagen. Dit tenzij zij direct na blootstelling (in ieder geval binnen 7 dagen na eerste blootstelling) positief zijn getest op mazelen-IgG. Een positieve mazelen-IgG binnen 7 dagen na eerste blootstelling wordt als te vroeg beschouwd om dit toe te kunnen schrijven aan deze recente blootstelling. In dat geval worden zij als beschermd beschouwd (UKHSA 2024).
Zorgverleners met voldoende bewijs van bescherming kunnen normaal blijven werken, tenzij zij koorts of huiduitslag ontwikkelen. Dan moeten zij alsnog worden geweerd van werk tot en met 4 dagen na het begin van de huiduitslag. Zie Bijlage Bescherming tegen mazelen in de gezondheidszorg.
Voor werknemers in de gezondheidszorg buiten het ziekenhuis die werken met de meest kwetsbare groep wordt hetzelfde weringsadvies geadviseerd.
2. Andere werknemers met beroepsmatig contact met anderen
Andere, matig of niet-beschermde medewerkers in de gezondheidszorg en in de kinderopvang moeten bij de eerst mogelijke symptomen van ziekte geweerd worden van werk. Zie Bijlage Bescherming tegen mazelen in de gezondheidszorg en Bijlage Bescherming tegen mazelen voor werknemers in de kinderopvang.
Dit geldt ook voor andere blootgestelde vatbare werknemers met direct contact met derden.
Melden als beroepsziekte
Indien de ziekte (waarschijnlijk) is opgelopen tijdens de beroepsuitoefening is de bedrijfsarts verplicht (Arbeidsomstandighedenwet, artikel 9.3) dit (online) te melden bij het Nederlands Centrum voor Beroepsziekten.
Tijdens de epidemie van 2013/2014 zijn bij het (Rijksinstituut voor Volksgezondheid en Milieu) 19 werknemers in de gezondheidszorg gemeld die tijdens hun werk mazelen hadden opgelopen. Na de epidemie van 2013/2014 zijn bij het (Nederlands Centrum voor Beroepsziekten) zijn 3 beroepsziekten gemeld door mazelen, de laatste was in 2018 (zie website NCvB). Het NCvB heeft te maken met structurele onderrapportage.
Wettelijk kader
Werkgevers en werknemers dragen samen de verantwoordelijkheid voor veilig en gezond werken. Dit is belangrijk voor goede werkomstandigheden en de continuïteit van bedrijfsvoering. Ze maken samen afspraken over veilige werkwijzen en het gebruik van beoordelingsinstrumenten hiertoe. De werkgever moet bij het beheersen van werkgebonden infectieziekten dusdanige maatregelen treffen dat de kans op blootstelling aan (en vervolgens mogelijke transmissie van) een agens in het werk zo laag mogelijk is.
Het risico op besmetting wordt bepaald door de kans op aanwezigheid van het agens bij een bron (bijvoorbeeld een kind met mazelen, de aard van de werkzaamheden (dit bepaalt de kans op overdracht) en de kwetsbaarheid van de werknemer (dit bepaalt in welke mate deze ontvankelijk is/gezondheidsrisico loopt).
Infectieziekten vallen binnen de Arbeidsomstandighedenwet onder biologische agentia, De zorglicht van de werkgever wordt hierin nader uitgewerkt. Middels een Risico-Inventarisatie en Evaluatie (RI&E) beoordeelt de werkgever de risico’s en stelt vervolgens beleid op. Hieruit volgt een plan van aanpak. Bestaat er een gezondheidsrisico voor de werknemer, dan neemt de werkgever (voor zover dit technisch uitvoerbaar is) zodanige maatregelen dat blootstelling aan het agens wordt voorkomen.
Daarbij staat bronaanpak voorop, gevolgd door (collectieve) technische en organisatorische maatregelen; persoonlijke beschermingsmiddelen en vaccinatie vormen het sluitstuk. In artikel 4.91 van het Arbeidsomstandighedenbesluit staat dat werknemers in de gelegenheid moeten worden gesteld voorafgaand aan of volgend op blootstelling aan biologische agentia arbeidsgezondheidskundig onderzoek te ondergaan.
Daarnaast dienen, voor zover mogelijk, aan iedere werknemer die nog niet immuun is voor het betreffende agens, doeltreffende vaccins ter beschikking te worden gesteld (lid 6). De werkgever kan hierbij voor het bepalen van het risico voor de kwetsbare derden gebruik maken van het afwegingskader zoals beschreven in tabel 1 Criteria voor vaccinatie uit het Gezondheidsraadadvies Werknemers en infectieziekten.
Literatuur
- Beersma MF, Kapsenberg JG, Renier WO, Galama JM, van Druten JA, Lucas CJ. Subacute scleroserende panencephalitis in Nederland (1976-1986). Ned Tijdschr Geneeskd. 1988;132:1194-9.
- Beggs CB, Shepherd SJ, Kerr KG. Potential for airborne transmission of infection in the waiting areas of healthcare premises: stochastic analysis using a Monte Carlo model. BMC Infect Dis. 2010;10:247. https://doi.org/10.1186/1471-2334-10-247
- Botelho-Nevers E, Cassir N, Minodier P, Laporte R, Gautret P, Badiaga S, et al. Measles among healthcare workers: a potential for nosocomial outbreaks. Euro Surveill. 2011;16(2).
- Burgmeijer R, Hoppenbrouwers K. Handboek vaccinaties: Van Gorcum; 2011.
- CDC. Fast facts: global measles 2024. Beschikbaar via: https://www.cdc.gov Geraadpleegd op 4-11-2024.
- CDC. Global measles outbreaks 2024. Beschikbaar via: https://www.cdc.gov Geraadpleegd op 4-11-2024.
- CDC. Measles symptoms and complications 2024. Beschikbaar via: https://www.cdc.gov
- Charlier C, Dina J, Freymuth F, Vabret A, Lortholary O, Antona D, et al. Prolonged Maternal Shedding and Maternal-fetal Transmission of Measles Virus. Clinical Infectious Diseases. 2021;72(9):1631-4. https://doi.org/10.1093/cid/ciaa915
- Chen SY, Anderson S, Kutty PK, Lugo F, McDonald M, Rota PA, et al. Health Care–Associated Measles Outbreak in the United States After an Importation: Challenges and Economic Impact. The Journal of Infectious Diseases. 2011;203(11):1517-25. https://doi.org/10.1093/infdis/jir115
- Croteau M, Trapé M. Globally emerging occupational infections. Couturier's occupational and environmental infectious diseases. Beverly Farms, MA: OEM Press; 2009. p. 692.
- Di Pietrantonj C, Rivetti A, Marchione P, Debalini MG, Demicheli V. Vaccines for measles, mumps, rubella, and varicella in children. Cochrane Database Syst Rev. 2021 Nov 22;11(11):CD004407. doi: 10.1002/14651858.CD004407.pub5. PMID: 34806766; PMCID: PMC8607336.
- (European Centre for Disease Prevention and Control). Who is at risk for measles in the (Europese Unie)/EEA? Stockholm 2019. Beschikbaar via: https://www.ecdc.europa.eu
- ECDC. Factsheet about measles 2023. Beschikbaar via: https://www.ecdc.europa.eu
- ECDC. Communicable desease threats report. Week 41, 5-11 October 2024. 2024. Beschikbaar via: https://www.ecdc.europa.eu
- ECDC. Measles. Annual Epidemiological Report for 2023. 2024. Beschikbaar via: https://www.ecdc.europa.eu
- ECDC. Measles on the rise again in Europe: time to check your vaccination status. 2025. Beschikbaar via: https://www.ecdc.europa.eu
- eClinicalMedicine. Concerning global rise in measles cases. eClinicalMedicine. 2024;68. https://doi.org/10.1016/j.eclinm.2024.102502
- EG. Richtlijn 2000/54/EG van het Europees Parlement en de Raad van 18 september 2000 betreffende de bescherming van de werknemers tegen de risico's van blootstelling aan biologische agentia op het werk (zevende bijzondere richtlijn in de zin van artikel 16, lid 1, van Richtlijn 83/391/EEG). Brussel; 2020. Beschikbaar via: https://eur-lex.europa.eu
- EMA. M-M-RVaxPro: EPAR – Product Information. European Medicines Agency 2025. Beschikbaar via: https://www.ema.europa.eu/nl/documents/product-information/m-m-rvaxpro-epar-product-information_nl.pdf
- Fappani C, Gori M, Canuti M, Terraneo M, Colzani D, Tanzi E, et al. Breakthrough Infections: A Challenge towards Measles Elimination? Microorganisms. 2022;10(8). https://doi.org/10.3390/microorganisms10081567
- Follin P, Dotevall L, Jertborn M, Khalid Y, Liljeqvist JA, Muntz S, et al. Effective control measures limited measles outbreak after extensive nosocomial exposures in January-February 2008 in Gothenburg, Sweden. Euro Surveill. 2008;13(30).
- Fu J, Jiang C, Wang J, Cai R, Cheng W, Shi L, et al. A hospital-associated measles outbreak in health workers in Beijing: Implications for measles elimination in China, 2018. Int J Infect Dis. 2019;78:85-92. https://doi.org/10.1016/j.ijid.2018.10.023
- Gadroen K, Dodd CN, Masclee GMC, de Ridder MAJ, Weibel D, Mina MJ, et al. Impact and longevity of measles-associated immune suppression: a matched cohort study using data from the THIN general practice database in the UK. BMJ Open. 2018;8(11):e021465. https://doi.org/10.1136/bmjopen-2017-021465
- Gastanaduy P, Haber P, Rota PA, Patel M. H13: Measles. Pink Book2024.
- Gastañaduy PA, Banerjee E, DeBolt C, Bravo-Alcántara P, Samad SA, Pastor D, et al. Public health responses during measles outbreaks in elimination settings: Strategies and challenges. Hum Vaccin Immunother. 2018;14(9):2222-38. https://doi.org/10.1080/21645515.2018.1474310
- Gershon A. Measles. In: Bennett JE DR, Blaser MJ, editors, editor. Mandell, Douglas, and Bennett's principles and practice of infectious diseases. Philadelphia: Elsevier Saunders; 2021. p. 2110-6.
- Gohil SK, Okubo S, Klish S, Dickey L, Huang SS, Zahn M. Healthcare Workers and Post-Elimination Era Measles: Lessons on Acquisition and Exposure Prevention. Clinical Infectious Diseases. 2015;62(2):166-72. https://doi.org/10.1093/cid/civ802
- Griffin DE. Measles virus persistence and its consequences. Curr Opin Virol. 2020;41:46-51. https://doi.org/10.1016/j.coviro.2020.03.003
- Guerra FM, Bolotin S, Lim G, Heffernan J, Deeks SL, Li Y, et al. The basic reproduction number (R(0)) of measles: a systematic review. Lancet Infect Dis. 2017;17(12):e420-e8. https://doi.org/10.1016/s1473-3099(17)30307-9
- Hahne S, te Wierik MJ, Mollema L, van Velzen E, de Coster E, Swaan C, et al. Measles outbreak, the Netherlands, 2008. Emerg Infect Dis. 2010;16(3):567-9. https://doi.org/10.3201/eid1603.090114
- Hahné SJ, Nic Lochlainn LM, van Burgel ND, Kerkhof J, Sane J, Yap KB, et al. Measles Outbreak Among Previously Immunized Healthcare Workers, the Netherlands, 2014. J Infect Dis. 2016;214(12):1980-6. https://doi.org/10.1093/infdis/jiw480
- Hübschen JM, Gouandjika-Vasilache I, Dina J. Measles. Lancet. 2022;399(10325):678-90. https://doi.org/10.1016/s0140-6736(21)02004-3
- Jackson LA, Stewart LK, Solomon SL, Boase J, Alexander ER, Heath JL, et al. Risk of infection with hepatitis A, B or C, cytomegalovirus, varicella or measles among child care providers. Pediatr Infect Dis J. 1996;15(7):584-9. https://doi.org/10.1097/00006454-199607000-00005
- Jain P, Rathee M. Koplik Spots. StatPearls. Treasure Island (FL): StatPearls Publishing Copyright © 2024, StatPearls Publishing LLC.; 2024.
- Jost M, Luzi D, Metzler S, Miran B, Mutsch M. Measles associated with international travel in the region of the Americas, Australia and Europe, 2001-2013: a systematic review. Travel Med Infect Dis. 2015;13(1):10-8. https://doi.org/10.1016/j.tmaid.2014.10.022
- Kessler ER. Vaccine preventable diseases in occupational medicine. Couturier's occupational and environmental infectious diseases. Beverly Farms, MA: OEM Press; 2009. p. 135-48.
- Khalil A, Samara A, Campbell C, Ladhani SN. Pregnant women and measles: we need to be vigilant during outbreaks. EClinicalMedicine. 2024;72:102594. https://doi.org/10.1016/j.eclinm.2024.102594
- Klinkenberg D, Nishiura H. The correlation between infectivity and incubation period of measles, estimated from households with two cases. J Theor Biol. 2011;284(1):52-60. https://doi.org/10.1016/j.jtbi.2011.06.015
- Kobayashi A, Shimada T, Tanaka-Taya K, Kanai M, Okuno H, Kinoshita M, et al. Epidemiology of a workplace measles outbreak dominated by modified measles cases at Kansai international airport, Japan, during august-september 2016. Vaccine. 2020;38(32):4996-5001. https://doi.org/10.1016/j.vaccine.2020.05.067
- Laksono BM, de Vries RD, Duprex WP, de Swart RL. Measles pathogenesis, immune suppression and animal models. Curr Opin Virol. 2020;41:31-7. https://doi.org/10.1016/j.coviro.2020.03.002
- Laksono BM, de Vries RD, Verburgh RJ, Visser EG, de Jong A, Fraaij PLA, et al. Studies into the mechanism of measles-associated immune suppression during a measles outbreak in the Netherlands. Nat Commun. 2018;9(1):4944. https://doi.org/10.1038/s41467-018-07515-0
- Lebon P, Gelot A, Zhang SY, Casanova JL, Hauw JJ. Measles Sclerosing Subacute PanEncephalitis (SSPE), an intriguing and ever-present disease: Data, assumptions and new perspectives. Rev Neurol (Paris). 2021;177(9):1059-68. https://doi.org/10.1016/j.neurol.2021.02.387
- Lessler J, Reich NG, Brookmeyer R, Perl TM, Nelson KE, Cummings DA. Incubation periods of acute respiratory viral infections: a systematic review. Lancet Infect Dis. 2009;9(5):291-300. https://doi.org/10.1016/s1473-3099(09)70069-6
- Leuridan E, Van Damme P. Passive transmission and persistence of naturally acquired or vaccine-induced maternal antibodies against measles in newborns. Vaccine. 2007;25(34):6296-304. https://doi.org/10.1016/j.vaccine.2007.06.020
- Maltezou HC, Wicker S. Measles in health-care settings. Am J Infect Control. 2013;41(7):661-3. https://doi.org/10.1016/j.ajic.2012.09.017
- Miller C, Farrington CP, Harbert K. The epidemiology of subacute sclerosing panencephalitis in England and Wales 1970-1989. Int J Epidemiol. 1992;21(5):998-1006. https://doi.org/10.1093/ije/21.5.998
- Minta AA, Ferrari M, Antoni S, Lambert B, Sayi TS, Hsu CH, et al. Progress Toward Measles Elimination - Worldwide, 2000-2023. (Morbidity and Mortality Weekly Report) Morb Mortal Wkly Rep. 2024;73(45):1036-42. https://doi.org/10.15585/mmwr.mm7345a4
- Minta AA, Ferrari M, Antoni S, Portnoy A, Sbarra A, Lambert B, et al. Progress Toward Measles Elimination - Worldwide, 2000-2022. MMWR Morb Mortal Wkly Rep. 2023;72(46):1262-8. https://doi.org/10.15585/mmwr.mm7246a3
- Moorer N. Vraag uit de praktijk: Bijwerkingen of mazelen? Infectieziekten Bulletin 2011;22(6):203. Beschikbaar via: https://www.rivm.nl/infectieziekten-bulletin/jaargang-22-2011-juli/bijwerking-of-mazelen
- Moss WJ, Griffin DE. Measles. The Lancet. 2012;379(9811):153-64. https://doi.org/10.1016/S0140-6736(10)62352-5
- Moss WJ, Griffin DE. What's going on with measles? J Virol. 2024;98(8):e0075824. https://doi.org/10.1128/jvi.00758-24
- Moussallem TM, Guedes F, Fernandes ER, Pagliari C, Lancellotti CL, de Andrade HF, Jr., et al. Lung involvement in childhood measles: severe immune dysfunction revealed by quantitative immunohistochemistry. Hum Pathol. 2007;38(8):1239-47. https://doi.org/10.1016/j.humpath.2007.01.015
- Muscat M. Who Gets Measles in Europe? The Journal of Infectious Diseases. 2011;204(suppl_1):S353-S65. https://doi.org/10.1093/infdis/jir067
- Opstelten W, Ruijs WLM, Warris A, van Binnendijk RS, Wolfs TFW, Hahne SJM. Er heerst weer mazelen. Ned Tijdschr Geneeskd. 2013;157:A6710.
- Orenstein WA. Plotkin's vaccines. In: Elsevier, editor.2023.
- Overheid. Artikel 4.91 Arbeidsomstandighedenbesluit Den Haag; 2024. Beschikbaar via: https://wetten.overheid.nl
- Portnoy A, Jit M, Ferrari M, Hanson M, Brenzel L, Verguet S. Estimates of case-fatality ratios of measles in low-income and middle-income countries: a systematic review and modelling analysis. Lancet Glob Health. 2019;7(4):e472-e81. https://doi.org/10.1016/s2214-109x(18)30537-0
- Rasmussen SA, Jamieson DJ. What Obstetric Health Care Providers Need to Know About Measles and Pregnancy. Obstet Gynecol. 2015;126(1):163-70. https://doi.org/10.1097/aog.0000000000000903
- Sakuta H, Sawada S, Kuroki Y. Severity of measles among patients with incidental postexposure vaccination. Jpn J Infect Dis. 2008;61(4):304-6.
- Shperling RB, Yogev Y. Adverse outcomes of measles infection during pregnancy and in the perinatal period. J Matern Fetal Neonatal Med. 2022;35(8):1586-91. https://doi.org/10.1080/14767058.2020.1759536
- SRI. Persoonlijke beschermingsmiddelen 2023.
- SRI. Isolatie. (Geraadpleegd 17-03-2024)
- Steingart KR, Thomas AR, Dykewicz CA, Redd SC. Transmission of measles virus in healthcare settings during a communitywide outbreak. Infect Control Hosp Epidemiol. 1999;20(2):115-9. https://doi.org/10.1086/501595
- Strebel PM, M.J. P, P.A. G, Goodson JL. Measles vaccines. Philadelphia, PA: Elsevier; 2018.
- Strebel PM, Orenstein WA. Measles. N Engl J Med. 2019;381(4):349-57. https://doi.org/10.1056/NEJMcp1905181
- Sundell N, Dotevall L, Sansone M, Andersson M, Lindh M, Wahlberg T, et al. Measles outbreak in Gothenburg urban area, Sweden, 2017 to 2018: low viral load in breakthrough infections. Euro Surveill. 2019;24(17). https://doi.org/10.2807/1560-7917.Es.2019.24.17.1900114
- (Ministerie van Sociale Zaken en Werkgelegenheid). Maatregelen bij het werken met biologische agentia (preventie); cited 2025 1-3-2025]. Beschikbaar via: https://www.arboportaal.nl
- Tipples GA, Hamkar R, Mohktari-Azad T, Gray M, Parkyn G, Head C, et al. Assessment of immunoglobulin M enzyme immunoassays for diagnosis of measles. J Clin Microbiol. 2003;41(10):4790-2. https://doi.org/10.1128/jcm.41.10.4790-4792.2003
- Tranter I, Smoll N, Lau CL, Williams DL, Neucom D, Barnekow D, et al. Onward Virus Transmission after Measles Secondary Vaccination Failure. Emerg Infect Dis. 2024;30(9):1747-54. https://doi.org/10.3201/eid3009.240150
- UKHSA. Green book of immunisation. Chapter 21: Measles 2019.
- UKHSA. National measles guidelines. 2024.
- van Binnendijk RS, van den Hof S, van den Kerkhof H, Kohl RH, Woonink F, Berbers GA, et al. Evaluation of serological and virological tests in the diagnosis of clinical and subclinical measles virus infections during an outbreak of measles in The Netherlands. J Infect Dis. 2003;188(6):898-903. https://doi.org/10.1086/377103
- van den Hof S, Conyn-van Spaendonck MA, van Steenbergen JE. Measles epidemic in the Netherlands, 1999-2000. J Infect Dis. 2002;186(10):1483-6. https://doi.org/10.1086/344894
- Waaijenborg S, Hahné SJ, Mollema L, Smits GP, Berbers GA, van der Klis FR, et al. Waning of maternal antibodies against measles, mumps, rubella, and varicella in communities with contrasting vaccination coverage. J Infect Dis. 2013;208(1):10-6. https://doi.org/10.1093/infdis/jit143
- Wetsteyn JC, de Rond WM, Schreuder (Medisch Centrum), de Boer HE, van Binnendijk RS, Wolthers KC. [An outbreak of measles at an emergency room]. Ned Tijdschr Geneeskd. 2008;152(37):2032-6. (Een uitbraak van mazelen op de Spoedeisende Hulp.)
- WHO. Manual for the laboratory diagnosis of measles and rubella virus infection. Geneva, Switzerland; 2007. Beschikbaar via: https://iris.who.int
- WHO. Global childhood immunization levels stalled in 2023, leaving many without life-saving protection 2024. Beschikbaar via: https://www.who.int Geraadpleegd op 6-1-2025.
- WHO. Measles 2024. Beschikbaar via: https://www.who.int Geraadpleegd op 4-11-2024.
- World Health Organization. Chapter 4. Antibody detection methods for laboratory confirmation of measles, rubella, and (congenitalerubellasyndroom). In: Manual for the Laboratory-based Surveillance of Measles, Rubella, and Congenital Rubella Syndrome. WHO 2018. Beschikbaar via: https://www.technet-21.org/en/manual-introduction.
- Woudenberg T, van Binnendijk RS, Sanders EA, Wallinga J, de Melker HE, Ruijs WL, et al. Large measles epidemic in the Netherlands, May 2013 to March 2014: changing epidemiology. Euro Surveill. 2017;22(3). https://doi.org/10.2807/1560-7917.Es.2017.22.3.30443
- Woudenberg T, Woonink F, Kerkhof J, Cox K, Ruijs WLM, van Binnendijk R, et al. The tip of the iceberg: incompleteness of measles reporting during a large outbreak in The Netherlands in 2013-2014. Epidemiol Infect. 2018;147:e23. https://doi.org/10.1017/s0950268818002698
- Young MK, Nimmo (Gezondheidsraad), Cripps AW, Jones MA. Post-exposure passive immunisation for preventing measles. Cochrane Database Syst Rev. 2014;2014(4):Cd010056. https://doi.org/10.1002/14651858.CD010056.pub2