Samenvatting
Verwekker: Humaan herpesvirus (HHV)
Incubatieperiode: 2-12 dagen (meestal 4 dagen)
Transmissieroute: Binnendringing via slijmvliezen van orofarynx, genitaliën of conjunctiva
Infectieuze periode: Tijdens primaire (herpessimplexvirus)-1 en HSV-2-infecties en reactivaties meerdere malen per jaar: levenslang
Maatregelen: Partnerwaarschuwing bij herpes genitalis
Symptomen: Herpes labialis: vaak asymptomatisch. Pijnlijke vesiculaire laesies van de orale mucosa, koorts, malaise. Herpes genitalis: vaak asymptomatisch. Koorts, malaise, spierpijn, urethritisklachten
blok
Deze richtlijn is ontwikkeld voor zorgprofessionals werkzaam binnen de infectieziektebestrijding. De primaire doelgroepen zijn GGD- en LCI-professionals. Deze richtlijn bevat adviezen, taken en verantwoordelijkheden en vormt een basis voor het nemen van geïnformeerde beslissingen en het maken van beleid in de praktijk. Voor meer informatie zie Ontwikkeling LCI-richtlijnen.
Vastgesteld (Landelijk Overleg Infectieziektebestrijding-Seksuele Gezondheid): 25 juni 2024.
Wijzigingen
- 18 maart 2025: Nieuwe indeling in achtergrondinformatie en een richtlijndeel (met de hoofdstukken Diagnostiek, Preventie en Maatregelen en waar van toepassing arbeidsrelevante aanvullingen en veterinaire informatie). Historie is ondergebracht in andere hoofdstukken en ten dele vervallen.
- 29 juli 2024: Herziene richtlijn gepubliceerd (op 25 juni 2024 vastgesteld door het LOI-SG). Nieuw en anders ten opzichte van de oude richtlijn: De richtlijn is aangepast naar aanleiding van de in 2024 herziene Multidisciplinaire richtlijn Seksueel overdraagbare aandoeningen (MDR Soa's). De epidemiologie is herzien.
Achtergronden
Herpessimplexvirusinfecties worden in klassieke gevallen gekenmerkt door typisch in groepjes gelegen blaasjes die soms overgaan in pijnlijke erosies met korstvorming. Het virus blijft latent aanwezig en kan vooral lokaal frequent recidieven veroorzaken.
Genitale herpes is de meest voorkomende ulceratieve soa in de westerse wereld (Mindel 1998).
Verwekker
Herpessimplexvirussen zijn dubbelstrengs DNA-virussen behorend tot de familie van de herpesvirussen. Er zijn meer dan honderd herpesvirussen, waarvan er minimaal negen bij de mens kunnen voorkomen. De officiële benaming van herpesvirussen die infecties veroorzaken bij de mens is humaan herpesvirus (HHV), waarbij elk type een nummer heeft gekregen.
Bekende ziektebeelden zijn:
- herpes labialis (koortslip) door herpessimplexvirus type 1 (HSV-1, officieel (humaan herpesvirus)-1);
- herpes genitalis door zowel (herpessimplexvirus)-1 als HSV-2 (HHV-2);
- waterpokken en gordelroos door het varicellazostervirus (VZV, HHV-3);
- mononucleosis infectiosa door het epstein-barrvirus (EBV, HHV-4);
- cytomegalovirus (CMV, HHV-5);
- zesde ziekte (HHV-6);
- kaposisarcoom (HHV-8).
De herpessimplexvirussen type 1 en type 2 zijn nauw aan elkaar verwant en vertonen dezelfde genoomstructuur (Pellet 2013).
Epidemiologie
Verspreiding in de wereld
HSV-infecties komen wereldwijd voor. De HSV-1-seroprevalentie is wereldwijd 67% onder personen jonger dan 50 jaar (WHO 2023). Het aantal personen met een (doorgemaakte) infectie stijgt met de leeftijd. Gemiddeld genomen zijn meer vrouwen dan mannen geïnfecteerd (James 2020).
Herpes genitalis komt overal in de wereld voor en is de belangrijkste ulceratieve soa in de westerse wereld met een geschatte prevalentie van 417 miljoen HSV-2-geïnfecteerden wereldwijd (WHO 2016). In Groot-Brittannië is de incidentie (primo-infectie) in 5 jaar tijd met 15% toegenomen (16.479 gerapporteerde gevallen in 1995; 19.180 gerapporteerde gevallen in 2004). In de Verenigde Staten hebben naar schatting 40-60 miljoen mensen de infectie, met een incidentie van 12 miljoen infecties en 600.000-800.000 klinische casussen per jaar. De prevalentie van genitale herpes in ontwikkelingslanden varieert van 2% tot 74% (Sen 2007).
Voorkomen in Nederland
Herpes labialis komt als primo-infectie vooral bij jonge kinderen voor. Daarnaast komen primo-infecties ook steeds vaker bij adolescenten en jongvolwassenen voor. In Nederland wordt de incidentie van herpes labialis geschat op 1,6 per 1000 personen per jaar gemeten in een huisartspraktijkpopulatie van ongeveer 376.000 personen (Linden 2004).
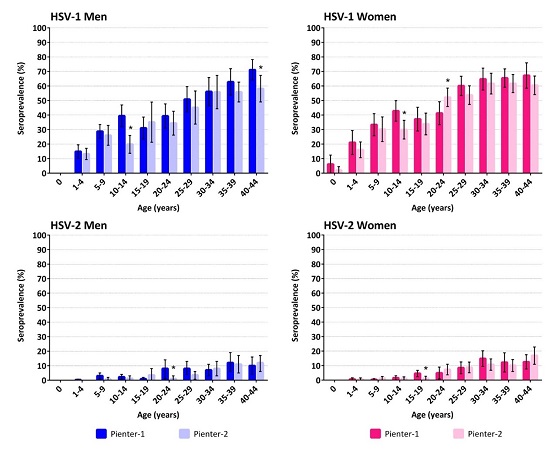
Onderzoek in Nederland laat in Nijmegen een seroprevalentie van 61% HSV-1-antistoffen zien onder zwangeren, tegenover 73-75% in het westen van Nederland (Amsterdam en Rotterdam) (Gaytant 2002). Seroprevalentie voor HSV-1 en HSV-2 in Nederland uitgevoerd op Pienter-1- (1995-1996) en Pienter-2 (2006-2007) -sera was respectievelijk 47,7 en 6,8% (Pienter-1) en 42,7% en 6% (Pienter-2) (zie afbeelding). Een significant lagere seroprevalentie voor HSV-1 werd waargenomen in Pienter-2 vergeleken met Pienter-1 in de leeftijd van 10-14 jaar. Dit maakt dat jongvolwassenen een grotere kans hebben op een genitale HSV-1-infectie (Woestenberg 2016). In de periode 2012-2015 was de incidentie van neonatale herpes in Nederland 4,8-6,5 per 100.000 geboorten (Van Oeffelen 2018).
Seroprevalentie van HSV-1 en HSV-2 in Nederland volgens Pienter-1 (1995-1996) en Pienter-2 (2006-2007). Bron: Woestenberg 2016.
In 2021 was het aantal diagnoses van genitale herpes bij de Centra voor Seksuele Gezondheid (CSG’s) 540 (van Wees 2022). (Centrum Seksuele Gezondheid)’s verrichten geen routinematig onderzoek naar genitale herpes. Genitale herpes wordt voornamelijk gediagnosticeerd bij de huisarts. In 2020 waren er naar schatting 29.300 diagnoses van genitale herpes (28.800 in 2019). In 2020 was het aantal meldingen van genitale herpesdiagnoses bij huisartsen 1,7 per 1.000 individuen. Dit was 2,5 per 1.000 voor vrouwen en 0,9 per 1.000 voor mannen. Het meldingspercentage voor vrouwen en mannen is hoger in de populatie van 25 jaar en ouder dan voor de groep onder de 25 jaar. Bij mannen was dit verschil het meest significant. Het aandeel genitale HSV-1 is in de huisartsenpraktijk aanzienlijk hoger bij met name jongere leeftijd en bij vrouwen (gegevens Brabant Zuid-Oost 2002-2010). Oorzaken voor meer genitale HSV-1 zouden kunnen zijn frequenter orogenitaal contact en minder “beschermende” immuniteit door pas op latere leeftijd in contact komen met herpes labialis. De beschikbare prevalentie- en incidentiegegevens zijn echter niet betrouwbaar omdat diagnostiek niet routinematig wordt uitgevoerd. Vanwege een hoog percentage asymptomatische infecties is onderrapportage zeer waarschijnlijk.
Zie voor actuele informatie over het voorkomen van herpes genitalis in Nederland: Herpes genitalis (rivm.nl).
Pathogenese
De pathogenese van genitale herpes, die door zowel HSV-1 als HSV-2 wordt veroorzaakt, verschilt niet van die van herpes labialis, die vooral wordt veroorzaakt door HSV-1. HSV dringt de slijmvliezen binnen van de orofarynx, genitaliën of conjunctiva en verspreidt zich van hieruit langs de perifere zenuwen naar de sensibele of autonome ganglia waar het virus latent verblijft. Tijdens een primaire infectie of primo-infectie met HSV wordt humorale en cellulaire afweer opgebouwd. Dit voorkomt reactivatie echter niet, doordat het virus zich verspreidt via zenuwcellen die slecht toegankelijk zijn voor het immuunsysteem. Van hieruit vindt periodiek en kortdurend (sub)klinische of (a)symptomatische reactivatie plaats met virusuitscheiding langs de zenuw naar de huid of slijmvliezen in het verzorgingsgebied (Corey 2007, Mark 2008). Reactivatie van latent virus kan door verschillende stimuli worden veroorzaakt, zoals uv-licht, stress, menstruatie, koorts en immuunsuppressie. HSV-infecties kunnen worden onderverdeeld in eerste-episode-infecties (te onderscheiden in primaire en niet-primaire infecties) en recidieven (reactivaties) (Drake 2000). Men spreekt van een primaire of primo-infectie wanneer er sprake is van een HSV-1- of HSV-2-infectie bij een HSV (zowel -1 als -2)-seronegatieve persoon. Is er in het verleden wel een labiale HSV-1- of HSV-2-infectie geweest, dan spreekt men van een eerste episode herpes genitalis.
Een eerste HSV-2-infectie bij iemand met reeds aanwezige HSV-1-specifieke antistoffen wordt dus een niet-primaire HSV, eerste HSV-2-episode genoemd. Ook hier betreft het een contactinfectie, in dit geval met de huid of slijmvliezen van de anogenitale regio. Op de plaats van de primaire infectie ontstaat een blaasje, dat na een ulceratief stadium uiteindelijk indroogt met korstvorming. Primaire infecties verlopen in ongeveer de helft van de gevallen symptoomloos. Een herinfectie ten slotte is een infectie met eenzelfde HSV-type waartegen reeds antilichamen bestonden. Een herinfectie is dus niet hetzelfde als een reactivatie.
Incubatieperiode
2 tot 12 dagen (meestal 4 dagen).
Ziekteverschijnselen
De herpessimplexvirussen type 1 en type 2 vertonen de volgende ziekteverschijnselen.
Herpes labialis (koortslip)
Een eerste episode herpes labialis vindt meestal plaats op de kleuterleeftijd en kan zich uiten als pijnlijke vesiculaire laesies van de orale mucosa (gingivostomatitis), eventueel gepaard met systemische symptomen (koorts, malaise). De laesies genezen over het algemeen binnen 1-2 weken. In het merendeel van de gevallen verloopt een eerste episode herpes labialis echter asymptomatisch.
Een recidief herpes labialis verloopt milder dan een eerste episode herpes labialis en blijft meestal beperkt tot de lippen (koortslip) zonder de mucocutane overgang te passeren, tenzij er sprake is van een gestoorde afweer. In het algemeen zijn recidieven te verwachten op plaatsen nabij de plek waar de eerste-episode-infectie zich heeft geuit (bijvoorbeeld herpes keratitis of herpetische fijt). Systemische symptomen komen bij een recidief van herpes labialis over het algemeen niet voor.
De blaasjes doorlopen verschillende stadia. Een blaasje kan spontaan opengaan, of door krabben en zo het aspect van een ulcus aannemen. Als de blaasinhoud daarna opdroogt treedt het crusteuze stadium in, waarin weinig tot geen infectieus virus meer wordt uitgescheiden. Daarna geneest de laesie doorgaans restloos. De totale duur kan variëren van 3 tot 7 dagen.
Bij het opnemen van de anamnese zal men zeker vragen of de cliënt deze (vroege) symptomen herkent van een eerdere gelegenheid.
Herpes genitalis
De aard en ernst van de ziekteverschijnselen worden bepaald door gastheerspecifieke factoren zoals lokalisatie, vroegere niet-genitale HSV-infectie, geslacht, immuunstatus van de persoon en of er sprake is van een primo-infectie (meestal heftiger verloop) of een recidief. Er is geen verschil in ziekteverschijnselen tussen herpes genitalis door HSV-1 en HSV-2 (Holmes 2008).
Volgens de literatuur is slechts 37% van de nieuwe (primaire infectie) HSV-2-infecties symptomatisch; voor HSV-1 ligt dit rond 67%. De rest van de infecties, en dus de meerderheid van de genitale herpesinfecties, verloopt asymptomatisch of wordt niet als zodanig herkend. Bij mannen zijn de infecties vaker asymptomatisch dan bij vrouwen (Drake 2000, Langenberg 1999). Bij een symptomatische primo-infectie heeft 40% van de mannen en 70% van de vrouwen een prodromale fase, bestaande uit koorts, malaise en spierpijn (Holmes 2008). Hierna volgen bij vrouwen klachten als pijn, jeuk, dysurie, vaginale afscheiding en regionale lymfadenopathie. Bij mannen komen ook urethritisklachten voor en kan de mictie zodanig pijnlijk verlopen dat urineretentie optreedt. Zes tot 7 dagen na de eerste symptomen volgen de huid- en slijmvliesafwijkingen met soms ontwikkeling van de karakteristieke, met helder vocht gevulde blaasjes. De laesies duren bij een primo-infectie 7-28 dagen en genezen zonder littekens. Men dient rekening te houden met atypische laesies die zich presenteren als fissuren, furunkels, plaatselijke erytheem, lineaire ulceraties of excoriaties. Verder kan een herpetische proctitis ontstaan met anorectale pijn, obstipatie en ulcererende herpetiforme laesies.
Bij mannen zijn de laesies voornamelijk gelegen op de schacht van de penis (met uitzondering van de anorectale herpes), bij vrouwen zijn de laesies verspreid over de hele vulva en het perineum (Wald 2001). Minder bekend is dat bij vrouwen ook de cervix uteri vaak betrokken is bij een primo-infectie (Soa bestrijding 1998). Dit kan zeer pijnlijk zijn, waardoor een onderzoek van de cervix in speculo niet goed mogelijk is en de diagnose gemist wordt. Primaire infecties bij zwangeren kunnen asymptomatisch verlopen; twee derde van de zwangeren, seropositief voor HSV-2, bleken geen ulceraties gehad te hebben (Westhoff 2011).
HSV is in een veel uitgebreider gebied aantoonbaar dan alleen het gebied van de zichtbare laesies (Tata 2010). De frequentie van de recidieven wisselt sterk, afhankelijk van het virustype en de lokalisatie. Het gemiddelde aantal recidieven is na een eerste episode zeer variabel met een mediaan van 4 per jaar voor HSV-2 en 1 per jaar voor HSV-1 (Laferty 1987, Benedetti 1994, Engelberg 2003). Bij de meeste patiënten is er een afname in de tijd en in ernst, maar dit patroon is zeer variabel (Benedetti 1999). Bij HSV-2 neemt het aantal recidieven af na het eerste jaar, maar blijft daarna vrij constant gedurende jaren (Phipps 2011).
Complicaties van een genitale herpesinfectie treden vrijwel alleen op bij een primaire infectie met HSV-1 of HSV-2. Een voorbeeld is aseptische meningitis (nekstijfheid, hoofdpijn en fotofobie), die vaker bij HSV-2 dan bij HSV-1 voorkomt. Ook kan autonome dysfunctie of myelitis transversa optreden. Symptomen van de autonome dysfunctie kunnen zijn: hyperesthesie of anesthesie in de lumbale of sacrale regio en urineretentie (het syndroom van Elsberg) of obstipatie.
Neonatale herpes
Neonatale HSV-1- en HSV-2-infectie kunnen milde tot zeer ernstige symptomen geven. Er zijn drie klinische verschijningsvormen van neonatale herpes te onderscheiden (James 2015, Forsgren 2009).
- De infectie blijft beperkt tot de huid en de slijmvliezen van ogen en/of mond (in de Engelstalige literatuur skin eye mouth (SEM) disease genoemd). De gemiddelde incubatieperiode is dan 7-12 dagen. Een lokale infectie heeft een veel betere prognose, maar kan gepaard gaan met oogschade, waaronder herpes keratitis. Neurologische schade, waaronder retinanecrose, kan later aan het licht komen (5-10%).
- Een infectie van het centraal zenuwstelsel met of zonder betrokkenheid van de huid/slijmvliezen. De gemiddelde incubatieperiode is 2-6 weken. Bij alleen symptomen van een infectie van het centraal zenuwstelsel is de mortaliteit zonder behandeling >50%; met aciclovir zakt dit naar 4% (Scott 2015). De kans op neurocognitieve schade is groot; slechts een derde van de kinderen met centraal zenuwstelsel betrokkenheid heeft een normale ontwikkeling (Scott 2015). HSV-2-infectie heeft een slechtere prognose dan HSV-1-infectie.
- Een gegeneraliseerde infectie waarbij zowel huid, slijmvliezen, lever, bijnieren, longen als centraal zenuwstelsel aangetast zijn. De incubatieperiode is 4-11 dagen. De symptomen bij deze vorm zijn meestal algemene verschijnselen als koorts, sufheid, slecht drinken, braken en ademhalingsproblemen. In een later stadium kunnen verschijnselen optreden van acidose, shock, anemie, pneumonie, convulsies, hepatomegalie, encefalitis en meningitis. Bij een gegeneraliseerde infectie is de sterfte zonder antivirale therapie hoog (>80%) met fulminant leverfalen of multiorgaanfalen en een grote kans op restverschijnselen. Met aciclovir zakt de kans op overlijden naar 29%, maar ook hier is de kans op neurocognitieve schade groot (Scott 2015).
Slechts in ongeveer 50% van de gevallen van neonatale herpes zijn blaasjes aanwezig, zodat de diagnose vaak moeilijk te stellen is. Herkennen van de symptomen en snelle start van behandeling zijn van belang voor een goede uitkomst (Forsgren 2009).
Bij oudere kinderen en adolescenten verloopt een infectie met HSV veelal asymptomatisch. Bij genitale herpes verloopt de infectie vergelijkbaar als bij volwassenen.
Natuurlijke immuniteit
Na een primaire infectie ontstaan antistoffen die wel beschermen tegen een herinfectie, maar recidieven niet kunnen voorkomen. De (immunoglobuline G)-antistoffen en specifieke geheugen-T-cellen worden transplacentair overgedragen (verticale transmissie). Het is echter onbekend welke mate van bescherming deze bieden voor het kind. Bovendien is het zo dat HSV-1 en -2 kruisreagerende antistoffen induceren, die gedeeltelijke kruisbescherming bieden en die de ernst van een eerste-ziekte-episode verminderen, maar geen invloed hebben op het aantal recidieven.
Reservoir
De mens; er is geen tussengastheer.
Transmissie
Transmissieroute
Direct contact tussen (vers lichaamsvocht van) een persoon die virus uitscheidt en de mucosa van mond-keelholte, oog, genitaliën en anus of huid of via contact met gecontamineerde voorwerpen. Transmissie via de intacte huid verloopt niet efficiënt en vindt dan ook meestal plaats via (micro‑)laesies.
Genitale herpes ontstaat via seksueel contact: genitogenitaal, anogenitaal of orogenitaal. Dit laatste verklaart hoe HSV-1 genitale herpes kan veroorzaken en HSV-2 labiale herpes.
Verticale transmissie kan op de volgende manieren geschieden: prenataal (5% is transplacentair), durante partu (75-95% is ascenderend bij langdurig gebroken vliezen of tijdens de partus), of postnataal (Kimberlin 2005). Ook kan neonatale herpes ontstaan via besmetting door iemand anders met een labiale herpesinfectie, bijvoorbeeld door knuffelen of zoenen van het kind (‘kiss of death’) (zie Verhoogde kans op ernstig beloop).
Infectie van de handen van medisch of verpleegkundig personeel via contact met een HSV-drager, kan leiden tot een fijt (bindweefselontsteking aan de binnenkant van een vingertop), ook wel ‘herpetic whitlow’ genoemd.
Aerogene transmissie is niet gebruikelijk.
Infectieuze periode
De infectieuze periode is niet goed vast te stellen. Bij aanwezigheid van laesies is tot tien dagen na ontstaan nog HSV aantoonbaar. Ook zonder aanwezigheid van laesies kunnen patiënten nog infectieus zijn door asymptomatische uitscheiding.
Tijdens primaire HSV-1- en HSV-2-infecties, zowel symptomatisch als asymptomatisch, treedt er uitscheiding op van soms grote hoeveelheden virus. Hierna kunnen meerdere malen per jaar reactivaties optreden, zowel symptomatisch als asymptomatisch, waarbij opnieuw virus wordt uitgescheiden. Daarom wordt een geïnfecteerde persoon levenslang als potentieel infectieus beschouwd, ook zonder dat er symptomen zijn.
Bij asymptomatische HSV-1- of HSV-2-seropositieven is virusuitscheiding gevonden in 2-8% van alle dagen, dus 7-28 dagen per jaar. Recente gegevens laten zien dat zich kortdurende perioden voordoen van (sub)klinische en asymptomatische reactivaties met ‘viral shedding’, zelfs tot 20% van alle dagen (Corey 2007).
>Het aantal reactivaties is het grootst in het eerste jaar na de primaire infectie en hangt mede af van gastheerfactoren, omgevingsfactoren en van de locatie van de infectie en het type HSV (Wald 2000).
Overdraagbaarheid
Herpesvirussen hebben een envelop en zijn hiermee gevoelig voor omgevingsfactoren, zoals temperatuur en uitdroging. Ze overleven niet lang in de omgeving, en worden vooral overgedragen via direct contact. In een experimentele setting werd overleving van HSV-1 op enkele voorwerpen van ten minste 2 uur gevonden (Suissa 2023).
Tijdens de primaire infectie worden grote hoeveelheden virus uitgescheiden. In een gesloten gemeenschap, zoals een kinderdagverblijf of school, kan primaire gingivostomatitis zeer infectieus zijn en leiden tot kleine uitbraken (Kuzushima 1991, Schmitt 1991).
De overdraagbaarheid van herpes labialis is het grootst als er actieve laesies aanwezig zijn, maar ook zonder laesies is er regelmatig virusuitscheiding (Douglas 1970).
De overdraagbaarheid is het hoogst vlak voor, tijdens en vlak na de symptomatische periode. Bij vaginale coïtus is de transmissiekans hoger van mannen naar vrouwen dan andersom. De transmissiekans is hoger bij frequenter seks zonder condoom of andere preventiemiddelen.
Bij monogame serodiscordante paren waarvan bekend was dat één partner HSV-seropositief was, varieerde de transmissiekans van 12% tot 30% per jaar (Drake 2000, Roest 1999).
Bij symptomatische patiënten is bij 70% HSV-2 aantoonbaar; bij asymptomatische patiënten is dat 13%. Dat betekent dat dus ook bij asymptomatische patiënten virusuitscheiding plaats kan vinden. Asymptomatische uitscheiding neemt sterk af in het eerste jaar na een genitale HSV-1-infectie (Johnston 2022). HSV wordt periodiek in episoden uitgescheiden, HSV-virusdetectie is mogelijk gedurende een periode van maximaal negen dagen bij patiënten met laesies en maximaal vier dagen bij patiënten zonder frequente laesies (Corey 2004, Tronstein 2011). De uitscheiding van HSV-2 wordt gekenmerkt door een snelle toe- en ook weer afname van virale load. Er is daarbij een extreme variatie in de hoogte van virale load en de duur van verschillende episoden. Het netto-effect is zeer frequente perioden van uitscheiding met hoge virale loads (Schiffer 2011). De meerderheid van de infecties blijkt via asymptomatische dragers te gebeuren.
Het herpessimplexvirus wordt snel geïnactiveerd bij kamertemperatuur en in droge omstandigheden. Aerogene transmissie vindt dan ook niet plaats.
De kans op verticale transmissie tijdens de baring is het grootst (ongeveer 50%) tijdens een primaire genitale herpes bij de zwangere. Bij een recidief is de kans op verticale transmissie klein. Borstvoeding is mogelijk indien geen laesies in dermatomen van het borstgebied (thoracaal 2 t/m 6) aanwezig zijn en actieve laesies elders zijn afgeplakt/afgedekt (mondmasker) en goede handhygiëne wordt betracht.
Risicogroepen
Verhoogde kans op infectie
Een primaire herpes labialis komt vooral voor op de kleuterleeftijd, maar wordt ook regelmatig gezien bij adolescenten. Frequent intiem contact geeft een verhoogde kans op transmissie.
Zoals bij alle soa’s is de kans dat iemand wordt geïnfecteerd afhankelijk van het aantal seksuele partners en de aard van seksuele activiteiten. Factoren die de kans op HSV-1-seropositiviteit vergroten zijn: vrouw, hogere leeftijd, migratieachtergrond en lager-gemiddeld educatieniveau. Factoren die de kans vergroten op HSV-2 zijn gelijk aan de factoren bij HSV-1 behalve dat HSV-2 vaker wordt gezien bij hogere educatieniveaus (Woestenberg 2016).
Inmiddels is goed gedocumenteerd in meerdere studies dat het hebben van genitale ulcera zoals bij herpes genitalis de transmissie van hiv bevordert. Genitale ulcera maken iemand ontvankelijker voor een hiv-infectie. Enkele studies laten zien dat personen die leven met hiv met genitale ulcera een verhoogde uitscheiding van hiv laten zien, waarschijnlijk door synergistische mechanismen (Nagot 2007, Gray 2004, Schacker 2002, Celum 2005).
Verhoogde kans op ernstig beloop
Bij immuno-incompetente personen, bij patiënten met constitutioneel eczeem en bij neonaten is er sprake van een verhoogde kans op een ernstig beloop.
Immuno-incompetente personen
Personen met een gestoorde cellulaire immuniteit hebben vaker HSV-reactivaties en een hogere kans op een ernstiger beloop. De meeste studies rapporteren over personen die leven met hiv met <200 CD4-cellen/ul, patiënten met maligniteiten en (hematopoëtische stamcel-)transplantatiepatiënten. Bij hen verlopen lokale (orale en genitale, primo- en recidief) infecties vaak ernstiger. Ook kan een gedissemineerde infectie (betrokkenheid van diverse orgaansystemen waaronder pneumonie, colitis, oesophagitis, meningo-encefalitis en retinanecrose) ontstaan. Deze heeft een hoge mortaliteit (Quinnan 1984, Bagdades 1992, Severson 1999).
Patiënten met constitutioneel eczeem
Bij patiënten met constitutioneel eczeem kan een infectie met HSV leiden tot het ontstaan van eczema herpeticum. Het betreft een zeldzame complicatie van een primaire of secundaire HSV-infectie. Eczema herpeticum begint meestal bij pre-existente eczemateuze laesies, maar kan zich verder verspreiden over niet-aangedane huid en gaat vaak gepaard met koorts, malaise en lymfeklierzwelling. Snelle behandeling met antivirale middelen is noodzakelijk om complicaties zoals meningitis te voorkomen. Bij lokale infectie met milde verschijnselen kan volstaan worden met orale therapie. Bij gevorderde infectie en ernstige klachten of complicaties kan ziekenhuisopname voor intraveneuze therapie noodzakelijk zijn (Aronson 2011, Luca 2012).
Risico’s voor zwangeren en neonaten
Zwangeren
Bij de zwangere vrouw zelf verloopt een HSV-infectie zelden ernstiger dan bij niet-zwangere vrouwen. Wel is het mogelijk dat het aantal recidieven hoger ligt bij zwangeren (Holmes 2008). Factoren die de kans op genitale herpes tijdens de zwangerschap verhogen, zijn niet-westerse etniciteit en een leeftijd <20 jaar (van Oeffelen 2018).
Neonaten
Neonatale herpes omvat prenataal, durante partu en postnataal verworven HSV-infecties (in twee derde van de gevallen veroorzaakt door HSV-1).
Besmetting van het kind durante partu, door direct contact van het kind met vaginaal secreet of ascenderend bij langdurig gebroken vliezen, is de meest gebruikelijke transmissieroute (90% van de gevallen) (Mandell 2005). Het ontbreken van passief via de moeder overgedragen antistoffen is waarschijnlijk een belangrijke risicofactor voor een ernstig beloop van de infectie. Het betreft meestal een vlak voor de partus opgelopen eerste-episode-infectie bij de moeder, waardoor de moeder nog geen beschermende antistoffen door kan geven aan het kind. Een primaire infectie geeft een 10-30 keer grotere kans op transmissie in vergelijking tot een recidiverende infectie van de moeder.
Een prenataal verworven infectie komt zeer zelden voor en betreft casuïstiek van mogelijke transplacentaire besmetting bij ogenschijnlijk intacte vliezen.
Daarnaast kan in zeldzame gevallen ook postnataal verworven HSV via de handen of mond van verzorgers tot ernstige infecties leiden bij neonaten (tot de leeftijd van ongeveer 1 maand).
Neonatale ziekteverschijnselen bij transmissie durante partu beginnen ongeveer vijf dagen na de geboorte.
Diagnostiek
Zie ook Diagnostisch Vademecum Herpesvirus (1, 2).
Microbiologische diagnostiek
Een koortslip is een vrij karakteristiek beeld waarvan de diagnose doorgaans op klinische gronden gesteld wordt. Bij twijfel over het klinisch beeld kan microbiologische diagnostiek worden ingezet.
Directe diagnostiek
De eerste keus voor het aantonen van het virus is de nucleïnezuuramplificatietest (NAAT). Met een swab kan langs de basis van de laesie of het vocht van een blaasje worden gegaan. Deze techniek wordt aanbevolen als diagnosticum bij genitale herpes. (nucleïnezuur amplificatietest (zoals PCR)) is tevens betrouwbaar voor het onderzoek van liquor bij verdenking op HSV-meningitis (Patel 2017). De meeste testen maken een onderscheid tussen type 1- en type 2-herpesvirus. Bij afwezigheid van laesies sluit een negatieve PCR/NAAT een HSV-infectie niet uit, aangezien het virus zich intermitterend verspreidt. Bij een orgaan- of gegeneraliseerde herpesinfectie, zoals hepatitis, is een HSV-virale load bepaling in bloed aangewezen.
De viruskweek, voorheen beschouwd als de gouden standaard, is minder sensitief dan nucleïnezuurtechnieken en meer afhankelijk van transportomstandigheden en stadium van de laesie. Viruskweek wordt daarom in de routine achterwege gelaten (Wald 2003). Bij patiënten met afweerstoornissen of ernstige therapieresistente recidieven kan het van belang zijn om resistentiebepalingen uit te voeren op geïsoleerde stammen die via de conventionele celkweken zijn verkregen of met sequentietechnieken op de geïsoleerde virale nucleïnezuren (Pinninti 2012, Van der Beek 2012).
Materialen die geschikt zijn voor PCR/NAAT en kweek zijn onder andere uitstrijken van de blaasjesbodem, blaasjesvocht en uitstrijken van cervix of urethra. Materialen die alleen geschikt zijn voor PCR/NAAT zijn liquor (bij encefalitis), serum en plasma (bij gedissemineerde herpessimplexvirusinfectie). Voor kweek moeten wattenstokken geplaatst worden in een virustransportmedium.
Een sneltest door middel van immuunfluorescentie op de uitstrijk van een blaasjesbodem kan binnen enkele uren een antwoord bieden (Bezold 2003).
Bij vermoeden van intraoculaire herpesinfecties wordt door de oogarts materiaal uit het oog afgenomen middels een voorsteoogkamerpunctie of vitrectomie. Het materiaal wordt serologisch onderzocht op lokale productie van antistoffen door berekenen van een Goldmann Witmer-coëfficiënt. Er is sprake van een lokale productie van antistoffen als deze coëfficiënt groter is dan 3. Tevens wordt door middel van NAAT de aanwezigheid van DNA van HSV-1 of -2 bepaald
In de diagnostiek van neonatale herpes kan onderzoek worden gedaan van: (ethyleendiaminetetra-azijnzuur)-bloed, urine, nasofaryngeale uitstrijk, conjunctiva, huidblaasjes (indien aanwezig), en liquor cerebrospinalis voor PCR/NAAT.
Indirecte diagnostiek
Het bepalen van HSV-typespecifieke antistoffen kent in de dagelijkse praktijk weinig toepassing. De serologie kan van nut zijn in sero-epidemiologische studies en indien men wil vaststellen of de klinische verschijnselen berusten op een primaire infectie of op een recidief. Met de huidige tests zijn bij een primaire infectie op het moment van de eerste klinische verschijnselen nog geen typespecifieke antistoffen aantoonbaar (soms pas >12 weken). Dit maakt dat ook bij de eerste recidieven serologie nog negatief kan zijn. Soms treedt er zelfs seroreversie (weer negatief worden) op, een probleem dat vooral bij zwangeren zou spelen (Arvaja 1999, Eskild 2000, Van Rooijen 2016). Serologische analyses maken op basis van het typespecifieke glycoproteïne G (gG) onderscheid tussen HSV-1 (glycoproteïne G1) en HSV-2 (glycoproteïne G2). De sensitiviteit van deze glycoproteïne G-typespecifieke testen voor de detectie van HSV-antilichamen varieert tussen de 80% en 90% voor HSV-2 en tussen de 69 en 98% voor HSV-1. Foutnegatieve resultaten treden sneller op in het vroege stadium van de infectie. De specificiteit is 93-97% voor HSV-2 en 92-95% voor HSV-1 (Ashley-Morrow 2004, Mark 2007, Morrow 2003, Summerton 2007). Ondanks een redelijke specificiteit is bij lage prevalentie (dit geldt met name voor HSV-2) de positief voorspellende waarde laag. De aanwezigheid van HSV-2-typespecifieke antilichamen impliceert een anogenitale infectie. Bij gebrek aan symptomen kan een HSV-1-positieve uitslag geen onderscheid maken in anogenitale, orolabiale of een cutane infectie. Men dient rekening te houden dat zelfs testen met goede sensitiviteit en specificiteit matige positiefvoorspellende waarden hebben bij lage prevalenties.
De typespecifieke HSV-serologische testen kunnen zinvol zijn bij:
- een patiënt die niet bekend is met genitale herpes maar diens partner wel;
- zwangeren indien er tijdens de zwangerschap of baring een verdenking is op (een) primo-infectie met herpes genitalis; vergelijk met serum van het begin van de zwangerschap indien voorhanden;
- recidiverende genitale laesies zonder bekende oorzaak op moment dat deze niet zichtbaar zijn.
Typering voor bron- en contactonderzoek
Niet van toepassing.
Niet-microbiologische diagnostiek
Niet van toepassing.
Preventie
Immunisatie
Er is vooralsnog geen effectief vaccin tegen HSV-1 en -2 beschikbaar (Holmes 2008, Mindel 1998).
Algemene preventieve maatregelen
Voorlichting en persoonlijke hygiëne vormen de basis van de preventieve maatregelen. Contact met laesies of geïnfecteerd (lichaams)materiaal moet men proberen te vermijden.
Preventie van herpes labialis
Contact met actieve laesies of geïnfecteerd (lichaams)materiaal (kussen op de mond, bestek delen) dient vermeden te worden. Daarnaast is goede handhygiëne van belang.
Preventie van herpes genitalis
Preventie van herpes genitalis omvat patiëntinstructies en gebruik van condooms. Chronisch profylactische behandeling draagt mogelijk bij aan vermindering van overdracht van herpes. Counseling na de gestelde diagnose herpes genitalis omvat preventie van transmissie. Er moet worden uitgelegd dat transmissie kan plaatsvinden in afwezigheid van laesies. Indien er sprake is van een prodromale fase of als er actieve laesies zijn, wordt seksueel contact ontraden, ook met condoom.
Hoewel HSV-transmissie met condoomgebruik (ook in de asymptomatische fase) niet uitgesloten is, wegens uitscheiding van het virus op onbedekte slijmvliezen, wordt consistent condoomgebruik, ook in de asymptomatische fase, geadviseerd. Vooral bij wisselende of losse sekspartners.
>Een andere benadering van preventie is die van de chronisch suppressieve behandeling bij discordante paren. In de praktijk moeten de voordelen van chronisch suppressieve behandeling (reductie van HSV-2-transmissie van 3,6% naar 1,9% in 8 maanden; Corey 2004) afgewogen worden tegen de nadelen (medicalisering, kans op resistentieontwikkeling). Een langdurige behandeling in een vaste discordante relatie lijkt niet reëel noch zinnig (expert opinion). De (onderliggende) redenen van zorgen moet besproken worden, voordat er behandeld wordt.
Preventieve maatregelen bij neonatale herpes
Onderstaande adviezen zijn afgeleid van verschillende richtlijnen (Foley 2014).
Zwangerschap/baring
Het wordt aanbevolen om zwangeren met een anogenitale primo-infectie te verwijzen naar een gynaecoloog.
Neonaat
Ten aanzien van iemand met een (recidiverende) herpes labialis die tijdens de geboorte of in de neonatale periode intensief met het kind omgaat (ouders, familie, ziekenhuispersoneel, kraamverzorgende, verloskundige):
- Voorkom direct contact tussen de laesie(s) en het kind (bijv. niet kussen).
- Was de handen goed voor de verzorging van het kind.
- Bedek de laesies bij de verzorging van het kind met een mondmasker totdat de laesies zijn ingedroogd.
Reiniging, desinfectie en sterilisatie
Conform de LCI-richtlijn Reiniging, desinfectie en sterilisatie in de openbare gezondheidszorg.
Informatie voor personeel op de kraam- of kinderafdeling met herpes labialis en de verpleging van een moeder met herpes labialis op de afdeling is te vinden in de Multidisciplinaire richtlijn Seksueel overdraagbare aandoeningen (MDR Soa's).
Maatregelen
Meldingsplicht
HSV-infectie is geen meldingsplichtige ziekte. Voor alle artsen geldt een meldplicht aan de (Gemeentelijke gezondheidsdienst) als zij een voor hun praktijk ongewoon aantal gevallen van herpes vaststellen, als die een gevaar vormen voor de volksgezondheid (Wet Publieke Gezondheid, Hfdst V paragraaf 2, Artikel 21.3).
Inschakelen van andere instanties
Niet nodig.
Bron- en contactonderzoek
Bronopsporing
Bij HSV-infectie is bronopsporing niet nodig.
Contactonderzoek
Bij herpes labialis is contactonderzoek niet nodig.
Bij herpes genitalis heeft, gezien de relatief hoge seroprevalentie in de bevolking en het grote aantal asymptomatische HSV-1- en HSV-2-dragers, contactonderzoek weinig zin (‘don’t hunt the virus’). Het kan in vaste relaties wel zinvol zijn om de partner te waarschuwen en eventueel te testen. Zijn beide partners positief voor hetzelfde type HSV (aangetoond door kweek of NAAT of typespecifieke serologie), dan hoeven binnen de relatie verder geen preventieve maatregelen genomen te worden. Bij personen die leven met hiv kan het ook nuttig zijn de HSV-status van de partner(s) te weten als de immuniteit nog laag is (Van der Meijden 1999). Vanwege de mogelijke psychosociale belasting met negatieve impact op seksuele gezondheid is goede en duidelijke informatie over het (asymptomatische) beloop van de infectie en kans op recidieven belangrijk.
Maatregelen ten aanzien van index, contacten en bron
Voor sommige mensen is het hebben van herpes en specifiek de wetenschap dat recidieven en transmissie levenslang mogelijk zijn, omgeven met schaamte en met negatieve gevolgen voor mentale en seksuele gezondheid. Door deze gevoelens te bespreken, kan de zorgverlener de ziektelast verminderen.
Effectieve preventie van herpes labialis en genitalis is bijzonder lastig gezien de mogelijke levenslange besmettelijkheid en het feit dat herpes vaak overgedragen wordt door asymptomatische dragers. Toch kunnen bepaalde maatregelen genomen worden om de transmissiekans te verlagen. Zie hiervoor paragraaf Algemene preventieve maatregelen.
Postexpositieprofylaxe
Het geven van profylaxe aan partners of andere contacten van personen met labiale en/of genitale herpeslaesies heeft over het algemeen weinig zin.
Voor profylaxe dan wel vroegtijdige behandeling van neonatale herpes wordt verwezen naar paragraaf Preventieve maatregelen bij neonatale herpes.
Voor profylaxe dan wel onderhoudsbehandeling van patiënten wordt verwezen naar de paragraaf Behandeling.
Wering
Wering van personen met herpes labialis is vanuit volksgezondheidsperspectief niet zinvol. Wel wordt verzorgend personeel met actieve herpes labialis en werkzaam met neonaten (tot de leeftijd van 1 maand) of immuno-incompetenten aangeraden extra hygiënemaatregelen te treffen bij (Fields 2007, American 2006). Maatregelen betreffen het dragen van een mondkapje bij verzorgende werkzaamheden en het in acht nemen van goede handhygiëne. Voor aanbevelingen t.a.v. hand- en persoonlijke hygiëne voor zorgmedewerkers, zie de SRI-richtlijn.
Een voorbeeld van een herpessimplexinfectie is een (zeldzame) actieve herpetische laesie aan de vinger (fijt, ‘herpetic whitlow’).Hoewel er geen vergelijkende studies zijn verricht over transmissie bij fijt, wordt door sommige experts aangenomen dat het dragen van handschoenen mogelijk niet voldoende zou zijn om transmissie te voorkomen, en wordt verzorging van neonaten (en immuno-incompetenten) door personeel met fijt afgeraden (Fields 2007, American 2006).
Aangezien oudere, immunocompetente kinderen in principe geen kans meer hebben op het ontwikkelen van een ernstige neonatale herpesinfectie, zijn maatregelen voor personeel werkend met oudere kinderen (leidsters kinderdagverblijf, etc.) niet nodig.
Er zijn geen aanwijzingen dat personeelsleden met een herpes genitalis een besmettingskans vormen voor de patiënt bij handhaving van normale hygiëne.
Behandeling
De herpessimplexvirussen type 1 (herpes labialis) en type 2 (herpes genitalis) worden op verschillende wijze behandeld.
Herpes labialis
Zie voor behandeling herpes labialis: NHG standaard koortslip (herpes labialis).
Herpes genitalis
Op de CSG kan een indicatie gesteld worden op basis van klinisch beeld of diagnostische test om een herpes genitalis te behandelen. De indicaties voor behandeling bij herpes genitalis zijn een primo-infectie en hinderlijke recidieven. Therapie met nucleoside analoga (aciclovir afgeleide middelen) onderdrukken de replicatie van het virus, maar hebben geen effect op het latent aanwezige virus zodat na stoppen van de behandeling HSV-reactivatie kan optreden. Dit wil zeggen dat alleen de duur en de ernst van de klachten erdoor worden bekort en de virusuitscheiding wordt beperkt. Mogelijk wordt ook de transmissiekans verkleind. Er is, buiten het verkorten van de duur van de klachten, nog veel onduidelijk over de zin van behandelen.
Aanbevolen behandeling van HSV bij niet-zwangere volwassenen
Het starten van therapie bij het vermoeden van een primo-infectie wordt doorgaans uitsluitend op de klinische presentatie gedaan (binnen vijf dagen na start van de symptomen), omdat diagnostiek in de praktijk niet snel mogelijk is. Primo-infecties geven meestal meer klachten dan recidieven en worden behandeld met orale toediening van (val)aciclovir of een analoog middel (Patel 2017). Het advies om primo-infecties met milde klachten al dan niet in alle gevallen te behandelen, kan niet goed worden onderbouwd. Onduidelijk is of behandeling van een primo-infectie de recidiefkans verlaagt. Tevens is in veel gevallen een als zodanig aangeduide primo-infectie, in feite een recidief. Anderzijds ontwikkelt een herpesinfectie zich geleidelijk en kan het enige tijd duren voor kan worden vastgesteld of sprake is van een ernstige infectie, waardoor in dat geval vertraging optreedt alvorens gestart wordt met een behandeling. Een eenduidig advies is niet te geven. De arts besluit samen met de cliënt of bij primo-infecties met milde klachten een behandeling wordt gestart of dat het beloop wordt afgewacht. Er is geen plaats voor topicale behandeling met nucleoside analogons zoals aciclovircrème vanwege gebrek aan bewijs omtrent de werkzaamheid.
Immuuncompetente volwassenen (Patel 2017, Patel 2015):
- valaciclovir 500 mg p.o., 2 dd gedurende 5 dagen; OF
- aciclovir 400 mg p.o., 3 dd gedurende 5 dagen; OF
- famciclovir 250 mg p.o., 3 dd gedurende 5 dagen.
Immuno-incompetente volwassenen:
- valaciclovir 1000 mg p.o., 2 dd gedurende 10 dagen of tot re-epithelialisatie van de laesies; OF
- aciclovir 800 mg p.o., 3 dd gedurende 10 dagen of tot re-epithelialisatie van de laesies; OF
- famciclovir 500 mg p.o., 3 dd gedurende 10 dagen of tot re-epithelialisatie van de laesies.
Behandeling van zwangeren
Zwangeren met een, al dan niet primaire, herpes genitalis die veel klachten veroorzaakt, kunnen met aciclovir, valaciclovir en famciclovir behandeld worden, onafhankelijk van de duur van de zwangerschap (Westhoff 2011, Pastemak 2010, Holmes 2008, Mindel 1998). Er is wel een voorkeur voor aciclovir, omdat daar de meeste gegevens over zijn (Foley 2014, Westhoff 2011).
Factoren die de kans op transmissie van HSV naar neonaat vergroten (Pinninti 2014):
- type maternale infectie: eerste periode met primaire infectie HSV-1;
- maternale HSV-antistoffenstatus;
- wijze van partus (vaginaal of sectio caesarea);
- duur gebroken vliezen;
- integriteit huidbarrière (gebruik schedelelektrode en ander instrumentarium);
- type HSV (HSV-1 en HSV-2).
Primaire anogenitale HSV-infectie in zwangerschap
Het wordt aanbevolen om zwangeren met een anogenitale primo-infectie te verwijzen naar een gynaecoloog in verband met partusbeleid.
Behandeling:
- aciclovir 400 mg p.o., 3 dd gedurende 5 dagen; of:
- valaciclovir 500 mg p.o., 2 dd gedurende 5 dagen.
Overweeg in de laatste 4 weken van de zwangerschap: aciclovir 400 mg p.o., 3 dd OF valaciclovir 500 mg p.o., 2 dd.
Behandeling van overige ziektebeelden door HSV
Voor de behandeling van herpes encefalitis, herpes keratitis, neonatale herpes en andere ziektebeelden geassocieerd met een HSV-infectie wordt verwezen naar de betreffende gespecialiseerde literatuur. Deze behandeling vindt over het algemeen plaats in de tweede lijn. Zie onder andere de Multidisciplinaire richtlijn Seksueel overdraagbare aandoeningen (MDR Soa's).
Behandeling van HSV bij kinderen
Zie voor de behandeling van kinderen de MDR Soa's, paragraaf Behandeling van HSV bij pasgeborenen en kinderen.
Behandeling van complicaties bij volwassenen
Indien er complicaties aanwezig zijn, is klinische behandeling aangewezen, eventueel met intraveneuze antivirale therapie. Intraveneuze antivirale therapie is ook aangewezen bij neurologische complicaties (o.a. meningo-encefalitis) en ernstige HSV-infectie.
Bij oogheelkundige herpesaandoeningen dient met spoed verwezen te worden naar de oogarts. Bij een herpetische keratitis kan de infectie in verschillende lagen van het hoornvlies tot uiting komen, waarvoor vaak tot één jaar orale systemische antivirale (valaciclovir) en lokale behandeling (steroïden, aciclovir) noodzakelijk is.
Behandeling bij recidief/onderhoudsbehandeling
Bij behandeling van een recidief kan volstaan worden met een indrogende therapie, bijvoorbeeld indifferente crème met zinkoxide of zinksulfaat (zinkoxide vaselinecrème 10% (Formularium der Nederlandse Apothekers) of zinksulfaat vaselinecrème 0,5% FNA) (Farmacotherapeutisch kompas 2017). Bij veel pijnklachten kan pijnstilling worden gegeven (lokaal: lidocaïne crème zinkoxidesmeersel 5% FNA of in combinatie met systemische pijnstilling). Het is belangrijk alert te zijn op eventuele secundaire bacteriële infecties en deze te behandelen.
Over de behandeling bestaat een grote mate van consensus. In vrijwel alle richtlijnen worden dezelfde behandelschema’s gepresenteerd (Patel 2017, CDC 2015, Holmes 2008). Bij recidiefinfecties wordt zo snel mogelijk, maar in ieder geval binnen 48 uur na het ontstaan van de eerste tekenen (prodromen), met de antivirale medicatie gestart om enig effect te kunnen bewerkstelligen. Het is dan ook aan te bevelen bij frequente en/of hinderlijk ervaren recidieven de cliënt een voorraad in huis te laten halen, om bij het begin van een volgende episode direct te kunnen starten.
Immuun(in)competente volwassenen (Patel 2017):
- valaciclovir 500 mg p.o., 2 dd gedurende 5 dagen; OF
- aciclovir 400 mg p.o., 3 dd gedurende 5 dagen; OF
- famciclovir 125 mg p.o., 2 dd gedurende 5 dagen.
Korte therapieën zijn te overwegen bij frequente recidieven (Patel 2017):
- valaciclovir 500 mg p.o., 2 dd gedurende 3 dagen; OF
- aciclovir 800 mg p.o., 3 dd gedurende 2 dagen; OF
- famciclovir 1000 mg p.o., 2 dd voor 1 dag.
Onderhoudsbehandeling
Personen met zeer frequente recidiefinfecties (>6/jaar) en veel klachten komen in aanmerking voor onderhoudstherapie met (val)aciclovir of een analoog middel. Antivirale therapie voor recidiverende herpes genitalis reduceert het aantal recidieven met 70-80% en verkort de duur van de laesies.
Onderhoudsbehandeling om recidieven te voorkomen:
- valaciclovir 500 mg p.o., 1 dd;
- valaciclovir 1000 mg p.o., 1 dd;
- aciclovir 400 mg p.o., 2 dd;
- famiciclovir 250 mg p.o., 2 dd.
Behandeling bij therapieresistente groepen
In studies blijkt, van de immuungecompromitteerde deelnemers, ongeveer 5% resistent te zijn voor HSV-stammen. Helicase-primaseremmers (zoals amenamevir en pritelivir) vormen een nieuwe klasse van krachtige antivirale middelen (Kawashima 2017). Hiervoor dient verwezen te worden naar de tweede lijn (zie ook MDR Soa's).
Controle
Indien aanhoudende klachten, of wanneer complicaties of ernstig verloop wordt gevreesd (bijvoorbeeld vanwege een onderliggend lijden).
Indien keuze voor profylaxebehandeling: evalueer na 6-12 maanden en bespreek of medicatie op proef kan worden gestaakt. Hervat medicatie als na het staken frequent recidieven optreden (≥twee episoden in korte tijd) en evalueer vervolgens jaarlijks.
Literatuur
- American Academy of Pediatrics. Herpes simplex. In: Pickering LK et al. Red Book: 2006 Report of the Committee on Infectious Deseases. 27th Edition. Elk Grove: American Academy of Pediatrics; 2006: 361-371.
- Aronson PL et al. Delayed acyclovir and outcomes of children hospitalized with eczema herpeticum. Pediatrics 2011; 128 (6): 1161-1167.
- Arvaja M et al. Serological evaluation of herpes simplex virus type 1 and type 2 infections in pregnancy. Sex Transm Infect 1999; 75: 168-171.
- Ashley-Morrow R et al. Performance of focus (enzym-linked immuno sorbent assay) tests for herpes simplex virus type 1 (HSV-1) and (herpessimplexvirus)-2 antibodies among women in ten diverse geographical locations. Clin Microbiol Infect 2004; 10: 530-536.
- Bagdades EK et al. Relationship between herpes simplex virus ulceration and CD4+ cell counts in patients with HIV infection. AIDS 1992; 6 (11): 1317-1320.
- van der Beek MT et al. Viral loads and antiviral resistance of herpesviruses and oral ulcerations in hematopoietic stem cell transplant recipients. Bone Marrow Transplant 2012; 47: 1222-1228.
- Benedetti J, Corey L, Ashley R. Recurrence rates in genital herpes after symptomatic first-episode infection. Annals of Internal Medicine 1994; 121: 847-854.
- Benedetti JK, Zeh J, Corey L. Clinical reactivation of genital herpes simplex virus infection decreases in frequency over time. Annals of Internal Medicine 1999; 131: 14-20.
- Bezold GL. Detection of cutaneous herpes simplex virus infections by immunofluorescence vs. PCR. J Eur Acad Dermatol Venereol 2003; 17 (4): 430-433.
- CDC. Genital herpes infections. In: Sexually transmitted infections treatment guidelines, 2021. Atlanta: Centers for Disease Control and Prevention; 2021. Via: cdc.gov.
- Celum CL, Robinson NJ, Cohen MS. Potential effect of HIV type 1 antiretroviral and herpes simplex virus type 2 antiviral therapy on transmission and acquisition of HIV type 1 infection. J Infect Dis 2005; 191 Suppl 1: S107-S114.
- Corey L et al. Once-daily valacyclovir to reduce the risk of transmission of genital herpes. N Engl J Med 2004; 350: 11-20.
- Daha, T. Herpes simplex virus. Tijdschrift Hygiëne en Infectiepreventie 1997; 4: 144.
- Drake S et al. Improving the care of patients with genital herpes. BMJ 2000; 321: 619-623.
- Douglas RG Jr, Couch RB. A prospective study of chronic Herpes simplex virus infection and recurrent herpes labialis in humans. J Immunol 1970; 104 (2): 289-95.
- Engelberg P et al. Natural history of genital herpes simplex virus type 1 infection. Sex Transm Dis 2003; 30: 174-177.
- Eskild A et al. Herpes simplex virus type-2 antibodies in pregnant women: the impact of the stage of pregnancy. Epidemiol Infect 2000; 125: 685-692.
- Farmacotherapeutisch kompas. 2017. Via: farmacotherapeutischkompas.nl.
- Foley E et al. Management of genital herpes in pregnancy. BASHH/RCOG; 2014.
- Forsgren M, Klapper PE. Herpes simplex virus type 1 and type 2. In: Zuckerman AJ et al. Principles and practice of clinical virology. 6th Edition. Wiley-Blackwell, 2009: 124-126.
- Gray RH et al. Determinants of HIV-1 load in subjects with early and later HIV infections, in a general-population cohort of Rakai, Uganda. J Infect Dis 2004; 189: 1209-1215.
- Holmes KK et al. Sexually transmitted diseases. 4th Edition. New York: McGraw-Hill, 2008.
- James SH, Kimberlin DW. Neonatal herpes simplex virus infection. Infect Dis Clin North Am 2015; 29: 391-400.
- Johnston C et al. Viral shedding 1 year following first-episode genital HSV-1 infection. JAMA 2022; 328 (17): 1730-1739.
- Kawashima M et al. Amenamevir, a novel helicase-primase inhibitor, for treatment of herpes zoster: A randomized, double-blind, valaciclovir-controlled phase 3 study. J Dermatol 2017; 44 (11): 1219-1227.
- Kimberlin DW. Herpes simplex infections in neonates and early childhood. Semin Pediatr Infect Dis 2005; 16: 271-281.
- Lafferty WE et al. Recurrences after oral and genital herpes simplex virus infection: influence of site of infection and viral type. N Engl J Med 1987; 316: 1444-1449.
- Langenberg AG et al. A prospective study of new infections with herpes simplex virus type 1 and type 2. N Engl J Med 1999; 341: 1432-1438.
- Luca NJ, Lara-Corrales I, Pope E. Eczema herpeticum in children: clinical features and factors predictive of hospitalization. J Pediatr 2012; 161 (4): 671-675.
- Mandell GL et al. Herpes simplex virus: neonatal herpes. Chapter 132 in: Mandell, Douglas, and Bennett’s principles and practice of infectious diseases. 6th edition. Churchill Livingstone; 2005: 1772.
- Mark HD et al. Performance of focus ELISA tests for HSV-1 and HSV-2 antibodies among university students with no history of genital herpes. Sex Transm Dis 2007; 34: 681-685.
- Mark KE et al. Rapidly cleared episodes of herpes simplex virus reactivation in immunocompetent adults. J Infect Dis 2008; 198: 1141-1149.
- van der Meijden WI. Expertmeeting partnerwaarschuwing: zin en onzin van partnerwaarschuwing bij virale SOA. Notulen 1999.
- Mindel A. Genital herpes: how much of a public health problem? Lancet 1998; 351 (suppl 3): 16-18.
- Morrow RA, Friedrich D, Krantz E. Performance of the focus and kalon enzyme-linked immunosorbent assays for antibodies to herpes simplex virus type 2 glycoprotein G in culturedocumented cases of genital herpes. J Clin Microbiol 2003; 41: 5212-5214.
- Nagot N et al. Reduction of HIV-1 RNA levels with therapy to suppress herpes simplex virus. N Engl J Med 2007; 356: 790-799.
- van Oeffelen L et al. Update on neonatal herpes simplex epidemiology in the Netherlands: a health problem of increasing concern? Pediatr Infect Dis J 2018; 37 (8): 806-813.
- Patel R et al. 2017 European guidelines for the management of genital herpes. Int J STD AIDS 2017; 28 (14): 1366-1379.
- Patel R et al. 2014 UK national guidelines on the management of anogenital herpes. Int J STD AIDS 2015; 26: 763-776.
- Pellet PE, Roizman B. Herpesviridae. In: Knipe DM, Howley PM. Fields Virology. 6th Edition. Wolters Kluwer/Lippincott Williams & Wilkins, 2013: 1802-1822.
- Phipps W et al. Persistent genital herpes simplex virus-2 shedding years following the first clinical episode. J Infect Dis 2011; 203: 180-187.
- Pinninti SG et al. Neonatal herpes disease following maternal antenatal antiviral suppressive therapy: a multicenter case series. J Pediatr 2012; 161 (1): 134-138.
- Pinninti SG, Kimberlin DW. Management of neonatal herpes simplex virus infection and exposure. Arch Dis Child Fetal Neonatal Ed 2014; 99 (3): F240-F244.
- Quinnan GV Jr et al. Herpesvirus infections in the acquired immune deficiency syndrome. JAMA 1984; 252 (1): 72-77.
- Roest RW, van der Meijden WI. Herpes genitalis. Soa Bulletin 1999; 20 (jubileumnummer).
- van Rooijen MS et al. False-negative type-specific glycoprotein G antibody responses in STI clinic patients with recurrent HSV-1 or HSV-2 DNA positive genital herpes, The Netherlands. Sex Transm Infect 2016; 92: 257-260.
- Schacker T et al. Changes in plasma human immunodeficiency virus type 1 RNA associated with herpes simplex virus reactivation and suppression. J Infect Dis 2002; 186: 1718-1725.
- Schiffer JT et al. The kinetics of mucosal herpes simplex virus-2 infection in humans: evidence for rapid viral-host interactions. J Infect Dis 2011; 204: 554-561.
- Schmitt DL, Johnson DW, Henderson FW. Herpes simplex type 1 infections in group day care. Pediatr Infect Dis J 1991; 10 (10): 729-734.
- Scott JH, Kimberlin DW. Neonatal herpes simplex infection. Inf Dis Clin North Am 2015; 29: 391-400.
- Severson JL, Tyring SK. Relation between herpes simplex viruses and human immunodeficiency virus infections. Arch Dermatol 1999; 135 (11): 1393-1397.
- Suissa CA et al. Investigating the survival of herpes simplex virus on toothbrushes and surrogate phallic devices. Int J STD AIDS 2023; 34 (3): 152-158.
- Summerton J et al. Effect of sexually transmitted disease (STD) coinfections on performance of three commercially available immunosorbent assays used for detection of herpes simplex virus type 2-specific antibody in men attending Baltimore, Maryland, STD clinics. Clin Vaccine Immunol 2007; 14: 1545-1549.
- Tata S et al. Overlapping reactivations of herpes simplex virus type 2 in the genital and perianal mucosa. J Infect Dis 2010; 201: 499-504.
- Tronstein E et al. Genital shedding of herpes simplex virus among symptomatic and asymptomatic persons with HSV-2 infection. JAMA 2011; 305: 1441-1449.
- Wald A et al. Effect of condoms on reducing the transmission of herpes simplex virus type 2 from men to women. JAMA 2001; 285: 3100-3106.
- Wald A et al. Polymerase chain reaction for detection of herpes simplex virus (HSV) DNA on mucosal surfaces: comparison with HSV isolation in cell culture. J Infect Dis 2003; 188: 1345-1351.
- van Wees DA et al. Sexually transmitted infections in the Netherlands in 2021. (Rijksinstituut voor Volksgezondheid en Milieu) Rapport 2022-0023. Bilthoven: Rijkinstituut voor Volksgezondheid en Milieu; 2022.
- Westhoff GL, Little SE, Caughey AB. Herpes simplex virus and pregnancy: a review of the management of antenatal and peripartum herpes infections. Gynecol Surv 2011; 66: 629-638.
- (World Health Organization). Guidelines for the treatment of genital herpes simplex virus. World Health Organization; 2016.
- Woestenberg PJ et al. Herpes simplex virus type 1 and type 2 in the Netherlands: seroprevalence, risk factors and changes during a 12-year period. BMC Infect Dis 2016; 16: 364.