Praktijkrichtlijn voor bedrijfsartsen: hepatitis B-vaccinatie van risicolopend (geen risicovormend) personeel
Deze praktijkrichtlijn is een bijlage bij de LCI-richtlijn Hepatitis B. | Versie juni 2024 (versiebeheer: zie onder aan deze pagina)
Voor hepatitis B-vaccinatie van (mogelijk) risicovormend personeel: zie de Landelijke richtlijn preventie transmissie van hepatitis B van medisch personeel naar patiënten, ook te vinden via de pagina Hepatitis B en C en hiv: preventie van iatrogene transmissie.
Voorwoord
In sommige beroepsgroepen is er een verhoogd risico op een infectie met hepatitis B. Hierbij denken we in eerste instantie vaak aan personeel dat medische handelingen verricht bij patiënten, maar ook medewerkers in andere beroepsgroepen kunnen een verhoogd risico hebben op een infectie met hepatitis B. Vaststellen van een verhoogd risico gebeurt aan de hand van een risico inventarisatie en evaluatie. Een werkgever is verantwoordelijk dat het arbobeleid in zijn bedrijf of instelling wordt nageleefd en moet preventieve maatregelen nemen waar dat nodig is. Deze praktijkrichtlijn is bedoeld voor werkgevers en bedrijfsartsen om de indicatie voor preventieve vaccinatie tegen hepatitis B vast te stellen en preventieve hepatitis B-vaccinatie te implementeren bij risicolopers.
1 Welke personeelsleden vaccineren?
De bedrijfsarts adviseert de werkgever en de werknemer op basis van een risico-inventarisatie en evaluatie (RIE) wie voor vaccinatie tegen hepatitis B in aanmerking komt. De bedrijfsarts heeft vier, elkaar aanvullende, criteria bij deze inschatting tot zijn/haar beschikking. Zie bijlagen 1 en 2 en het advies ‘werknemers en infectieziekten’ van de Gezondheidsraad (3):
- De werknemer verricht medische, verplegende of verzorgende handelingen bij cliënten of patiënten.
- De werknemer kan in contact komen met lichaamsmaterialen zoals bloed, serum, ascites, vruchtwater, etc. Excreten, zoals urine, feces en speeksel vormen geen risico voor het besmet raken met hepatitis B, tenzij er bloed in aanwezig is.
- Uit de RIE kan blijken dat ook ander personeel in aanmerking komt voor vaccinatie.
- De prikaccidentenregistratie kan uitwijzen dat in de praktijk prikaccidenten optreden bij ander personeel dan op basis van de arbobeleidsregel en de RIE als risicolopend was aangemerkt.
Ook werknemers die in opleiding zijn en studenten of stagiaires lopen risico op accidenteel (bloed) contact. Het is met name bij deze groepen belangrijk dat ook zij beschermd zijn tegen een infectie met het hepatitis B-virus (HBV). De Gezondheidsraad adviseert om al tijdens de opleiding de mogelijkheid tot vaccinatie te bieden, zodat bij aanvang van stages of praktijkwerk de benodigde bescherming is bereikt (Gezondheidsraad 1996; rapport ‘Bescherming tegen hepatitis B’, publicatie nummer 1996/15). Juist leerlingen zijn vaak onervaren en lopen daardoor een verhoogd risico.
Naast de medische, verplegende en verzorgende beroepen zijn er ook andere beroepsgroepen waar vaccinatie sterk aanbevolen wordt, denk bijvoorbeeld aan werkenden in de uitvaart, werknemers van de politie, brandweer, etc.
Van volledige bescherming tegen het HBV is pas sprake na een volledige vaccinatiereeks en na aantonen van een voldoende hoeveelheid antistoffen. Vanaf 2002 wordt in Nederland een postvaccinatietiter van gelijk aan of hoger dan 10 IU/l als indicator voor langdurige bescherming tegen acute hepatitis B beschouwd (Briefadvies Hepatitis B-vaccinatie, Gezondheidsraad 2002).
Een screening op hepatitis B voorafgaand aan de vaccinatie is niet nodig. Deze richtlijn heeft betrekking op risicolopers. Het geven van de vaccinatie aan personen die met het hepatitis B-virus besmet zijn heeft geen nadelige gevolgen. Hepatitis B-dragerschap blijkt in de regel uit een positieve HBsAg-bepaling die volgt na de non-respons op de vaccinatie.
2 Wat zijn weer risicolopers en risicovormers?
Risicolopers zijn werknemers of personen die door hun werkzaamheden of gedrag risico kunnen lopen op een infectie met het hepatitis B-virus. Zie bijlage 1.
Risicovormers zijn werknemers in de gezondheidszorg die door de handelingen die ze verrichten een patiënt zouden kunnen besmetten indien hij of zij zelf geïnfecteerd is met het hepatitis B-virus. Risicovormers zijn ook risicolopers, echter vanwege de vereiste veiligheid voor patiënten gelden voor risicovormend personeel aanzienlijk strengere regels met betrekking tot HBV-preventie (bijvoorbeeld het weigeren van vaccinatie heeft vergaande consequenties). Het landelijk verplichte beleid voor risicovormend personeel wordt beschreven in de Landelijke richtlijn preventie transmissie van hepatitis B van medisch personeel naar patiënten. Ook de afbakening van wel en niet risicovormende handelingen en de speciale titercontrole na vaccinatie staan beschreven in deze richtlijn.
Vanwege het detaillistische beleid bij risicovormend personeel wordt op deze plaats geen samenvatting of impressie van dat beleid gegeven, maar verwezen naar de Landelijke richtlijn preventie transmissie van hepatitis B van medisch personeel naar patiënten.
3 Praktische aspecten
3.1 Voorlichting
Voor aanvang van HBV-vaccinatie wordt betrokkene in een gesprek geïnformeerd over:
- hygiënisch en veilig werken;
- hepatitis B (ziekte, overdracht, preventie);
- het eigen beslissingsrecht inzake vaccinatie van de werknemer;
- de procedure van vaccinatie;
- de beperkte bescherming tegen HBV-infectie gedurende de vaccinatieperiode;
- de aanwezig blijvende kans op infectie met andere bloedoverdraagbare aandoeningen;
- de definitie van een prik-, snij-, bijt- of spataccident;
- het bestaan en de werkwijze van het prikaccidentenprotocol;
- de blijvende noodzaak van melden van prikaccidenten;
- de noodzaak dat betrokkene zijn/haar vaccinatiegegevens (en met name de titeruitslag) goed bewaart.
Voorafgaand aan de vaccinatieprocedure wordt een anamnese afgenomen en worden eventuele voorzorgsmaatregelen genomen (zie bijlage 3).
Voor de werkgever of de organisatie is het noodzakelijk een registratie bij te houden van de vaccinatiegegevens van de werknemer en daarbij vast te leggen:
- risicovormer/risicoloper;
- beschermd/onbeschermd/onbekend;
- datum titerbepaling.
Daarnaast is het voor een werkgever belangrijk op de hoogte te zijn van de EU-regelgeving omtrent preventie van scherpe letsels in de ziekenhuis- en gezondheidszorgbranche, vastgelegd in Richtlijn 2010/32/EU die te vinden is op de website Eur-lex.europa.eu, waarin nadruk gelegd wordt op een veilige werkomgeving en het voorkomen van letsels, o.a. door werken met veilige systemen (4).
Het is nuttig om de mondelinge informatie te ondersteunen met schriftelijk materiaal dat aan de werknemer wordt meegegeven.
Het RIVM heeft informatie over hepatitis B op de RIVM-website beschikbaar.
Zie bijlage 4 voor bevoegdheden van artsen en verpleegkundigen in het kader van de uitvoering van de hepatitis B-vaccinatie.
3.2 Beschikbare HBV-vaccins
Alle in Nederland geregistreerde vaccins bevatten recombinant hepatitis B-eiwitten (HBsAg) en zijn recombinant subunit vaccins. Verkrijgbare vaccins voor gezonde volwassenen zijn:
- HBV: Engerix-B®: 20 µg HBsAg per dosis van 1 ml (thiomersal-arm);
- HBV: HB-VAX-PRO: 10 µg HBsAg per dosis van 1 ml (thiomersal-vrij);
- HBV+HAV: Twinrix® (combinatievaccin): 20 µg HBsAg + 720 EU geïnactiveerd HAV per dosis van 1 ml (thiomersal-arm).
Zowel Engerix-B® als HB-VAX-PRO kan gegeven worden aan personen van 16 jaar en ouder. Voor personen tot en met 15 jaar bestaan junior-doseringen die volgens hetzelfde schema (bijlage 5 en paragraaf 3.4) gegeven worden als de vaccins voor volwassen. De juniorvariant van Twinrix® is Ambirix®, waarvan twee in plaats van drie doses gegeven worden.
Wanneer uit de RIE blijkt dat werknemers kans lopen op blootstelling aan hepatitis B- en hepatitis A-virus, kan gelijktijdige immunisatie overwogen worden (bijvoorbeeld bij werknemers in de verstandelijk gehandicaptenzorg of werknemers die naar het buitenland uitgezonden worden). Hierbij kan men gebruik maken van één gecombineerd vaccin of twee aparte vaccins tegen hepatitis A en B.
NB: bij personen met een nierziekte wordt Fendrix® of een vaccin met een verhoogde dosis (HBVaxPro40) aanbevolen, of een dubbele dosis van een standaard vaccin Engerix-B® of HBVaxPro10.
NB: Bij hivpositieven wordt een ander schema aangehouden. Zie daarvoor de LCI-richtlijn Personen met hiv vaccineren binnen het Vaccinatieprogramma hepatitis B-risicogroepen, die te vinden is als bijlage bij het LCI-draaiboek Hepatitis B-vaccinatieprogramma voor risicogroepen.
3.3 Wijze van toediening HBV-vaccin
Eén dosis bestaat uit 1 ml intramusculaire toediening, in de musculus deltoideus.
Toediening in de bilspier of subcutane toediening kunnen leiden tot niet-optimale immuunrespons.
3.4 Toedieningsschema HBV-vaccin
(Zie ook bijlage 5.)
Het standaardschema omvat drie injecties, als volgt:
| Eerste bezoek | Maand 0 | Voorlichting, uitleg over vaccinatie (zie 3.1), eerste vaccinatie |
| Tweede bezoek | Maand 1 | Tweede vaccinatie |
| Derde bezoek | Maand 6 | Derde vaccinatie |
| Vierde bezoek (4 tot 8 weken na derde vaccinatie) | Maand 7 | Bloedafname voor anti-HBs-titerbepaling |
De tijd tussen de eerste en tweede dosis is minimaal 3 weken en maximaal 2 maanden. De derde dosis kan 5 tot 12 maanden na de eerste dosis gegeven worden. De titerbepaling moet 4 tot 8 weken na de laatste vaccinatie plaats te vinden.
Wanneer iemand aangeeft in het verleden gevaccineerd te zijn tegen hepatitis B volgens het standaardschema, maar geen bewijs van vaccinatie en geen titeruitslag heeft, kan alleen volledige zekerheid worden verkregen over de mate en duur van bescherming tegen een HBV-infectie als een volledig vaccinatieschema wordt toegediend gevolgd door een titercontrole. Gezien het relatieve lage risico bij risicolopers kan in voorkomende gevallen worden volstaan met een booster (1x) vaccinatie gevolgd door titercontrole.
Er bestaan versnelde schema’s die veelal een vierde dosis vereisen en daardoor duurder zijn. Deze schema’s kunnen in bijzondere situaties gebruikt worden, namelijk als er op korte termijn bescherming bereikt moeten worden. De mate van tussentijdse bescherming voor de derde vaccinatie is echter niet duidelijk en niet compleet, en een vierde injectie op maand 12 is nodig voor langdurige bescherming. Voor werknemers heeft het normale schema, waarvan de effectiviteit bewezen is, de voorkeur.
3.5 Bijwerkingen, contra-indicaties, interacties
Bij 1 op de 10 tot 1 op de 100 gevaccineerden wordt pijn, jeuk, roodheid of zwelling op de injectieplaats gemeld; dit verdwijnt binnen 48 uur.
Vermoeidheid, koorts, griepachtige verschijnselen komen bij 1 op de 100 tot 1 op de 10.000 gevaccineerden voor. Anafylactische reacties komen in minder dan 1 op de 10.000 gevaccineerden voor. Zie ook bijlage 6.
Relatieve contra-indicaties zijn allergie voor vaccincomponenten en eerdere anafylactische reacties. Er zijn geen specifieke contra-indicaties en geen specifieke interacties bekend bij HBV-vaccinatie. Bij vaccinatie geldt wel de algemene regel dat bij ernstige ziekte of koorts (> 38,5 °C) de vaccinatie, waar mogelijk, uitgesteld moet worden. In analogie aan de vaccinatieregels van het Landelijk Coördinatiecentrum Reizigersadvisering (LCR) kunnen verschillende soorten vaccins tegelijkertijd of op verschillende tijden toegediend worden.
Zwangeren die behoren tot een risicogroep krijgen het advies zich ondanks de zwangerschap te laten vaccineren. Vaccinatie is ook in het belang van het ongeboren kind omdat een hepatitis B-besmetting kan leiden tot perinatale besmetting. Op theoretische gronden heeft hepatitis B-vaccinatie geen nadelige consequenties voor de zwangerschap en er zijn vanuit de praktijk ook geen aanwijzingen daarvoor. Het geven van borstvoeding is geen reden om vaccinatie uit te stellen. Zie eventueel de LCI-richtlijn Hepatitis B.
3.6 Beschermingsduur
Gedurende de vaccinatieperiode, vanaf twee weken na de eerste vaccinatie tot aan de postvaccinatietiter is enige bescherming te verwachten van het vaccin. Niettemin moeten werknemers gedurende deze gehele periode als onbeschermd beschouwd worden.
Indien na een volledige serie HBV-vaccinaties een anti-HBs-titer gelijk aan of groter dan 10 IU/L bereikt wordt, geeft dit langdurig bescherming (5, 6, 7, 8, 9, 10). Op basis van de huidige literatuur kan men uitgaan van een beschermingsduur van dertig jaar (6, 7, 9, 10). Er is vooralsnog geen reden om mensen die ooit een anti-HBs-titer vertoonden van minstens 10 IU/L te revaccineren (6). Het is waarschijnlijk dat succesvolle vaccinatie (titer gelijk aan of hoger dan 10 IU/L) levenslang bescherming biedt. Verder onderzoek zal dit echter moeten bevestigen. Het is belangrijk dat de bedrijfsarts de vaccinatiegegevens van werknemers registreert en bij verandering van werkkring overdraagt aan de opvolgende bedrijfsarts. Voor de werknemers is het belangrijk dat zij ook zelf hun vaccinatiegegevens bewaren.
3.7 Postvaccinatietiter
(Zie ook bijlage 5.)
Om bescherming tegen hepatitis B bij risicolopende werknemers aan te tonen dient 4 tot 8 weken na de laatste vaccinatie een anti-HBs-titerbepaling verricht te worden. Een anti-HBs > 10 IU/L is beschermend. (7)
Bij ca. 95% van de jonge gezonde volwassenen is na de volledige serie voldoende antistoffen (minstens 10 IU/L) aantoonbaar. Bij personen bij wie de anti-HBs na drie vaccinaties nog < 10 IU/L is, moeten als onbeschermd aangemerkt worden (non-responder na drie vaccinaties). De volgende factoren, in volgorde van belangrijkheid, verminderen de kans op een goede respons: hogere leeftijd (> 40 jr), roken, obesitas, mannelijk geslacht, genetische factoren, medicijngebruik (met name immunosuppressiva).
Chronische HBV-infectie kan zich voordoen als oorzaak van een non-respons, daarom moet bij non-responders een test op HBsAg en op anti-HBcore ingezet worden.
Goede respons (minstens 10 IU/L)
Indien de anti-HBs-titer minstens 10 IE/L bedraagt, is men langdurig beschermd tegen hepatitis B. De gevaccineerde werknemer dient een vaccinatiebewijs te ontvangen waarop personalia, de datum van vaccinatie en titerbepaling en de antistoftiter vermeld staan.
Non-responders (< 10 IU/L)
Aanvullende vaccinaties kunnen verricht worden, met als doel om alsnog een immuunrespons te induceren. Dit mag pas gebeuren na uitsluiten van HBV-infectie, na overleg hierover met de betrokkene, met behulp van een test op HBsAg en op anti-HBcore (zie bijlage 5). Bij een positieve en bevestigde HBsAg-test moet de gevonden HBV-infectie gemeld worden aan de GGD, met doorverwijzen naar huisarts of MDL-arts. In geval van HBV-infectie is revaccinatie niet zinvol.
3.8 Revaccinatieschema voor non responders met negatief anti-Hbc
Als de anti-HBc negatief is, wordt advies tot een revaccinatieschema gegeven. De kans op seroconversie naar een anti-HBs ≥ 10 IU/l na 1 revaccinatie hangt af van de titerhoogte (aantal IU anti-HBs/L) van de non-responder na de eerste vaccinatiereeks. Aanbevolen wordt dat laboratoria een anti-HBs titerbepaling < 10 IU/l kwantificeren met vermelding van de detectiegrens (‘limit of detection’) van het assay. Non-responders zonder aantoonbare antistoffen (anti-HBs kleiner dan de detectielimiet van de gebruikte test) zijn zero-responders. Non-responders met een titer kleiner dan 10 IU/l maar gelijk aan of boven de detectielimiet van het gebruikte test zijn poor-responders.
Op basis van de hoeveelheid anti-HBs kan gekozen worden voor een aangepast revaccinatieschema (bijlage 5) voor poor-responders of zero-responders. voor het standaard revaccinatieschema van 3 revaccinaties gegeven met telkens 1 maand ertussen voor b) zero-responders (zie Hepatitis B non-responders).
Geef 1 revaccinatie en bepaal na 4 tot 8 weken de anti-HBs titer. Indien de titer onder de 10 IU/l blijft, geef dan alsnog 2 revaccinaties met telkens 1 maand ertussen, waarna 4 tot 8 weken na de laatste revaccinatie wederom controle van de titer plaatsvindt (zie bijlage 5). Indien de titerhoogte onder de 10 IU/l niet bekend is, dient het revaccinatieschema van de zero-responder gevolgd te worden (bijlage 5). Vier tot acht weken na revaccinatie volgens bijlage 5 volgt anti-HBs-titerbepaling. Wanneer de anti-HBs-titer ook na zes inentingen minder is dan 10 IU/L, is er sprake van definitieve non-respons. Volgens protocol wordt er geen actie ondernomen t.a.v. verdere vaccinatie voor risicolopers. Bij blootstelling van een non-responder aan HBV of bij blootstelling tijdens de vaccinatieserie dient HBIg toegediend te worden, conform de Landelijke Richtlijn Prikaccidenten (12).
Voor de revaccinatie bestaan meerdere mogelijkheden, zoals het zelfde vaccin nogmaals gebruiken, of overgaan op vaccins met een hogere antigeendosering (bijvoorbeeld HBVaxPro-40) of een krachtiger adjuvans (Fendrix). HBVax-pro-40 of Fendrix kunnen overwogen worden wanneer het risico op blootstelling aan hepatitis B-virus hoog is (o.a. seksuele partners van chronische HBV-dragers), een hoge anti-HBs-titer gewenst is (o.a. risicovormers) en/of bij afwezigheid van antistoffen tegen HBsAg (zero-responder) na een primaire vaccinatieserie. Een informed consent voor gebruik van deze vaccins is belangrijk, gezien de off-label-status van deze vaccins voor gezonde non-responders.
Bijlagen
Bijlage 1. Wie komen er in aanmerking voor vaccinatie?
Deze lijst dient als hulpmiddel bij de overweging of er een risico op besmetting met hepatitis B te verwachten is en kan derhalve niet compleet zijn. Onderzoek op de werkvloer op basis van een RIE kan verdere ondersteuning bieden.
Op basis van een te verwachten risico op besmetting door het uitvoeren van medische handelingen of anderszins kans op contact met lichaamsvloeistoffen, komen in aanmerking:
- artsen, verpleegkundigen, verzorgenden en paramedici die geregeld met bloed in aanraking komen of met ander patiëntmateriaal dat met humaan bloed verontreinigd is, of met lichaamsvloeistoffen zoals serum, ascites, vruchtwater (uitgezonderd urine en feces);
- patholoog-anatomen en werknemers die met niet gefixeerd potentieel besmet materiaal werken;
- personeel van hemodialyseafdelingen dat bij de patiëntenzorg of bij de techniek van de hemodialyseprocedure betrokken is, inclusief werknemers in het technisch onderhoud;
- personeel van laboratoria, dat geregeld met bloed of bloedproducten in aanraking komt;
- verloskundigen en kraamverzorgsters;
- tandartsen, mondhygiënisten, tandartsassistenten en indirect bij de tandheelkundige patiëntenzorg betrokkenen, die kans lopen te worden besmet;
- werknemers die proefdieren verzorgen in laboratoria waar met het hepatitis B-virus gewerkt wordt;
- werknemers in ziekenhuizen, verpleeghuizen en zorginstellingen die schoonmaakwerkzaamheden verrichten of afval verwijderen en wanneer een gerede kans op besmetting bestaat;
- werknemers die niet-gefixeerd, potentieel besmet pathologisch materiaal vervoeren wanneer een gerede kans op besmetting bestaat;
- studenten, stagiaires en leerlingen van alle bovengenoemde beroepen en instellingen, voor zover hun werk of studie mogelijk contact met bloed meebrengt.
De Gezondheidsraad adviseert om al tijdens de opleiding de mogelijkheid tot vaccinatie te bieden, zodat bij aanvang van stages of praktijkwerk de benodigde bescherming is bereikt. Juist leerlingen zijn vaak onervaren en lopen een verhoogd risico. Omdat van volledige bescherming tegen het HBV pas sprake is na een serie van drie vaccinaties en een aantoonbaar voldoende hoeveelheid antistoffen, is het zaak om tijdig te beginnen. Leerlingen en stagiaires moeten ook als werknemers worden beschouwd.
Daarnaast worden ook andere werknemers gevaccineerd als uit de risico-inventarisatie en -evaluatie (RIE) blijkt dat er bij hen sprake is van verhoogd risico. Een RIE op het punt van bloedoverdraagbare aandoeningen is daarom noodzakelijk voor alle functies waarbij een beroepsgebonden risico kan bestaan.
Ook kan de prikaccidentenregistratie uitwijzen dat er in de praktijk prikaccidenten optreden bij ander personeel dan op basis van de arbobeleidsregel en RIE als risicolopend was aangemerkt.
Voorbeelden van beroepen waarbij sprake kan zijn van een verhoogd risico op besmetting met hepatitis B zijn:
- politieagenten die in contact kunnen komen met agressie en hulp bieden bij ongevallen;
- medewerkers van brandweer of defensie die hulp bieden bij ongevallen;
- werknemers in de vuilnisbranche;
- werknemers in de uitvaartbranche;
- werknemers in penitentiaire inrichtingen;
- personeel in opvangcentra voor asielzoekers;
- prostituees;
- langdurig verblijf (al dan niet beroepsmatig) in middel- of hoogendemische gebieden (zie Hepatitis B yellow book 2024, CDC);
- personen die via een verwonding zijn blootgesteld aan bloed van een persoon met hepatitis B of waarvan besmetting onbekend is;
- familieleden en huisgenoten van hepatitis B-dragers (niet beroepsmatig maar via GGD);
- overige die op basis van een RIE mogelijk verhoogd risico op een besmetting lopen.
Bijlage 2. Wettelijke kaders
De wettelijke regelgeving omtrent bescherming van werknemers aan beroepsmatige risico’s is vastgelegd in het arbeidsomstandighedenbesluit hoofdstuk 4.
De werkgever moet bijhouden welke werknemers er, conform de uitkomst van de RIE, een verhoogd risico lopen om in aanraking te komen met, mogelijk met hepatitis B besmet, bloed. Verder moet de werkgever bijhouden of deze werknemers beschermd zijn tegen hepatitis B. Daarnaast moet de werkgever ook een prikaccidentenprotocol hebben waarin duidelijk wordt omschreven wie wat moet doen na een prikaccident en wie waar verantwoordelijk is. Onder prikaccidenten worden ook snij- of bijtwonden verstaan (zie de LCI-richtlijn Prikaccidenten).
Alle accidenten moeten, ongeacht de ernst van het accident en ongeacht de vaccinatietoestand van de verwonde, conform het prikaccidentenprotocol gemeld worden aan de bedrijfsarts of medisch beoordelaar. Behalve hepatitis B zijn er immers ook andere aandoeningen waartegen mogelijk maatregelen genomen moeten worden (en waarvoor de werkgever ook verantwoordelijk is). Het verdient aanbeveling om alle accidentele bloedcontacten, ook daar waar niet tot handelen wordt overgegaan, met overwegingen van de keuze, te registreren. Bij het optreden hepatitis B en/of andere bloedoverdraagbare aandoeningen samenhangend met het accident is er sprake van een beroepsziekte. Beroepsgebonden aandoeningen dienen door een bedrijfsarts gemeld te worden bij het Nederlands Centrum voor Beroepsziekten (NCvB).
Een essentieel onderdeel van een prikaccidentenprotocol is centrale registratie. De registratie is een middel om te controleren aan welke risico’s werknemers worden blootgesteld en of de preventieve maatregelen effectief zijn. Wanneer een dekkende prikaccidentenregistratie wordt bijgehouden is het mogelijk dat blijkt dat er werknemers in bepaalde functies zijn die niet als risicolopers werden bestempeld maar toch met enige regelmaat een prikaccident oplopen. Een onderzoek op de werkplek zal uitwijzen of hier extra voorzorgsmaatregelen genomen moeten en kunnen worden. Eventueel wordt hierbij een extra risicoloper functie geïdentificeerd die voor vaccinatie in aanmerking komt.
Bijlage 3. Vragenlijst hepatitis B-vaccinatie
Via deze link downloadt u automatisch de 'Vragenlijst hepatitis B-vaccinatie'.
Bijlage 4. Bevoegdheden volgens de wet BIG
De wet BIG is een kwaliteitswet die zich richt op individuele beroepsbeoefenaars. In de wet zijn de bevoegdheden voor medisch handelen en de regeling betreffende voorbehouden handelingen vastgelegd. Voorbehouden handelingen (artikel 36 wet BIG) zijn handelingen die risico’s voor de gezondheid van de patiënt met zich mee kunnen brengen en hieronder vallen o.a. injecties en venapuncties.
De wet is te vinden op de website Wettenbank van de overheid.
De bevoegdheidsregeling voorbehouden handelingen heeft betrekking op alle beroepsbeoefenaren in de individuele gezondheidszorg. De regeling voorbehouden handelingen kent drie categorieën bevoegdheden:
- bevoegd tot de indicatiestelling van de voorbehouden handeling en de uitvoering hiervan, de arts of artikel 36-bevoegde volgens de wet BIG;
- bevoegd tot het functioneel zelfstandig verrichten van de voorbehouden handeling in opdracht van de eerstgenoemde bevoegde arts (verpleegkundige);
- bevoegd tot het verrichten van de handeling in opdracht, onder toezicht en met aanwijzing van de eerstgenoemde bevoegde (analist, overigen) (niet-zelfstandig bevoegde, artikel 35).
Een BIG-geregistreerde arts is bevoegd tot het verrichten van medische handelingen. Voor het daadwerkelijk uitvoeren van deze handelingen dient een beroepsbeoefenaar bevoegd én bekwaam te zijn. Een verpleegkundige is bevoegd tot zelfstandig verrichten van handelingen in opdracht van de eerstgenoemde.
Niet-zelfstandig-bevoegden mogen voorbehouden handelingen verrichten mits:
- hij/zij hiertoe opdracht heeft gekregen van een bevoegd persoon;
- hij/zij beschikt over bekwaamheid;
- hij/zij zich houdt aan de aanwijzingen van de bevoegde opdrachtgever.
Betreffende de aanwezigheid van een arts: in het rapport ‘Aanwezigheid arts op een reizigersvaccinatiebureau’ (2006) wordt aanbevolen dat voor elke specifieke situatie waarin wordt gevaccineerd, beoordeeld moet worden of het verantwoord is dat er gevaccineerd wordt zonder de aanwezigheid van een arts.
Bijlage 5. Vaccinatieschema, bloedafname en vervolgstappen bij onvoldoende anti-HBs respons
Stroomschema 1
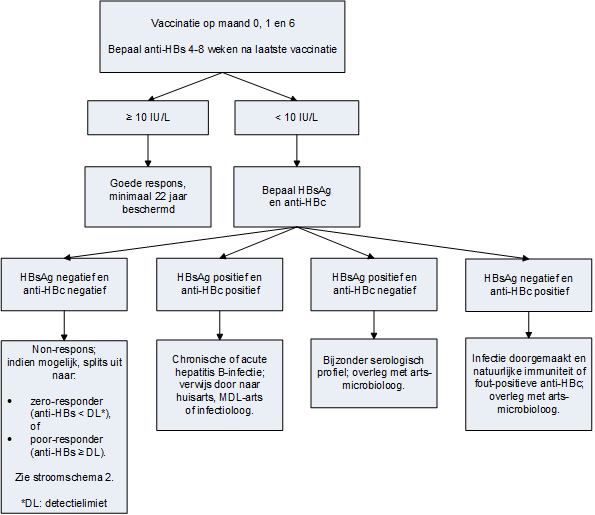
Stroomschema 2: zero- en poor-responders
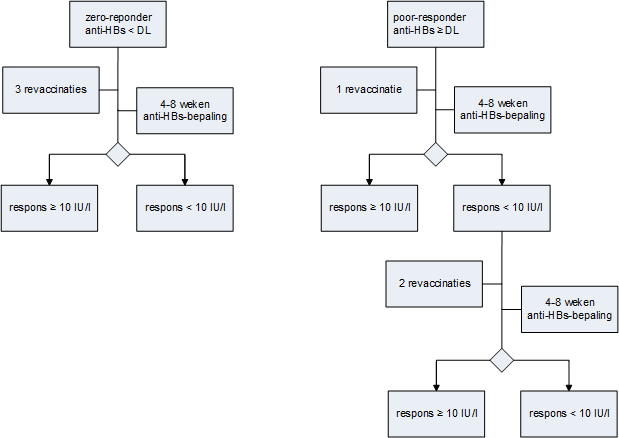
DL: Detectielimiet
Bijlage 6. Bijwerkingen vaccinatie hepatitis B
Bijwerkingen zijn arbitrair in twee groepen te verdelen:
1. Veel voorkomende, niet ernstige bijwerkingen:
- lokaal:
pijnlijkheid, roodheid en zwelling rondom de injectieplaats; - systemisch:
hoofdpijn, moeheid en koorts gedurende 24 tot 48 uur na de injectie; vasovagale collaps.
2. Zeldzame, ernstige bijwerkingen:
- anafylaxie:
shock, oedeem en zwelling van de mond, tong en larynx, status astmaticus, urticaria optredend binnen enkele minuten tot 1 uur na toediening van het vaccin; - Hyperimmunisatie (nooit gerapporteerd na hepatitis B):
heftige lokale reacties, vaak met algemene verschijnselen zoals koorts en exantheem bij personen met zeer hoge antistoftiters ten gevolge van voorafgaande vaccinaties.
3. Hoe te handelen bij bijwerkingen:
Hieronder volgen enkele algemene adviezen over de handelswijze in geval van bijwerkingen. Wat ter plekke de beste handelswijze is in geval van ernstige bijwerkingen, hangt onder andere af van de setting waarin gevaccineerd wordt en de protocollen van de plaatselijke ambulancedienst of het ziekenhuis waarin eventuele vervolgopvang plaatsvindt. Vandaar dat wordt aanbevolen in overleg lokaal een eigen protocol op te stellen.
Collaberen tijdens of vlak na vaccinatie zal meestal een vasovagale reactie zijn (flauwte). De kans op optreden van een anafylactische shock is erg klein. Verschil tussen beide toestanden bij lichamelijk onderzoek is:
- anafylactische shock: warme, rode huid, toenemende snelle pols;
- flauwte: koude, bleke huid, langzame pols.
3.1 Algemene voorzorgsmaatregelen:
- Wees ervan overtuigd dat de benodigde medicatie altijd en op een vaste plaats aanwezig is.
- Controleer regelmatig de uiterste vervaldatum van de medicamenten en leg het vast in een logboek.
- Laat de cliënt tijdens de vaccinatie altijd zitten of liggen.
- Zorg ervoor tijdens het vaccineren altijd vóór de cliënt te staan.
- Laat een cliënt die onwel wordt nooit alleen.
- Waarschuw iemand (of laat waarschuwen) die hulp kan verlenen (aanwezigheid van telefoon).
- Zorg dat er altijd een tweede medewerker in de buurt is.
3.2 Vasovagale collaps (flauwvallen)
Deze kan voor de betrokkenen zelf ook onverwachts optreden.
Symptomen:
- patiënt is bleek en voelt koud aan;
- langzame pols;
- hypotensie;
- duizeligheid, zwarte vlekken voor de ogen;
- misselijkheid en braakneigingen;
- incidenteel spiertrekkingen of incontinentie bij vasovagale collaps.
Maatregelen bij vasovagale collaps:
- plat neerleggen met de benen omhoog of hoofd tussen de benen;
- niet te snel op laten staan.
3.3 Wees alert op een ernstige bijwerking / maak een differentiaal diagnose vaatcollaps:
- anafylactische shock;
- myocardinfarct/ritmestoornissen;
- epileptisch insult.
3.4 Maatregelen bij vermoeden op in punt 3.3 genoemde ernstige bijwerkingen:
- patiënt neerleggen, of anderszins ervoor zorgen dat de persoon zich niet kan bezeren;
- ademhalingswegen vrij maken (Mayo-tube);
- ambulance laten bellen (tel: 1-1-2);
- tensiemeterband om de arm doen;
- regelmatig pols en tensie meten, de gegevens vastleggen op een lijst;
- bij systematische reacties zo nodig medicatie instellen.
4. Anafylactische shock:
Direct na het contact met het antigeen wordt de patiënt veelal angstig, soms geagiteerd.
4.1 Symptomen:
- jeukend gevoel in de mond, met name verhemelte en tong, later gehele lichaam;
- misselijkheid, diarree en/of braken;
- urticaria;
- soms zwelling van neusslijmvlies;
- de huid wordt rood, de patiënt rillerig en klam en gedesoriënteerd;
- de pols is snel en week;
- de tensie daalt in de loop van een paar minuten. In deze periode komen hartritmestoornissen voor en soms een zeer uitgesproken bronchusobstructie of larynxoedeem.
4.2 Medicatie bij anafylactische shock (zie tabel):
- Geef adrenaline intramusculair (1:1000) 1 mg/ml, doseringsschema 0,5 mg (=0,5 ml) Bel (intussen) een ambulance met A1-indicatie (tel 1-1-2)
- Bij onvoldoende verbetering of verergering van de symptomen herhaal toedoening van 0,5 ml na van 5 tot 15 minuten .
- Gebruik een injectiespuit met een nauwkeurige maatverdeling van 0,05 ml (1 ml spuitje). Verdunnen met NaCl 0,9% is dan niet nodig.
| Geneesmiddel | Dosering | Werkingssnelheid/-duur |
|---|---|---|
| Adrenaline Injectievloeistof 1 mg/ml; ampul 1 ml |
Volwassene en kind ≥ 12 jaar:
|
na 3-5 minuten |
Bron: Anafylaxie en acuut angio-oedeem - Het Acute Boekje.
Bijlage 7. Lijst van afkortingen
| Anti-HBc | antistoffen tegen het hepatitis B-core antigeen |
| Anti-HBs | antistoffen tegen het hepatitis B-surface antigeen |
| BOA | Bloedoverdraagbare aandoeningen |
| Elisa | Enzyme linked immuno sorbent assay |
| HBIg | Hepatitis B-Immunoglobuline |
| HBsA | Hepatitis B-surface antigeen |
| HBV | Hepatitis B-virus |
| IU/L | international units per liter (= IE/L; internationale eenheden per liter) |
| LCI | Landelijke Coördinatie Infectieziektebestrijding |
| RIE | Risico- Evaluatie en -Inventarisatie |
| Wet BIG | Wet op de Beroepen in de Individuele Gezondheidszorg |
Bijlage 8. Samenstelling van de werkgroep
- Dr. G.J. Boland, klinisch microbioloog, afdeling Medische Microbiologie, UMC Utrecht
- Drs. R.J. Naber, bedrijfsarts, Livio (tot 1/9/2015), bedrijfsarts AMC (vanaf 1/9/2015)
- Dr. H. Ruijs, arts infectieziektebestrijding, CIb, RIVM
- Dr. P.M. Schneeberger, arts-microbioloog, Regionaal Laboratorium Medische Microbiologie, Jeroen Bosch Ziekenhuis, ’s-Hertogenbosch
- Dr. J. E. Steenbergen, CIb, RIVM
- Prof. Dr. H.L. Zaaijer, Sanquin en Universiteit van Amsterdam
Bijstelling vaccinatieschema en update n.a.v. Hepatitis B non-responders 2024: dr. S.H.M.A. Wijffels-de Groot, bedrijfsarts in opleiding, CIb, RIVM.
Bronnen en verwijzingen
- Landelijke richtlijn preventie transmissie van hepatitis B van medisch personeel naar patiënten: 3e editie: vastgesteld op 10 september 2012. Commissie preventie iatrogene transmissie van HBV, HCV en HIV. Link
- LCI-richtlijn hepatitis B. Link
- Rapport gezondheidsraad Werknemers en infectieziekten: criteria voor vaccinatie. Link
- Richtlijn 2010/32/EU van de raad van 10 mei 2010 tot uitvoering van de door HOSPEEM en EPSU gesloten kaderovereenkomst inzake de preventie van scherpe letsels in de ziekenhuis- en gezondheidszorgbranche. Link
- Isken, LD et al. 2009. Revaccinatie tegen hepatitis B niet nodig, ook niet bij personen die door hun werk een verhoogd risico lopen. Ned Tijdschr Geneeskd 2009; 153: A415. Link
- European Consensus Group on Hepatitis B immunity 2000. Are booster immunisations needed for lifelong hepatitis B immunity? Lancet 2000 Feb 12; 355 (9203): 561-5. https://doi.org/10.1016/S0140-6736(99)07239-6
- Gezondheidsraad, 4 maart 2002. Briefadvies Hepatitis B vaccinatie. Link
- FitzSimons D et al. 2013. Hepatitis B vaccination: a completed schedule enough to control HBV lifelong? Milan, Italy, 17-18 November 2011. Vaccine 2013 Jan 11; 31 (4): 584-90. doi: 10.1016/j.vaccine.2012.10.101. Epub 2012 Nov 8. Hepatitis B vaccination: A completed schedule enough to control HBV lifelong?: Milan, Italy, 17–18 November 2011 - ScienceDirect
- Hoebe CJ et al. 2012. Revaccination with Fendrix® or HBVaxPro® results in better response rates than does revaccination with three doses of Engerix-B® in previous non-responders. Vaccine 2012 Nov 6; 30 (48): 6734-7. doi: 10.1016/j.vaccine.2012.08.074. Epub 2012 Sep 11. Revaccination with Fendrix® or HBVaxPro® results in better response rates than does revaccination with three doses of Engerix-B® in previous non-responders - ScienceDirect
- Bruce MG et al. 2016. Antibody levels and protection after hepatitis B vaccine: results of a 30-year follow-up study and response to a booster dose. J Infect Dis 2016 Jul 1; 214 (1): 16-22. doi: 10.1093/infdis/jiv748. Epub 2016 Jan 21. Antibody Levels and Protection After Hepatitis B Vaccine: Results of a 30-Year Follow-up Study and Response to a Booster Dose | The Journal of Infectious Diseases | Oxford Academic (oup.com)
- Roukens AH & Visser LG 2011. Hepatitis B vaccination strategy in vaccine low and nonresponders: a matter of quantity of quality? Hum Vaccin 2011 Jun; 7 (6): 654-7. doi: 10.4161/hv.7.6.14986. Epub 2011 Jun 1. Link
- Landelijke richtlijn prikaccidenten. Link
Versiebeheer
- Juni 2024: tekst revaccinatieschema is aangepast aan de hand van nieuwe richtlijn Hepatitis B non-responders. Bij 'Bijwerkingen, contra-indicaties, interacties' is informatie over zwangerschap toegevoegd. Omgezet van pdf naar html.
- Juni 2019: verouderde hyperlinks zijn aangepast.
- Maart 2016: eerste versie vastgesteld.