Bijlage bij het LCI-draaiboek Hepatitis B-vaccinatieprogramma risicogroepen
Deze richtlijn is, als bijlage van het LCI-draaiboek Hepatitis B-vaccinatieprogramma risicogroepen, in 2012 opgesteld door de LCI in afstemming met de Nederlandse Vereniging voor Hiv Behandelaren (NVHB). In 2024 is de richtlijn herzien door een werkgroep, bestaande uit de internist-infectiologen L. Smid, dr. W.F.W. Bierman, dr. A.H.E. Roukens en dr. T.E.M.S. de Vries-Sluijs. De richtlijn is geautoriseerd door het (Landelijk Overleg Infectieziektebestrijding) en de NVHB. De LCI heeft de richtlijn geredigeerd en gepubliceerd op haar website. In 2025 heeft een update plaatsgevonden in verband met het programmatisch beschikbaar worden van gecombineerd een hepatitis A/B-vaccin (Twinrix Adult; ‘Twinrix’). Deze tekst is in mei 2025 geautoriseerd door de NVHB en in januari 2026 vastgesteld door het (Landelijk Overleg Infectieziektebestrijding-Seksuele Gezondheid).
De richtlijn wordt periodiek herzien. Uiterlijk in 2031 bepaalt de LCI in afstemming met de NVHB of de richtlijn nog actueel is. Zo nodig wordt het herzieningstraject eerder opgestart, als nieuwe ontwikkelingen daartoe aanleiding geven.
1. Inleiding
Het doel van het (hepatitis B-virus)-programma is om de overdracht van hepatitis B onder risicogroepen te verminderen via hepatitis B-vaccinatie. Het tweede doel is het opsporen van personen met chronische hepatitis B. Personen met hiv worden gevaccineerd in het hivbehandelcentrum of bij de (Gemeentelijke gezondheidsdienst). Het vaccinatieschema voor personen met hiv die binnen de risicogroepen van het HBV-vaccinatieprogramma vallen – mannen die seks hebben met mannen (MSM*) en sekswerkers – wijkt niet af van het reguliere vaccinatieschema. Het startmoment van de hepatitis B-vaccinatie, de hoeveelheid vaccin, de uitvoerende organisatie en de noodzaak tot titerbepaling wijken echter af van de binnen het programma gebruikelijke routine. Uit literatuurstudies blijkt namelijk dat de immuunrespons van personen met hiv tegen hepatitis B volgens het standaard schema suboptimaal is met een enkele dosis vaccin, variërend van 34 tot 89% (20 µg HBsAg op maand 0, 1 en 6) (Mena 2015). Daarnaast blijkt het resultaat van de vaccinatie afhankelijk te zijn van het aantal CD4-cellen en de hoogte van de viral load.
Vanaf 2 juni 2025 komen (mannen die seks hebben met mannen) en MSM-sekswerkers (met of zonder hiv) binnen het Vaccinatieprogramma hepatitis B-risicogroepen in aanmerking voor een gratis gecombineerd hepatitis A/B-vaccin (Twinrix Adult; vanaf hier aangeduid als ‘Twinrix’). Bij MSM en MSM-sekswerkers die geen immuniteit hebben tegen hepatitis A en B vervangt Twinrix het hepatitis B-vaccin Engerix-B. Het doel van de opname van hepatitis A-vaccinatie in het programma is het voorkomen van hepatitis A-gerelateerde ziektelast onder de risicogroepen, waaronder ziekenhuisopnames, en het voorkomen van verdere verspreiding van hepatitis A. Daarmee nemen ook de uitbraak-gerelateerde werkdruk en kosten bij de GGD’en af.
* Waar MSM staat wordt de volgende doelgroep bedoeld: cisgender mannen die seks hebben met mannen en genderdiverse personen die seks hebben binnen MSM-netwerken. Deze doelgroep komt onder bepaalde voorwaarden in aanmerking voor een gratis hepatitis (A/)B-vaccinatie; voor meer informatie zie paragraaf 4.4 Geslacht in het draaiboek Hepatitis B-vaccinatieprogramma risicogroepen.
2. Beleid dubbele dosis hepatitis B-vaccinatie hivpositieve MSM en sekswerkers
2.1 Startmoment vaccinatie
Uit diverse studies blijkt dat voor een optimaal vaccinatieresultaat het aantal CD4-cellen medebepalend is voor het moment waarop met vaccineren tegen hepatitis B gestart dient te worden (Cornejo-Juárez 2006, Cruciani 2009, de Vries-Sluijs 2011, Fonseca 2005, Landrum 2009, Ungulkraiwit 2007, Veiga 2006). Tevens blijkt uit de literatuur dat de respons mede afhankelijk is van de viral load op het moment van vaccineren (Cruciani 2009, Fonseca 2005, Landrum 2009, Tedaldi 2004, Veiga 2006). Na start van combinatie antiretrovirale therapie (cART) stijgt het aantal CD4-cellen langzaam en daalt de viral load snel. Hieronder is in het kort weergegeven bij welke situatie een hepatitis B-vaccinatie overwogen kan worden.
CD4 ≥ 350 cellen/mm³
- Start hepatitis B-vaccinatieschema met dubbele dosis
CD4 < 350 cellen/mm³*
- Wacht bij voorkeur totdat virale load ondetecteerbaar is (< 50 kopieën/ml)
- Start vervolgens met een hepatitis B-vaccinatieschema met dubbele dosis
*NB: Als de persoon een hoog risico loopt op hepatitis B, kan de hivbehandelaar overwegen om toch te starten met vaccineren.
2.2 Dubbele dosis, vaccinkeuze en schema's
2.2.1 Dubbele dosis
Personen met hiv (MSM, sekswerkers en trans personen die onder de doelgroep MSM of sekswerker vallen; zie paragraaf 4.4 over geslacht in het LCI-draaiboek Hepatitis B-vaccinatieprogramma risicogroepen) worden binnen het Vaccinatieprogramma hepatitis B-risicogroepen gevaccineerd met een dubbele dosis hepatitis B-vaccin. Dit betekent dat ze per vaccinatiemoment twee injecties hepatitis B-vaccin of één gecombineerd hepatitis A/B-vaccin tegelijk met één hepatitis B-vaccin krijgen toegediend (zie paragraaf 2.2.2). Deze twee injecties worden bij voorkeur in twee verschillende spiergroepen gezet.
Een dubbele dosis recombinant hepatitis B-vaccin (Engerix-B of HBVaxPro) geeft een significant betere respons 4-6 weken na een primaire serie ten opzichte van een standaard dosis (OR 1.76, 95% BI 1.36-2.29) (Lee 2020). In een andere review en meta-analyse was de respons rate na een dubbele dosis 75,2% (95% BI 66,2%-82,5%) ten opzichte van 65,5% (95% BI 53,1%-76,1%) na een enkele dosis (Tian 2021). In beide meta-analyses zaten naast het reguliere schema ook studies met vier doses en andere driedosesschema’s.
Naar de duur van de bescherming van het hepatitis B-vaccin bij personen met hiv is momenteel nog onvoldoende onderzoek gedaan om hierover een uitspraak te kunnen doen (Farooq 2019). In de praktijk wordt een anti-HBs ≥ 10 IE/l aangehouden als maat voor langdurige bescherming en wordt geen follow-up van anti-HBs verricht.
2.2.2 Vaccinkeuze en schema
Binnen het programma worden Engerix-B 20 µg en sinds juni 2025 ook Twinrix vergoed. (De afgelopen jaren werd voor het HBV-programma in sommige perioden Engerix-B 20 µg en in andere perioden HBVaxPro 10 µg gebruikt. Dit was afhankelijk van beschikbaarheid en aanbestedingen. De vaccins HBVaxPro en Engerix-B zijn met elkaar uitwisselbaar. Dit betekent dat een vaccinatieschema dat gestart is met Engerix-B vervolgd kan worden met HBVaxPro en vice versa. Ook hebben beide vaccins dezelfde biologische effectiviteit.)
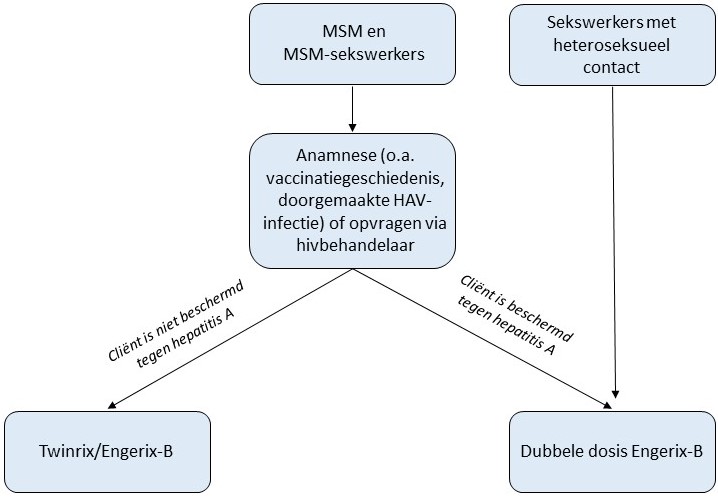
De doelgroepen MSM en MSM-sekswerkers komen in aanmerking voor een schema met drie doses Twinrix/Engerix-B op maand 0, 1 en 6. Geadviseerd wordt om tevoren de (hepatitis A-virus)-status uit te vragen: of iemand eerder (bijvoorbeeld reisgerelateerd) een hepatitis A-vaccinatie heeft gehad (bij voorkeur gedocumenteerd) of hepatitis A heeft doorgemaakt. Hiernaast kan de HAV status tevoren nagegaan worden bij de hivbehandelaar; deze is bij ruim meer dan de helft van de personen met hiv bekend (69% in 2023). Van de personen met een bekende HAV-status had 66% van de doelgroep MSM een positieve anti-HAV (immunoglobuline G) (SHM 2024). Indien er geen immuniteit tegen HAV aanwezig is, en ook indien de HAV-status niet bekend is, wordt geadviseerd het schema Twinrix/Engerix-B te volgen.
Sekswerkers met heteroseksuele contacten worden gevaccineerd met drie dubbele doses Engerix-B op maand 0, 1 en 6. Voor een overzicht van vaccinkeuze, zie het schema in figuur 1.
Figuur 1: Vaccinkeuze bij personen met hiv
Kwaliteit van bewijs
De effectiviteit van de combinatie Twinrix/Engerix-B is als primaire serie niet onderzocht bij personen met hiv. Een primaire serie met (mono) Twinrix heeft bij gezonde personen > 40 jaar een superieure immunogeniciteit ten opzichte van monovalente hepatitis B-vaccins (Van der Wielen 2006). In een RCT onder adolescenten met hiv hadden de studiearmen die gevaccineerd werden met (mono) Twinrix en dubbele dosis Engerix-B een overeenkomstige vaccinatierespons (respectievelijk 75,4% en 73,2%) (Flynn 2011). Daarom is het aannemelijk dat bij volwassen personen met hiv een combinatie Twinrix/Engerix-B tot een goede, en mogelijk superieure, respons leidt ten opzichte van een dubbele dosis recombinant hepatitis B-vaccin. Het gebruik van een dubbele dosis Twinrix voor verkrijgen van immuniteit tegen hepatitis B is niet onderzocht als primaire serie bij personen met hiv. Binnen het programma wordt toepassing van een dubbele dosis Twinrix als primaire serie bij personen met hiv daarom niet toegepast, ook omdat een dubbele dosis hepatitis A-vaccin niet noodzakelijk is voor bescherming tegen hepatitis A.
Gewenste en ongewenste effecten
Een schema met Twinrix kan mogelijk een betere vaccinatierespons geven (zie hierboven). De frequentie van gemelde bijwerkingen na toediening van Twinrix is niet verschillend van de frequentie van gemelde bijwerkingen na toediening van de monovalente vaccins in vergelijkende onderzoeken (EMA 2024).
Waarden en voorkeuren patiënt
Er zijn geen studies die dit onderwerp onderzocht hebben bij personen met hiv. Aannemelijk is dat het toedienen van combinatievaccins door patiënten wordt geprefereerd boven het afzonderlijk toedienen van afzonderlijke hepatitis A vaccins door de reductie van het aantal prikken.
Kosten(effectiviteit)
Beide vaccins worden vergoed binnen het (hepatitis B-virus)-programma, de inkoopprijs van Twinrix is hoger dan die van Engerix-B.
Aanvaardbaarheid, haalbaarheid, implementatie
Het combinatieschema is een voorzetting van bestaand beleid waarbij de hepatitis A-component voorheen op eigen kosten betaald moest worden. Er worden geen problemen verwacht in de aanvaardbaarheid, haalbaarheid en implementatie.
Versneld schema (bij uitzondering)
Bij personen met een CD4-aantal > 500/mm³ is er goede respons beschreven op een versneld vaccinatieschema (0, 1, 3 weken t.o.v. 0, 1, 6 maanden). Als er zorgen zijn over het nakomen van de vaccinatieafspraken is voor personen met een CD4-aantal > 500/mm³ een versneld schema te overwegen. Zie voor meer informatie de NVHB-richtlijnen Hepatitis A en B. In de praktijk is dit alleen van toepassing bij een contra-indicatie voor een combinatie van hivbehandeling zonder tenofovirdisoproxil of tenofoviralafenamide (TDF of TAF). Geadviseerd wordt om een eventueel versneld schema te bespreken met de hivbehandelaar.
Overgangsfase na beschikbaar komen van Twinrix
Tijdens de overgangsfase kan het zijn dat personen met hiv al een of twee dubbele doses Engerix-B ontvangen hebben als Twinrix via het programma beschikbaar komt. Ook voor personen met hiv is het mogelijk om al over te gaan naar Twinrix na een of twee dubbele doses Engerix-B.
Er zijn te weinig onderzoeksdata om te kunnen zeggen of bij volwassen personen met hiv met een of twee doses Twinrix ook adequate seroprotectie tegen hepatitis A kan worden opgebouwd, zoals bij personen zonder hiv (≥ 90%) (Bakker 2016). Gemelde percentages zijn 40,5% na een of twee doses bij 101 personen met hiv (Jimenez 2013) en 50% (6/12) na één dosis (Schnyder 2025). Na een volledige serie van drie doses was dat respectievelijk 53% en 100%. Dit percentage wordt vooral beïnvloed door verschillen in het CD4-getal in beide cohorten.
Vervolgvaccinaties tegen hepatitis A zijn dus nodig bij de meerderheid van de personen met hiv nadat er slechts een of twee doses Twinrix zijn gegeven, omdat minimaal drie doses Twinrix nodig zijn om adequate en langdurige bescherming tegen hepatitis A te verkrijgen bij personen met hiv. Het advies is om de hepatitis A-serie af te maken via de hivbehandelaar. Dit kan via onderstaande routes:
- Bij verkregen bescherming tegen hepatitis B: afzonderlijke hepatitis A-vaccinaties via de hivbehandelaar (op eigen kosten; zie onderstaand onder Indicaties).
- Bij non-respons op hepatitis B-vaccinatie: via het revaccinatieschema dat Twinrix bevat. (Dit valt binnen het programma.)
De hepatitis A-vaccinaties verlopen tijdens een overgangsfase niet volgens het reguliere schema (0, 1 en 6 maanden). Geadviseerd wordt om individueel beleid te laten bepalen door hivbehandelaren met betrekking tot het bepalen van (hepatitis A-virus)-serologie (zie paragraaf 2.4).
Chronische hepatitis B en doorgemaakte hepatitis B – hepatitis A-vaccinatie
Alle personen met hiv (onafhankelijk van doelgroep) met een chronische hepatitis B hebben in verband met de chronische leveraandoening een indicatie voor hepatitis A-vaccinatie (dit wordt vergoed). Dit valt buiten het programma en deze hepatitis A-vaccinatie wordt uitgevoerd via de hivbehandelaar.
Personen met hiv van wie uit de screening later blijkt dat zij hepatitis B al hebben doorgemaakt én die wel een indicatie hebben voor hepatitis A-vaccinatie (zie onderstaand onder Indicaties) worden geadviseerd om, na de reeds toegediende eerste dosis Twinrix/Engerix-B tijdens het eerste screenings/vaccinatieconsult, de hepatitis A-vaccinatieserie af te maken via de hivbehandelaar. Dit valt buiten het programma.
Indicaties
- Bij het bestaan van een chronische leverziekte. Dit wordt vergoed.
- De NVHB adviseert om vaccinatie tegen hepatitis A te overwegen bij (mannen die seks hebben met mannen) zonder antistoffen tegen hepatitis A. Afzonderlijke hepatitis A-vaccins worden echter niet vergoed door de basisverzekering (zie NVHB-richtlijnen Hepatitis A en B).
2.3 Uitvoering vaccinatie
De indicatiestelling van hepatitis B-vaccinatie kan gedaan worden door zowel de hivbehandelaar als door de zorgverlener van de (Gemeentelijke gezondheidsdienst) (oftewel: de arts seksuele gezondheid van de GGD óf een verpleegkundige die onder supervisie van deze arts werkt). Indien het CD4-getal onbekend is bij de GGD, verwijst de zorgverlener van de GGD voor vaccinatie naar de hivbehandelaar. Afhankelijk van regionale afspraken tussen hivbehandelaren en GGD kan de hivbehandelaar zelf het hepatitis B-vaccin (of gecombineerd hepatitis A/B-vaccin) geven (in geval van samenwerking als regionaal partner met de GGD) OF de persoon met hiv doorverwijzen naar de GGD voor vaccinatie.
2.4 Titerbepaling
Vanwege de mogelijke lage respons op hepatitis B-vaccinatie is het belangrijk dat personen met hiv 4 tot 8 weken na de derde dubbele dosis een titerbepaling laten doen (anti-HBs). Het advies voor post-vaccinatie-titerbepaling wordt gegeven door degene die vaccineert. De uitvoering van de anti-HBs-bepaling kan gedaan worden door zowel de GGD als het hivbehandelcentrum. Een titerbepaling wordt niet vergoed door het Vaccinatieprogramma hepatitis B-risicogroepen.
Vaccinatie tegen hepatitis A bij personen met hiv is onderzocht in retrospectieve analyses, met een seroconversie van 53%-80% na een volledige serie (Fritzsche 2019, Jimenez 2013). In een prospectieve studie bij personen met hiv met virale suppressie en adequate CD4-getallen is de seroconversie hoger: 97% (Schnyder 2025). Vanwege een mogelijke lage respons wordt HAV-serologie na vaccinatie geadviseerd bij personen met hiv met een CD4-getal < 500 cellen/mm³. Dit verloopt via de hivbehandelaar en valt buiten het programma. Aanvragen HAV-serologie is daarnaast (logistiek) niet mogelijk via de GGD.
2.5 Non-responders
2.5.1 Hepatitis B
Indien een persoon met hiv het vaccinatieschema voltooid heeft en de anti-HBs titer onder de 10 IE/l is, wordt de persoon beschouwd als non-responder en komt deze in aanmerking voor revaccinatie (vergoed door het Vaccinatieprogramma hepatitis B-risicogroepen).
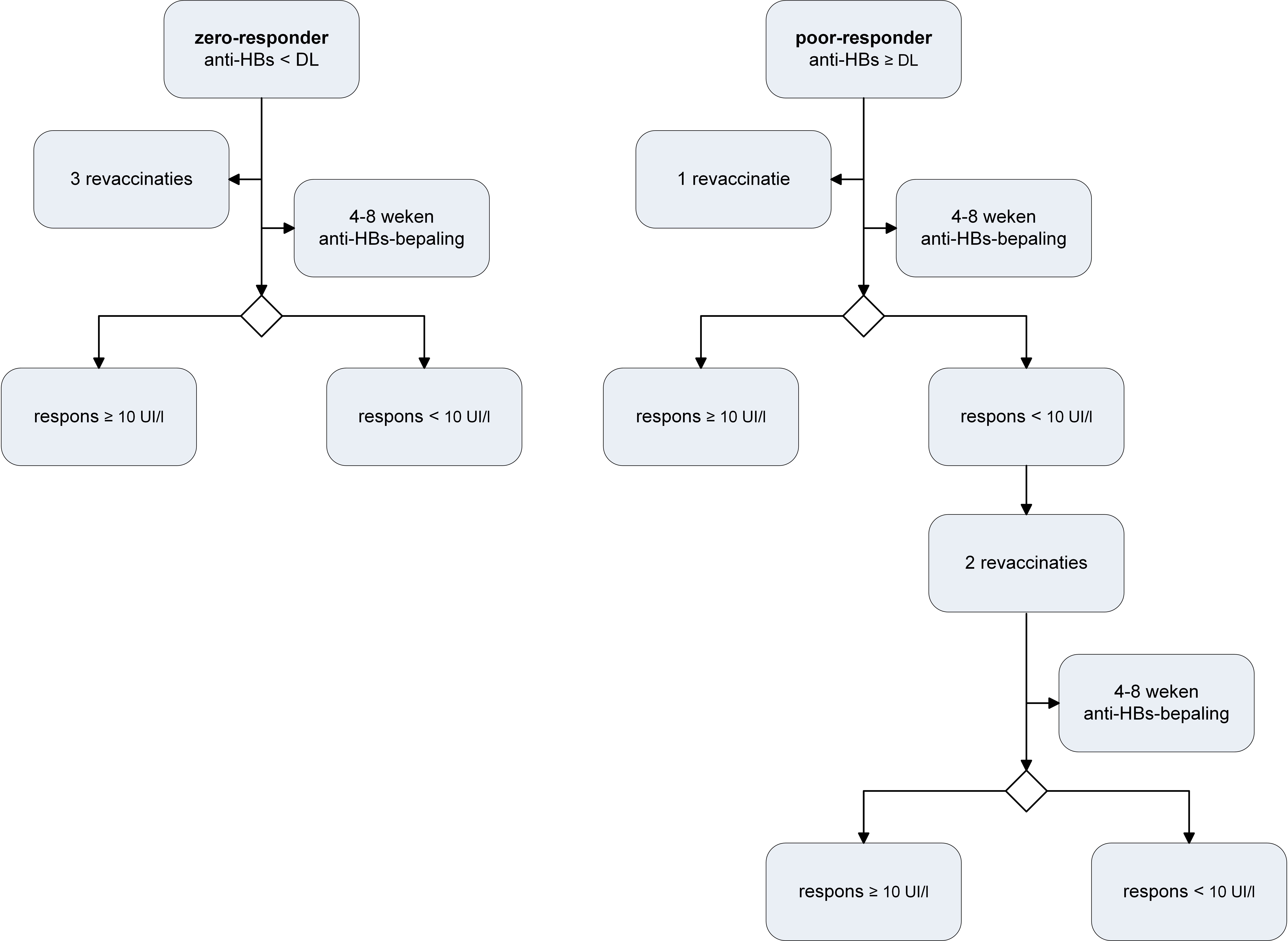
Bij een non-respons wordt ook voor personen met hiv geadviseerd het beleid te volgen conform de bijlage Hepatitis B non-responders. Hierbij wordt aanbevolen de anti-HBs-titer te kwantificeren om een onderscheid te maken tussen een poor-responder en zero-responder. Afhankelijk van de hoeveelheid anti-HBs kan gekozen worden voor een aangepast revaccinatieschema en kan de werkwijze potentieel dosisbesparend zijn (zie de stroomschema’s in figuur 2).
Voor personen met hiv wordt geadviseerd te revaccineren met een dubbele dosis hepatitis B-vaccin middels Twinrix/Engerix-B (zowel na een serie dubbele dosis Engerix-B als na Twinrix/Engerix-B).
Door de hivbehandelaar kan ook overwogen worden om bij non-responders met andere immunogene hepatitis B-vaccins te revaccineren (Fendrix, HBVaxPro, Heplisav B). Deze vaccins worden echter niet vergoed uit het programma.
Indien hierna sprake is van een persisterende non-respons, kan overwogen worden om verder te vaccineren, bijvoorbeeld met Twinrix, Fendrix, HBVaxPro of Heplisav B (zie Overwegingen). Vaccinatie van persisterende non-responders wordt echter niet vergoed vanuit het Vaccinatieprogramma hepatitis B-risicogroepen. Een andere optie is een TDF of TAF bevattend (combinatie antiretrovirale therapie)-regime te handhaven als hivbehandeling aangezien dit bescherming biedt tegen infectie met (hepatitis B-virus) (Heuft 2014).
Figuur 2: Beleid voor non-responders uitgesplitst naar zero-responders (links) en poor-responders (rechts)
DL: detectielimiet (van de betreffende anti-HBs-test)
Voor personen met hiv geldt voor elke revaccinatie een dubbele dosis bestaande uit Twinrix/Engerix-B. Indien de titerhoogte onder de 10 IU/l niet bekend is, dient het revaccinatieschema van de zero-responder gevolgd te worden.
Kwaliteit van bewijs
De effectiviteit van de combinatie Twinrix/Engerix-B of dubbele dosis Twinrix is niet onderzocht bij personen met hiv die non-responder zijn. Het is aannemelijk dat Twinrix/Engerix-B een betere respons geeft ten opzichte van een dubbele dosis Engerix-B. Eén dosis Twinrix bleek immunogener dan één dosis Engerix-B 20 µg bij gezonde individuen die non-responder zijn (Raven 2020). Revaccinatie met een dubbele dosis Twinrix geeft bij gezonde individuen die non-responder zijn ook een goede respons (95%). Omdat dit echter niet werd vergeleken met een ander schema bij non-responders is niet duidelijk hoe groot de winst hiervan is (Cardell 2008). Het is niet goed te voorspellen óf en wat de eventuele meerwaarde is van een dubbele dosis Twinrix ten opzichte van een Twinrix/Engerix-B-revaccinatieschema bij personen met hiv die non-responder zijn.
Er zijn ook data over hepatitis B-vaccins die niet via het programma worden aangeboden. Revaccinatie van non-responders met Fendrix heeft een hoog slagingspercentage, onafhankelijk van het CD4-getal (81%, 95% BI 72-88%) (Machiels 2019). Fendrix heeft een significant hogere response rate ten opzichte van drie dubbele dosis Engerix-B (respectievelijk 86% en 65%) (de Vries-Sluijs 2020). Zowel twee als drie doses Heplisav B geven een superieure seroprotectie ten opzichte van drie enkele doses Engerix-B in personen met hiv die non-responder zijn (respectievelijk 93 en 99% t.o.v. 81%) (Marks 2025). In een kleine prospectieve studie hadden 19/26 non-responders seroconversie na 1-3 boosters HBVvaxPro 40 mcg (Cruciani 2009).
Gewenste en ongewenste effecten
Een revaccinatieschema dat Twinrix bevat is immunogener ten opzichte van een enkele dosis hepatitis B-revaccinatie. De meerwaarde van een dubbele dosis Twinrix is niet te voorspellen (zie hierboven). De frequentie van gemelde bijwerkingen na toediening van (enkele dosis) Twinrix is niet verschillend van de frequentie van gemelde bijwerkingen na toediening van de monovalente vaccins in vergelijkende onderzoeken (EMA 2024).
Waarden en voorkeuren patiënt
Er zijn geen studies die dit onderwerp onderzocht hebben bij personen met hiv.
Kosten(effectiviteit)
De kosteneffectiviteit van diverse nonresponsschema’s is niet bekend. Twinrix en Engerix-B worden beide vergoed binnen het programma. De inkoopprijs van Twinrix is hoger dan die van Engerix-B. Andere immunogene vaccins (Fendrix, HBVaxPro, Heplisav B) worden niet vergoed binnen het programma.
Aanvaardbaarheid, haalbaarheid, implementatie
Verwacht wordt dat het veld het aanvaardbaar vindt om te starten met een immunogener combinatieschema van Twinrix/Engerix-B bij non-responders en de respons eerst te evalueren, en niet direct over te gaan naar een dubbele dosis Twinrix. Er worden geen problemen verwacht ten aanzien van de haalbaarheid en implementatie.
2.5.2 Hepatitis A
Er kan individueel beleid zijn door hivbehandelaren met betrekking tot hepatitis A-revaccinatie in geval van non-respons op hepatitis A-vaccinatie. Dat valt buiten het Vaccinatieprogramma hepatitis B-risicogroepen. Er is geen mogelijkheid binnen het programma om afzonderlijke hepatitis A-vaccins te gebruiken bij hepatitis A-non-responders. Deze vaccins worden niet vergoed vanuit het programma.
3. Praktische uitvoering
3.1 Bekend hivpositief, hepatitis B-status onbekend
Als een (hepatitis B-virus)-vaccinatie-indicatie wordt gesteld, is hepatitis B-serologie (anti-HBc, indien positief aanvullend HBsAg) vooraf nodig om een actieve of doorgemaakte infectie uit te sluiten. Hiernaast dient de (hepatitis A-virus) status te worden nagaan (zie paragraaf 2.2.2). Op de (Gemeentelijke gezondheidsdienst)-locatie wordt wegens logistieke redenen de bloedafname voor hepatitis B-screening en toediening van de vaccinatie tijdens hetzelfde eerste consult uitgevoerd.
Uitvoering: personen met hiv, nooit hepatitis B-vaccinatieserie gehad of HBV-vaccinatiestatus onbekend (figuur 3)
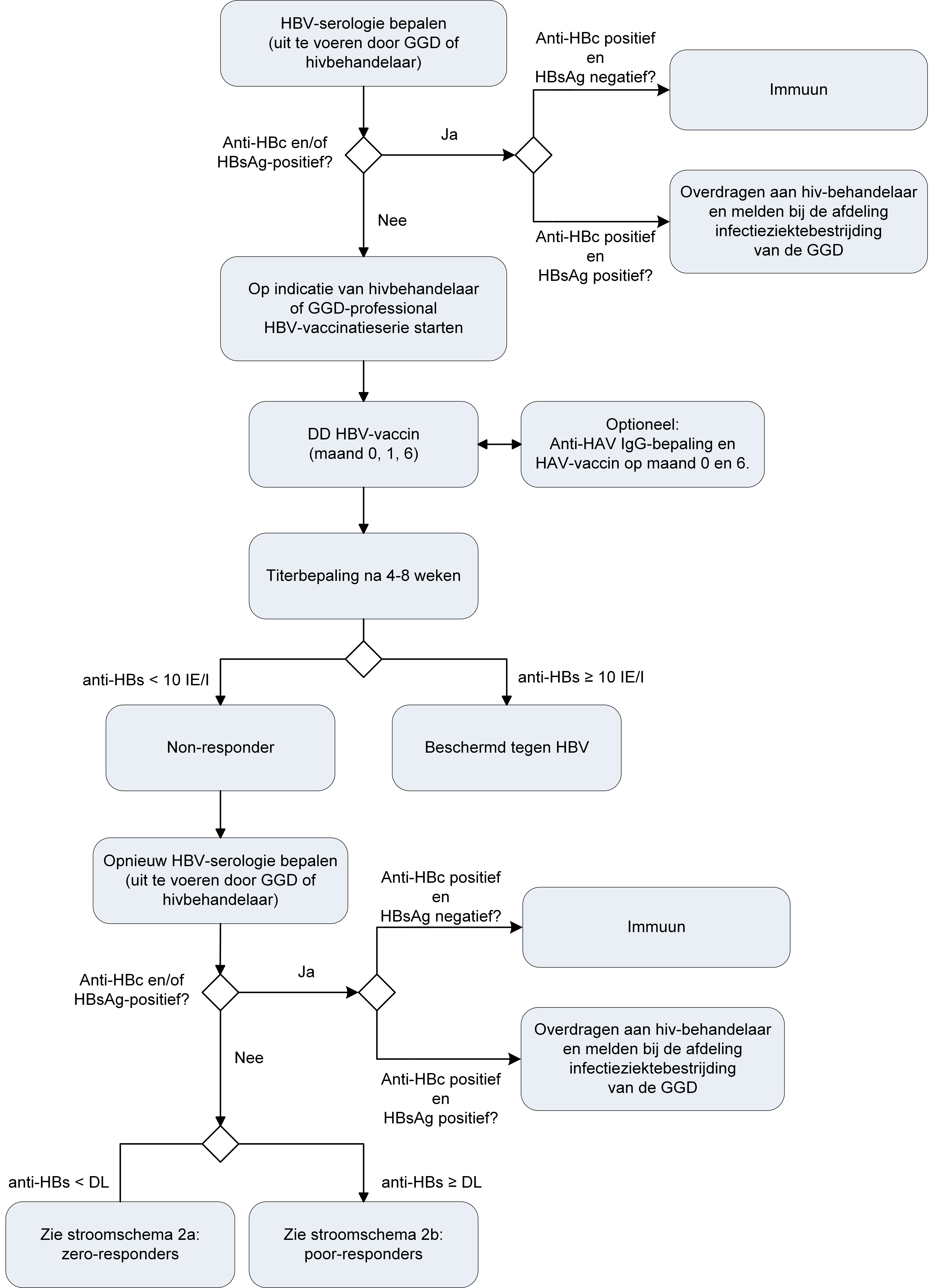
- Twinrix/Engerix-B of dubbele dosis Engerix-B (zie paragraaf 2.2.2 voor vaccinkeuze) op maanden 0, 1, 6. Titerbepaling 4-8 weken na 3e dubbele dosis.
- Anti-HBs ≥ 10 IE/l: cliënt is beschermd.
- Anti-HBs < 10 IE/l: er is sprake van een ‘non-respons’. Bepaal anti-HBc en HBsAg (cliënt kan tussen de vaccinaties in geïnfecteerd zijn).
- Anti-HBc en/of HBsAg positief:
- Anti-HBc positief en HBsAg negatief: cliënt is immuun.
- Anti-HBc positief en HBsAg positief: cliënt overdragen aan hivbehandelaar en melden bij de afdeling infectieziektebestrijding van de GGD.
- Anti-HBc en HBsAg negatief: ga na of de titer gekwantificeerd is (als de titer niet gekwantificeerd is, volg dan het beleid van zero-respons).
- Titer < detectiegrens (‘zero-respons’): geef via versneld schema (maand 0, 1 en 2) de combinatie Twinrix/Engerix-B.
- Titer ≥ detectiegrens, maar < 10 IE/l ('poor-respons'): geef één revaccinatie met de combinatie Twinrix/Engerix-B, waarna titerbepaling na 4-8 weken. Indien de titer < 10 IE/l blijft, geef alsnog twee revaccinaties met telkens een maand ertussen, waarna titerbepaling na 4-8 weken.
- Titerbepaling: 4-8 weken na drie Twinrix/Engerix-B-revaccinaties: indien de titer nog steeds < 10 IE/l is, zal de persoon met hiv worden meegedeeld dat die niet beschermd is tegen hepatitis B. Voor opties bij persisterende non-respons, zie paragraaf 2.5 Non-responders.
- Anti-HBc en/of HBsAg positief:
Figuur 3: HBV-vaccinatie bij bekend hivpositieve personen: cliënt is niet gevaccineerd tegen HBV of HBV-vaccinatiestatus is onbekend
DD: dubbele dosis in de vorm van combinatie Twinrix/Engerix-B of dubbele dosis Engerix-B (zie paragraaf 2.2.2)
DL: detectielimiet (van de betreffende anti-HBs-test)
Uitvoering: personen met hiv, ooit hepatitis B-vaccinatie serie gehad, mogelijk onvolledig (figuur 4)
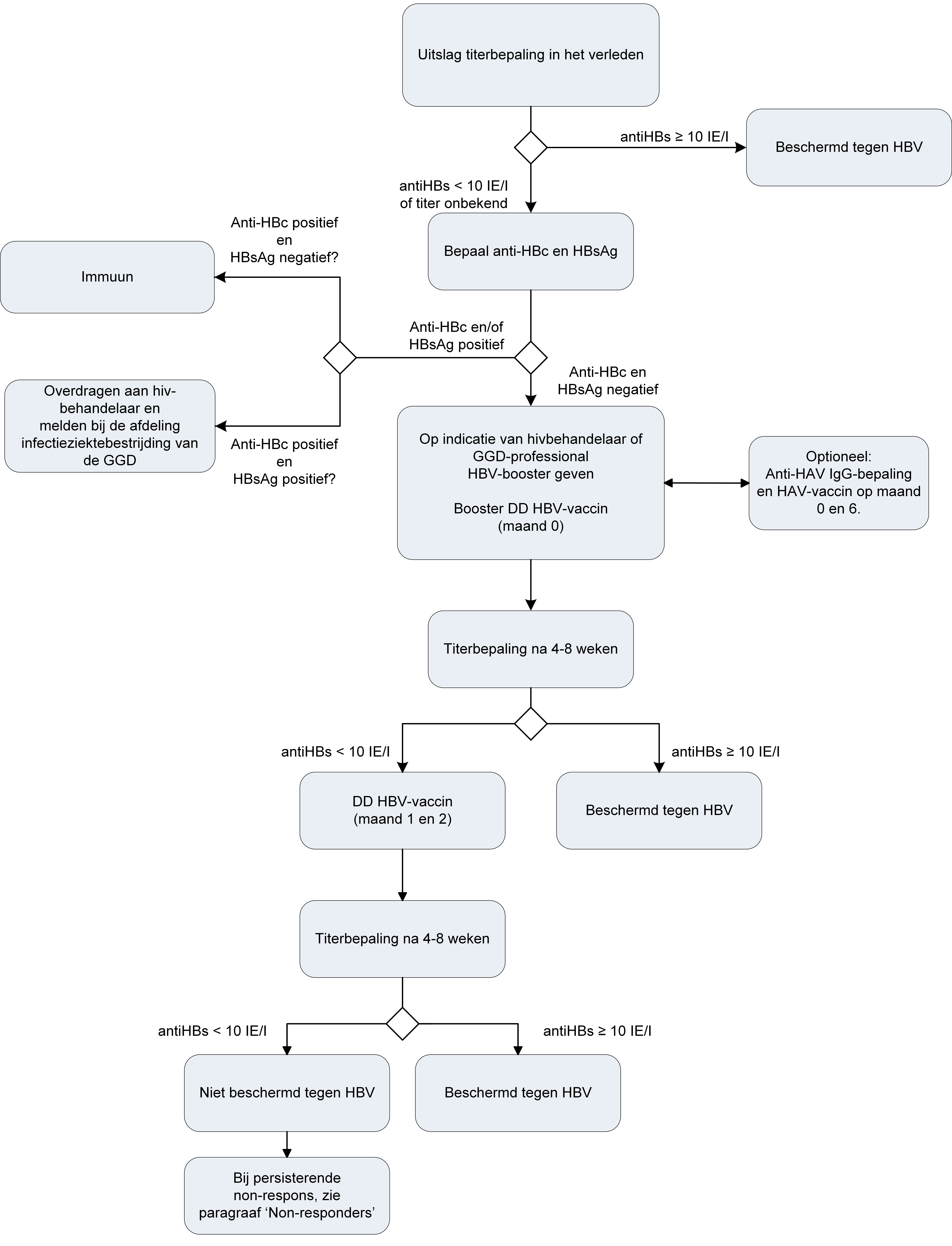
Ga bij voorkeur uit van bestaande documentatie van eerder gegeven vaccinaties. Indien er maar één vaccinatie gegeven is, wordt een nieuwe volledige serie geadviseerd conform het schema in figuur 3. Bij twee gegeven vaccinaties in het verleden is één booster geadviseerd conform onderstaande uitvoering (zie ook het schema in figuur 4).
- Anti-HBs in het verleden ≥ 10 IE/l: cliënt is beschermd.
- Anti-HBs in het verleden < 10 IE/l of onbekend: anti-HBc en HBsAg bepalen (cliënt kan tussen de vaccinaties in geïnfecteerd zijn).
- Anti-HBc en/of HBsAg positief:
- Anti-HBc positief en HBsAg negatief: cliënt is immuun.
- Anti-HBc positief en HBsAg positief: cliënt overdragen aan hivbehandelaar en melden bij de afdeling infectieziektebestrijding van de GGD.
- Anti-HBc en HBsAg negatief: cliënt krijgt een eenmalige booster met combinatie Twinrix/Engerix-B of dubbele dosis Engerix-B* hepatitis B-vaccinatie. Titerbepaling 4-8 weken na dubbele dosis:
- Anti-HBs ≥ 10 IE/l: cliënt is beschermd.
- Anti-HBs < 10 IE/l: er is sprake van een ‘non-respons’. Geef nogmaals een combinatie Twinrix/Engerix-B of dubbele dosis Engerix-B* op maand 1 en maand 2. Na de derde dubbele dosis: tweede titerbepaling na 4-8 weken:
- Anti-HBs ≥ 10 IE/l: de cliënt is beschermd.
- Indien de titer nog steeds < 10 IE/l is, zal de persoon met hiv worden meegedeeld dat die niet beschermd is tegen hepatitis B. Voor opties bij persisterende non-respons, zie paragraaf 2.5 Non-responders.
- Anti-HBc en/of HBsAg positief:
* Voor vaccinkeuze zie paragraaf 2.2.2. Bij personen met hiv met een indicatie voor hepatitis A-vaccinatie: indien na één booster met de combinatie Twinrix/Engerix-B reeds immuniteit is verkregen tegen hepatitis B, wordt geadviseerd ter bescherming tegen hepatitis A de vaccinatieserie af te maken via de hivbehandelaar. Dit valt buiten het programma.
Mensen met hiv die al een volledige vaccinatieserie met een enkele dosis HBV-vaccin gehad hebben (voor of na vaststelling van de hiv-infectie), hoeven niet nogmaals gevaccineerd te worden als er destijds een titerbepaling is gedaan en deze voldoende was (anti-HBs ≥ 10 IE/l). Er zijn geen aanwijzingen dat een volledige serie met een enkele dosis bij personen met hiv een andere beschermingsduur geeft dan een dubbele dosis. Als er geen titerbepaling is gedaan na een volledige serie met een enkele dosis HBV-vaccin, of de titer was onvoldoende, dan dient het schema in figuur 4 gevolgd te worden.
Indien een booster wordt gegeven na een volledige vaccinatieserie in het verleden waarbij geen titerbepaling heeft plaatsgevonden, is dit op eigen kosten van de cliënt.
Figuur 4: HBV-vaccinatie bij bekend hivpositieve personen: cliënt is ooit eerder gevaccineerd tegen HBV
DD: dubbele dosis in de vorm van combinatie Twinrix/Engerix-B of dubbele dosis Engerix-B (zie paragraaf 2.2.2)
3.2 Hivstatus onbekend, hepatitis B-status onbekend
Indien de hivstatus van de cliënt onbekend is op de soapolikliniek van de GGD, wordt een hivtest aangeboden. Er kan gekozen worden voor een hivsneltest die tijdens het eerste consult al direct een resultaat geeft.
Wanneer de cliënt niet op hiv getest wil worden, zal die gevaccineerd worden tegen hepatitis B (en eventueel hepatitis A) alsof deze persoon hivnegatief is (d.w.z. met een enkele dosis hepatitis B-vaccin). Aan de cliënt moet duidelijk uitgelegd worden dat er een aannemelijke kans is dat de vaccinatie onvoldoende beschermt als de persoon hivpositief is.
Indien de uitslag van de hivtest niet direct bekend is tijdens het eerste consult, kan in afwachting daarvan overwogen worden om al een enkele dosis hepatitis B-vaccinatie (Twinrix of enkele dosis Engerix-B) toe te dienen. Indien de hivtest later positief blijkt, dient er overgegaan te worden naar een dubbeledosisschema (Twinrix/Engerix-B of dubbele dosis Engerix-B op 0, 1 en 6 maanden). Dit kan in overleg met de toekomstige hivbehandelaar gedaan worden op de GGD of op de hivpolikliniek, afhankelijk van de regionale afspraken. De eerste enkele dosis die de cliënt heeft ontvangen, moet als niet gegeven worden beschouwd.
3.3 Vaccineren tijdens outreach-acties
Optimale individuele zorg is niet op elke plek mogelijk en bij een moeilijk te bereiken doelgroep wegen de voordelen van een vaccinatie tijdens een outreach-activiteit op tegen de nadelen van een minder optimaal inhoudelijk beleid. Het toedienen van een vaccinatie kan weinig kwaad omdat bijwerkingen zeer beperkt zijn; wel is de effectiviteit in sommige gevallen helaas sub-optimaal. Voor de outreach-acties heeft dan ook het toedienen van de eerste vaccinatie prioriteit. Tijdens outreach-acties kan actief naar de hivstatus van cliënten worden gevraagd. Cliënten worden er mondeling van op de hoogte gebracht dat de vaccinatie mogelijk niet goed werkt als ze hivpositief zijn.
Na deze uitleg kan de cliënt alsnog uit zichzelf aangeven dat die hivpositief is. In dat geval is het niet verstandig om deze persoon tijdens de outreach-actie te vaccineren, maar is het beter om door te verwijzen naar de eigen hivbehandelaar of een aparte afspraak te maken bij de GGD.
3.4 Registratie
Indien een vaccinatie wordt gegeven aan een persoon met hiv, moet dit geregistreerd worden in het landelijk registratiesysteem, inclusief de gebruikte vaccins. Dit vergemakkelijkt latere effectiviteitsonderzoeken ter evaluatie van de vaccinatiestrategie.
4. Literatuur
- Bakker M, Bunge EM, Marano C, de Ridder M, De Moerlooze L. Immunogenicity, effectiveness and safety of combined hepatitis A and B vaccine: a systematic literature review. Expert Rev Vaccines. 2016;15(7):829-51. doi.org/10.1586/14760584.2016.1150182
- Cardell K, Akerlind B, Sällberg M, Frydén A. Excellent response rate to a double dose of the combined hepatitis A and B vaccine in previous nonresponders to hepatitis B vaccine. J Infect Dis. 2008;198(3):299-304. doi.org/10.1086/589722
- Cornejo-Juárez P, Volkow-Fernández P, Escobedo-López K, Vilar-Compte D, Ruiz-Palacios G, Soto-Ramírez LE. Randomized controlled trial of Hepatitis B virus vaccine in HIV-1-infected patients comparing two different doses. AIDS Res Ther. 2006;3:9. doi.org/10.1186/1742-6405-3-9
- Cruciani M, Mengoli C, Serpelloni G, Lanza A, Gomma M, Nardi S, et al. Serologic response to hepatitis B vaccine with high dose and increasing number of injections in HIV infected patients. Vaccine. 2009;27(1):17-22. doi.org/10.1016/j.vaccine.2008.10.040
- de Vries-Sluijs T, Andrinopoulou ER, de Man RA, van der Ende ME. Fendrix® compared to Engerix® in HIV-infected patients nonresponding to initial- and re-vaccination schedule. Neth J Med. 2020;78(6):376-80.
- de Vries-Sluijs TE, Hansen BE, van Doornum GJ, Kauffmann RH, Leyten EM, Mudrikova T, et al. A randomized controlled study of accelerated versus standard hepatitis B vaccination in HIV-positive patients. J Infect Dis. 2011;203(7):984-91. https://doi.org/10.1093/infdis/jiq137
- EMA. Samenvatting van de productkenmerken Twinrix. 2024. Beschikbaar via: www.ema.europa.eu/nl/documents/product-information/twinrix-adult-epar-product-information.nl.pdf
- Farooq PD, Sherman KE. Hepatitis B Vaccination and Waning Hepatitis B Immunity in Persons Living with HIV. Curr HIV/AIDS Rep. 2019;16(5):395-403. doi.org/10.1007/s11904-019-00461-6
- Flynn PM, Cunningham CK, Rudy B, Wilson CM, Kapogiannis B, Worrell C, et al. Hepatitis B vaccination in HIV-infected youth: a randomized trial of three regimens. J Acquir Immune Defic Syndr. 2011;56(4):325-32. doi.org/10.1097/QAI.0b013e318203e9f2
- Fonseca MO, Pang LW, de Paula Cavalheiro N, Barone AA, Heloisa Lopes M. Randomized trial of recombinant hepatitis B vaccine in HIV-infected patients comparing a standard dose to a double dose. Vaccine. 2005;23(22):2902-8. https://doi.org/10.1016/j.vaccine.2004.11.057
- Fritzsche C, Bergmann L, Loebermann M, Glass A, Reisinger EC. Immune response to hepatitis A vaccine in patients with HIV. Vaccine. 2019;37(16):2278-83. doi.org/10.1016/j.vaccine.2019.02.064
- Heuft MM, Houba SM, van den Berk GE, Smissaert van de Haere T, van Dam AP, Dijksman LM, et al. Protective effect of hepatitis B virus-active antiretroviral therapy against primary hepatitis B virus infection. Aids. 2014;28(7):999-1005. doi.org/10.1097/qad.0000000000000180
- Jimenez HR, Hallit RR, Debari VA, Slim J. Hepatitis A vaccine response in HIV-infected patients: are TWINRIX and HAVRIX interchangeable? Vaccine. 2013;31(9):1328-33. doi.org/10.1016/j.vaccine.2012.12.045
- Landrum ML, Huppler Hullsiek K, Ganesan A, Weintrob AC, Crum-Cianflone NF, Barthel RV, et al. Hepatitis B vaccine responses in a large U.S. military cohort of HIV-infected individuals: another benefit of HAART in those with preserved CD4 count. Vaccine. 2009;27(34):4731-8. https://doi.org/10.1016/j.vaccine.2009.04.016
- Lee JH, Hong S, Im JH, Lee JS, Baek JH, Kwon HY. Systematic review and meta-analysis of immune response of double dose of hepatitis B vaccination in HIV-infected patients. Vaccine. 2020;38(24):3995-4000. doi.org/10.1016/j.vaccine.2020.04.022
- Machiels JD, Braam EE, van Bentum P, van Vugt M, de Vries-Sluijs T, Schouten I, et al. Vaccination with Fendrix of prior nonresponding patients with HIV has a high success rate. Aids. 2019;33(3):503-7. doi.org/10.1097/qad.0000000000002085
- Marks KM, Kang M, Umbleja T, Cox A, Vigil KJ, Ta NT, et al. HepB-CpG vs HepB-Alum Vaccine in People With HIV and Prior Vaccine Nonresponse: The BEe-HIVe Randomized Clinical Trial. Jama. 2025;333(4):295-306. doi.org/10.1001/jama.2024.24490
- Mena G, García-Basteiro AL, Bayas JM. Hepatitis B and A vaccination in HIV-infecteds: A review. Hum Vaccin Immunother. 2015;11(11):2582-98. doi.org/10.1080/21645515.2015.1055424
- Raven SFH, Hoebe C, Vossen A, Visser LG, Hautvast JLA, Roukens AHE, et al. Serological response to three alternative series of hepatitis B revaccination (Fendrix, Twinrix, and HBVaxPro-40) in healthy non-responders: a multicentre, open-label, randomised, controlled, superiority trial. Lancet Infect Dis. 2020;20(1):92-101. doi.org/10.1016/s1473-3099(19)30417-7
- Schnyder JL, Garcia Garrido HM, Tanck MW, Maurer I, Harskamp AM, Kootstra N, et al. Hepatitis a vaccine immunogenicity and boostability ins receiving immunosuppressive therapy ands living with HIV: a prospective single-centre cohort study. J Travel Med. 2025;32(2). https://doi.org/10.1093/jtm/taae125
- SHM. HIV Monitoring Report 2024. 2024. Beschikbaar via: www.hiv-monitoring.nl/application/files/8117/3212/3792/STICHTING_HIV_MONITORING_REPORT_2024.pdf
- Tedaldi EM, Baker RK, Moorman AC, Wood KC, Fuhrer J, McCabe RE, et al. Hepatitis A and B vaccination practices for ambulatory patients infected with HIV. Clin Infect Dis. 2004;38(10):1478-84. doi.org/10.1086/420740
- Tian Y, Hua W, Wu Y, Zhang T, Wang W, Wu H, et al. Immune Response to Hepatitis B Virus Vaccine Among People Living With HIV: A Meta-Analysis. Front Immunol. 2021;12:745541. doi.org/10.3389/fimmu.2021.745541
- Ungulkraiwit P, Jongjirawisan Y, Atamasirikul K, Sungkanuparph S. Factors for predicting successful immune response to hepatitis B vaccination in HIV-1 infected patients. Southeast Asian J Trop Med Public Health. 2007;38(4):680-5.
- Van der Wielen M, Van Damme P, Chlibek R, Smetana J, von Sonnenburg F. Hepatitis A/B vaccination ofs over 40 years old: comparison of three vaccine regimens and effect of influencing factors. Vaccine. 2006;24(26):5509-15. doi.org/10.1016/j.vaccine.2006.04.016
- Veiga AP, Casseb J, Duarte AJ. Humoral response to hepatitis B vaccination and its relationship with T CD45RA+ (naïve) and CD45RO+ (memory) subsets in HIV-1-infected subjects. Vaccine. 2006;24(49-50):7124-8. doi.org/10.1016/j.vaccine.2006.06.079