Landelijke richtlijn preventie iatrogene transmissie van hepatitis B-virus
Samenvatting
Uitgangspunten
- De (hepatitis B-virus)-status (immuun/niet-immuun/geïnfecteerd) van elke risicovormer moet vastgelegd zijn.
- Risicohandelingen zijn niet toegestaan als de HBV-status onbekend is.
- Risicohandelingen zijn niet toegestaan als er HBV-infectie is met HBV-DNA load hoger dan 1000 IU/mL.
Aanbevelingen
- Elke risicovormer1 moet gevaccineerd zijn tegen hepatitis B, met controle van de respons (antistoftiterbepaling: anti-HBs).
- Bij non-responders en bij vaccinweigeraars moet gecontroleerd worden of er infectie is met HBV.
- Een risicovormende non-responder of vaccinweigeraar zonder HBV-infectie kan doorwerken, mits deze persoon ieder kwartaal gecontroleerd wordt met een HBsAg-test op afwezigheid van HBV-infectie, en met een anti-HBcore test op afwezigheid van seroconversie (seroconversie wijst op recent doorgemaakte HBV-infectie).
- In geval van HBV-infectie moet bepaald worden of de risicovormer kan doorwerken.
- Voor een zelfstandig werkende risicovormer geldt dat deze persoon zelf verantwoordelijk is voor het sluitend toepassen van deze richtlijn.
- Bij personeel in dienstverband zijn risicovormer en werkgever beiden verantwoordelijk. Hierbij dient ook rekening gehouden te worden met de van toepassing zijnde privacywetgeving. Afspraken over infectiepreventie dienen geborgd te worden in het lokale instellingsbeleid, in samenspraak met de bedrijfsarts of arbodienst.
1 Een risicovormer is iemand die risicohandelingen uitvoert. Risicohandelingen zijn die handelingen waarbij de kans op bloed-bloedcontact tussen gezondheidszorgwerker en patiënt groot is. Het betreft vooral handelingen waarbij de (gehandschoende) handen binnen lichaamsholten of wonden in contact kunnen komen met scherpe instrumenten, naalden of scherpe weefseldelen (bijvoorbeeld botpunten of gebitselementen), terwijl de handen of vingertoppen soms niet zichtbaar zijn.
Risicovormers zijn onder andere:
- tandartsen, mondhygiënisten, orthodontisten, orthodontie-assistenten, en sommige tandartsassistenten;
- verloskundigen;
- bepaalde medische specialisten, bepaalde verpleegkundigen, bepaalde paramedische medewerkers.
Aanpassing op organisatorische aspecten
Deze richtlijn is op organisatorische aspecten aangepast naar aanleiding van het opheffen van de commissie Preventie Iatrogene Transmissie van (hepatitis B-virus), (hepatitis C-virus) en hiv (PIT) per 1 september 2025.
Het opheffen van de commissie betekent dat de door de commissie uitgevoerde centrale monitoring van patiënten die hepatitis-B-drager zijn en risicovormend werk verrichten is gestopt. Meer informatie over de afbouw van de commissie, de rol van de (Landelijke Coördinatie Infectieziektebestrijding) en de verantwoordelijkheden van zorgverlener en zorgaanbieder staat in de inleiding.
Vaststelling 4e editie door commissie Preventie Iatrogene Transmissie: 6 april 2021.
Vaststelling 4e editie door (Landelijk Overleg Infectieziektebestrijding): 21 september 2021.
Wijzigingen sinds vaststelling
- 23 april 2026: In de samenvatting stond dat risicovormende hyporesponders ieder kwartaal gecontroleerd moeten worden op de afwezigheid van (hepatitis B-virus)-infectie. Dit is niet het geval, en derhalve weggehaald.
- 28 augustus 2025: De richtlijn is op organisatorische aspecten aangepast naar aanleiding van het opheffen van de commissie Preventie Iatrogene Transmissie van HBV, (hepatitis C-virus) en hiv (PIT) per 1 september 2025. De centrale monitoring en controle van patiënten die hepatitis B-drager zijn en risicovormend werk verrichten stopt. Het is niet meer nodig risicovormende zorgmedewerkers met een HBV-infectie te melden bij de commissie. De controle en actieve monitoring moet nog wel worden uitgevoerd maar wordt overgelaten aan de werkgever (zorgaanbieder) en de desbetreffende zorgmedewerker (zorgverlener). De adviserende rol van de commissie wordt overgenomen door de (Landelijke Coördinatie Infectieziektebestrijding) van het (Rijksinstituut voor Volksgezondheid en Milieu).
Nieuw in de 4e editie (2021)
- De mate van HBV-viremie bij een risicovormer, waarboven hij/zij geen risicovormende handelingen mag uitvoeren, is verlaagd naar 1000 IU/mL HBV DNA.
- De richtlijn biedt concrete aanwijzingen bij beoordeling van geschiktheid van een risicovormer met HBV-vaccinatie in het verleden, zie het stroomschema.
- Het controlebeleid bij vaccinweigeraars en non-responders is aangescherpt.
1. Inleiding
Deze richtlijn beschrijft het beleid dat moet voorkomen dat een gezondheidszorgwerker met een hepatitis B-virusinfectie (HBV-infectie) patiënten besmet. Het beleid omvat de maatregelen bij risicovormers met HBV-infectie, bij risicovormers die HBV-vaccinatie weigeren, en bij risicovormers die niet reageren op HBV-vaccinatie.
Werkers in de gezondheidszorg kunnen behalve 'risicoloper' ook ‘risicovormer’ zijn ten aanzien van transmissie van HBV. Deze richtlijn beperkt zich tot het beleid bij risicovormend personeel en is niet van toepassing op personen die alleen risico lopen. Risicovormend personeel omvat het personeel dat risicohandelingen uitvoert (zie 2.1). Ter bescherming van de patiënten is het van belang dat risicovormend personeel tijdens de beroepsuitoefening geen HBV overdraagt op patiënten. Deze richtlijn beschrijft het beleid dat daarvoor nodig is.
Afbouw commissie Preventie Iatrogene Transmissie
Per 1 september 2025 is de commissie Preventie Iatrogene Transmissie van HBV, (hepatitis C-virus) en HIV (PIT) opgeheven. De commissie was actief tussen 1 februari 2000 en 1 september 2025. De commissie stelde zelf richtlijnen en documenten op, die de Landelijke Coördinatie Infectieziektebestrijding (LCI) op haar website publiceerde. Met de afbouw van de commissie wordt de centrale monitoring van patiënten die hepatitis B-drager zijn en risicovormend werk verrichten, niet meer uitgevoerd door de commissie. Ondanks het stoppen van de commissie blijft het monitoren van patiënten noodzakelijk.
Taken en verantwoordelijkheden
Werkgever en werknemer in loondienst
Het toe te passen beleid gericht op het voorkomen van transmissie van hepatitis B door risicovormers die HBV-geïnfecteerd zijn, valt in geval van loondienst onder de verantwoordelijkheid van de werkgever (zorgaanbieder) en de betreffende gezondheidszorgwerker (zorgverlener). Zij zijn beiden, op basis van artikel 2 wet kwaliteit, klachten en geschillen zorg (Wkkgz), primair verantwoordelijk voor het (laten) monitoren van de virale load op basis van de richtlijn. Hierbij dient ook rekening gehouden te worden met de van toepassing zijnde privacywetgeving. Afspraken over infectiepreventie dienen geborgd te worden in het lokale instellingsbeleid, in samenspraak met de bedrijfsarts of arbodienst.
Zelfstandigen
Een zelfstandig werkende risicovormer die HBV-geïnfecteerd is, is zelf verantwoordelijk (Wkkgz) voor het sluitend toepassen van de richtlijn, in samenspraak met de behandelaar, huisarts of verbonden bedrijfsarts/arbodienst.
Bedrijfsarts en behandelaar
De bedrijfsarts of arbodienst kan, eventueel in samenspraak met de behandelaar of huisarts, beoordelen of de virale load van betrokkene onder of boven de detectiegrens zit door deze richtlijn toe te passen.
IGJ
De Inspectie Gezondheid en Jeugd (IGJ) ziet toe op het algehele beleid.
RIVM/LCI
Het RIVM/LCI is beschikbaar voor advies bij het duiden van de richtlijn en bij vragen over individuele casuïstiek.
Achtergrond
Hepatitis B is een infectieziekte die zowel seksueel als via bloed-bloedcontact overdraagbaar is. Door de transmissie via bloed-bloedcontact hebben werkers in de gezondheidszorg een grotere kans om de infectie op te lopen (‘risicolopers’) dan de algemene bevolking. In 1999 bleek dat HBV-dragerschap van een chirurg in een Nederlands ziekenhuis heeft geleid tot besmetting van een aanzienlijk aantal patiënten (1,2,21). Ook elders in de medische literatuur zijn incidenten beschreven waarbij HBV is overgedragen van een gezondheidszorgwerker naar een patiënt (3-12). Overdracht van HBV van personeel naar patiënt blijkt vooral op te treden tijdens 'risicohandelingen'.
Risicovormend personeel met HBV-infectie
De afweging of een HBV-drager risicovormend werk kan voortzetten is soms moeilijk. Een werkverbod kan grote consequenties hebben voor de betrokkene en zijn organisatie. Het RIVM/LCI is beschikbaar voor advies, bijvoorbeeld over het interpreteren van de viral load of de condities waarbij een HBV-drager het werk kan voortzetten (zie voor adresgegevens hoofdstuk 6).
Het belang van vaccinatie van risicovormers en van controle na vaccinatie
Het identificeren van HBV-geïnfecteerde risicovormers is cruciaal voor de preventie van iatrogene HBV-infectie. Vaccinatie tegen hepatitis B is onmisbaar voor deze preventie, omdat vaccinatie infectie van risicovormers voorkomt, en omdat via de controle na vaccinatie HBV-geïnfecteerde risicovormers opgespoord worden. Deze richtlijn beschrijft daarom hoe de respons op HBV-vaccinatie bij risicovormers gecontroleerd moet worden. In het bijzonder wordt gewezen op de betekenis van afwezige (21) of geringe (22) immuunrespons na HBV-vaccinatie, waarbij altijd de verdenking op HBV-dragerschap moet bestaan en waarbij nader onderzoek nodig is.
2. Richtlijn voor de preventie van transmissie van HBV van personeel naar patiënten
2.1 Definitie van risicohandelingen
Deze richtlijn heeft betrekking op risicovormend personeel, oftewel personeel dat risicohandelingen uitvoert. Daarbij is het begrip risicohandelingen (exposure prone procedures) als volgt gedefinieerd:
Risicohandelingen zijn die handelingen waarbij de kans op bloed-bloedcontact tussen gezondheidszorgwerker en patiënt groot is. Het betreft vooral handelingen waarbij de (gehandschoende) handen binnen lichaamsholten of wonden in contact kunnen komen met scherpe instrumenten, naalden of scherpe weefseldelen (bijvoorbeeld botpunten of gebitselementen), terwijl de handen of vingertoppen soms niet zichtbaar zijn.
Tandartsen, verloskundigen, orthodontisten, orthodontie-assistenten en mondhygiënisten vallen per definitie onder risicovormend personeel. Tandartsassistenten zijn risicovormend als zij tandheelkundige handelingen uitvoeren. Bepaalde medische specialismen, bepaalde verpleegkundigen en bepaald paramedisch personeel is risicovormend.
De richtlijn bevat bewust geen opsomming van alle denkbare risicohandelingen, omdat een dergelijke opsomming nooit compleet kan zijn en niet inspeelt op nieuwe ontwikkelingen. De richtlijn volgt de benadering van de ‘U.K. Health Department’s Expert Advisory Group on AIDS’. Deze adviesgroep heeft sinds 1993 gegevens verzameld over risicohandelingen voor de overdracht van bloedoverdraagbare virussen. Dit heeft geleid tot de benoeming van belangrijke risicohandelingen voor verschillende disciplines binnen de gezondheidszorg. Deze lijst van risicohandelingen is niet compleet, maar kan hulp bieden bij adviezen per discipline. Het rapport van de U.K. Health Advisory Group met de voorbeelden van risicohandelingen per specialisme is als bijlage 1 toegevoegd (met dank aan Dr. Hugh Nicholas van de U.K. Health Department’s Expert Advisory Group on AIDS). Het RIVM/LCI is beschikbaar om advies uit te brengen in geval van vragen over risicohandelingen.
2.2 Uitgangspunten en overwegingen
Voor risicovormend personeel geldt:
- Om de veiligheid van patiënten te garanderen moet van elke gezondheidszorgwerker die risicohandelingen verricht de HBV-status vastgelegd zijn en zo nodig vervolgd worden. Hierbij dient rekening gehouden te worden met de van toepassing zijnde privacywetgeving. Afspraken over infectiepreventie dienen geborgd te worden in het lokale instellingsbeleid, in samenspraak met de bedrijfsarts of arbodienst.
- Elke risicovormer moet weten of hij/zij immuun is voor hepatitis B, of geïnfecteerd is, of geïnfecteerd kan raken met HBV.
- In de praktijk wordt de HBV-status van een risicovormer meestal vastgesteld bij de controle na vaccinatie tegen HBV. Controle na HBV-vaccinatie van een risicovormer is van groot belang en dient te worden nageleefd volgens het schema in paragraaf 2.9.
- Een risicovormer met HBV-infectie die gepaard gaat met een hoge mate van HBV-viremie vormt een besmettingsrisico voor de patiënt.
- Een risicovormer die niet immuun is voor HBV kan geïnfecteerd raken en daardoor een besmettingsrisico vormen voor de patiënt.
- Bij non- en hyporesponderschap na HBV-vaccinatie kan sprake zijn van HBV-infectie.
- Ter bescherming van de patiënt is een zo hoog mogelijke vaccinatiegraad tegen HBV gewenst bij gezondheidszorgwerkers die een risico voor de patiënt kunnen vormen (23).
- Het niet-ondergaan van HBV-vaccinatie door een gezondheidszorgwerker die risicohandelingen uitvoert (vaccinweigeraar), is terug te voeren ofwel op verwijtbare nalatigheid, ofwel op te eerbiedigen medische, religieuze of andere bezwaren, waarbij de medewerker zijn of haar visie stelt boven het risico de patiënt te besmetten.
- De kennis over de grootte van de kans op overdracht van HBV door een laag- of hoog-viremische bron is beperkt.
- Een grenswaarde, op grond waarvan men chronische HBV-infectie met hoge viremie onderscheidt van infectie met lage viremie, is arbitrair, maar onmisbaar voor te voeren beleid.
- Een onderverdeling in medische handelingen met en zonder risico op HBV-overdracht is arbitrair, maar onmisbaar voor te voeren beleid.
- Behandeling met antivirale middelen van een persoon met chronische HBV-infectie kan leiden tot sterke reductie van de mate van viremie. Terugval naar hoge viremie kan optreden tijdens of na therapie. Bij therapie is begeleiding door hepatoloog of internist-infectioloog aangewezen.
2.3 Definities
Begrippen die relevant zijn voor deze richtlijn zijn als volgt gedefinieerd:
- Chronische HBV-infectie en recente HBV-infectie. Het begrip ‘hepatitis B’ is verwarrend omdat het gebruikt wordt bij recente en bij chronische infectie met HBV, zowel bij symptomatisch als bij asymptomatisch beloop van de infectie. Het begrip ‘HBV-infectie’ voorkomt verwarring.
- HBV-infectie: hiervan is sprake indien een enzym-immuno-assay voor detectie van HBsAg positief is waarbij ofwel een neutralisatieprocedure het testresultaat bevestigt, ofwel een positieve HBV-DNA test de uitslag bevestigt. Bij een eerste, éénmalige detectie van HBsAg is aanvullend onderzoek nodig om onderscheid te maken tussen recente en chronische HBV-infectie. Ook (eventueel geïsoleerde) aanwezigheid van HBV-DNA wijst op HBV-infectie.
- Recente HBV-infectie: indien aanwezigheid van HBsAg korter dan zes maanden is.
- Chronische HBV-infectie of HBV dragerschap: als HBsAg zes maanden of langer aanwezig is.
- Mate van viremie. Voor deze richtlijn geldt: een HBV-drager is hoog-viremisch als de viremie meer dan 1000 IU/mL HBV-DNA bedraagt. Een HBV-drager is laag-viremisch als de viremie 1000 IU/mL of minder bedraagt. Het vaststellen van de mate van viremie moet voldoen aan kwaliteitseisen, volgens paragraaf 2.10 van deze richtlijn. Aanwezigheid van het e-antigeen wijst in de regel op een hoge mate van viremie. Een hoge mate van viremie kan echter ook voorkomen in afwezigheid van het e-antigeen. Acute, recente HBV-infectie wordt per definitie als hoog-viremisch beschouwd.
- Risicohandelingen. Zie paragraaf 2.1.
2.4 Beleid ten aanzien van HBV-geïnfecteerd risicovormend personeel
- In de praktijk wordt de HBV-status van een risicovormer vastgesteld bij de controle na vaccinatie tegen HBV. Controle na HBV-vaccinatie van een risicovormer is van groot belang en moet worden nageleefd volgens het schema in paragraaf 2.9.
- Bij een HBV-geïnfecteerde risicovormer moet vastgesteld worden of sprake is van chronische of recente (acute) HBV-infectie.
- Bij een risicovormer met chronische HBV-infectie moet de mate van viremie worden vastgesteld volgens paragraaf 2.10 van deze richtlijn.
- Uitgesloten van risicohandelingen zijn:
- Personen met meer dan 1000 IU/mL HBV-DNA;
- HBV-dragers met onbekende mate van viremie;
- personen met recente HBV-infectie.
- Een gezondheidszorgwerker met laag-viremische chronische HBV-infectie mag alle risicohandelingen uitvoeren, mits de mate van viremie minstens eens per zes maanden wordt gemeten en de gevonden viremie daarbij steeds niet hoger is dan 1000 IU/mL.
- Bij het uitvoeren van risicohandelingen moeten de hygiënische voorzorgen, zoals vermeld in de richtlijnen van het Samenwerkingsverband Richtlijnen Infectiepreventie (SRI), uiteraard steeds nauwkeurig worden nageleefd.
- De gezondheidszorgwerker (zorgverlener) en diens werkgever (zorgaanbieder) zijn primair verantwoordelijk voor het (laten) monitoren van de virale load op basis van de richtlijn. Hierbij dient rekening gehouden te worden met de van toepassing zijnde privacywetgeving. Afspraken over infectiepreventie dienen geborgd te worden in het lokale instellingsbeleid, in samenspraak met de bedrijfsarts of arbodienst.
- Als een tot dan toe laag-viremische drager die risicohandelingen uitvoert, bij controle een HBV-viremie vertoont van meer dan 1000 IU/mL, geldt dat
per direct risicovormende handelingen gestaakt moeten worden (zie volgende paragraaf voor beleid herstarten werkzaamheden). - RIVM/LCI is bereikbaar voor advies en hulp bij duiden van de richtlijn (zie hoofdstuk 6 voor contactgegevens).
Antivirale therapie
- Een chronisch HBV-geïnfecteerde medewerker, die voorafgaand aan antivirale behandeling veelal hoog-viremisch was, en tijdens voortgaande behandeling laag-viremisch is, mag risicohandelingen uitvoeren. Bij het beleid moet men rekening houden met de kans op spontane terugval naar hoge viremie tijdens antivirale therapie en na staken van antivirale therapie.
- Na het starten van therapie moet de HBV-viremie in minstens twee metingen, met een interval van minstens drie maanden, niet hoger zijn dan 1000 IU/mL, voordat de medewerker met zekerheid ‘laag-viremisch’ is en risicohandelingen mag gaan uitvoeren.
- Vervolgens moet tijdens de antivirale therapie (vrijwel altijd met entecavir of tenofovir) de mate van viremie minstens eens per zes maanden worden gemeten.
- Na het staken van antivirale therapie wordt gedurende één jaar de mate van viremie om de drie maanden gemeten. In de periode daarna vindt de monitoring van de viral load om de zes maanden plaats.
- De betrokken medewerker en -indien van toepassing- de werkgever zijn verantwoordelijk voor het correct toepassen en/of laten uitvoeren van het beleid. Zodra bij een meting de mate van viremie groter blijkt dan 1000 IU/mL: zie de voorafgaande alinea.
Beleid bij incidenten
- Indien een niet-HBV-immune patiënt is blootgesteld aan bloed van een HBV-positieve medewerker, moet HB-immunoglobuline en HBV-vaccin aan de patiënt worden toegediend (zie de Landelijke Richtlijn Prikaccidenten).
- Indien een redelijk vermoeden bestaat dat zich één of meer gevallen van hepatitis hebben voorgedaan in aansluiting op medische ingrepen, verricht door een HBV-geïnfecteerde gezondheidszorgwerker, is het van belang contact op te nemen met de regionale (Gemeentelijke gezondheidsdienst) (zie ook de LCI-richtlijn Hepatitis B, onderdeel maatregelen en meldingsplicht). De GGD kan retrospectief onderzoek starten in samenwerking met de instelling en indien gewenst overleggen met LCI/RIVM of aan LCI/RIVM een signaal doorgeven.
Samenvatting van het beleid bij een HBV-geïnfecteerde risicovormer
- Een laag-viremische HBV-drager mag risicohandelingen uitvoeren. De mate van viremie moet daarbij regelmatig gecontroleerd worden.
- Een hoog-viremische HBV-drager mag geen risicohandelingen verrichten.
- Tijdens en na anti-virale therapie gelden speciale voorschriften voor de risicovormer.
2.5 Beleid ten aanzien van niet-gevaccineerd risicovormend personeel (vaccinweigeraars)
Een niet-gevaccineerd persoon, die ook geen immuniteit heeft verworven door doorgemaakte, geklaarde HBV-infectie, mag risicohandelingen verrichten, mits hij of zij elk kwartaal getest wordt op HBsAg en op anti-HBcore, waarbij beide testresultaten negatief moeten zijn. Bij elk ander testresultaat van het vervolgonderzoek (bijvoorbeeld als HBsAg plots positief is, maar ook als alleen anti-HBcore plots positief is) moeten onmiddellijk alle risicovormende handelingen gestaakt worden. Seroconversie van anti-HBcore antistoffen kan betekenen dat recent acute HBV-infectie is doorgemaakt.
Als bij een eerste onderzoek al blijkt dat er mogelijk sprake is van doorgemaakte HBV-infectie (HBsAg=negatief, anti-HBcore=positief): zie 2.8.
2.6 Beleid ten aanzien van gevaccineerd risicovormend personeel
Zie ook het stroomschema van paragraaf 2.9.
A) Serologische controle van recente HBV-vaccinatie bij risicovormer
Aansluitend op volledige HBV-vaccinatie moet de aanwezigheid van immuniteit bij risicovormers gecontroleerd worden volgens paragraaf 2.9 van deze richtlijn, inclusief het nadere onderzoek als de anti-HBs-spiegel lager dan 100 IE/L blijkt te zijn.
- Een anti-HBs-titer na vaccinatie van 100 IE/L of hoger geeft langdurige bescherming. Het vervolgens dalen of niet-detecteerbaar worden van de anti-HBs is niet relevant. Revaccinatie is vooralsnog ook bij risicovormers niet noodzakelijk (24-26).
- Bij een anti-HBs-respons in het gebied van 10 t/m 99 IE/L is sprake van een hypo-responder. Een hypo-responder kan geïnfecteerd zijn met HBV, omdat HBV-infectie soms gepaard gaat met de aanwezigheid van een lage spiegel anti-HBs (27). Als nader onderzoek conform paragraaf 2.9 afwezigheid van HBV-infectie uitwijst, wordt een anti-HBs-titer na vaccinatie van 10 tot 100 IE/L beschouwd als teken van immuniteit gedurende vijf jaar. Boostering (gevolgd door titercontrole) na vijf jaar is vooralsnog noodzakelijk, met aansluitend controle conform het stroomschema van 2.9. Als er HBV-infectie blijkt te zijn: zie paragraaf 2.4.
- Bij een anti-HBs-titer na vaccinatie lager dan 10 IE/L is sprake van een non-responder, met of zonder HBV-infectie, zie paragraaf 2.7.
B) Beleid bij gedocumenteerde HBV-vaccinatie in het verleden
Als de risicovormer schriftelijk bewijs heeft dat de anti-HBs titer na HBV-vaccinatie in het verleden minstens 100 IE/L bedroeg, dan mogen risicovormende handelingen uitgevoerd worden en is titercontrole of revaccinatie vooralsnog niet nodig.
Als de gedocumenteerde anti-HBs respons minder is dan 100 IE/L: overweeg hernieuwde vaccinatie met vervolgens titercontrole en herbeoordeling, of pas het beleid toe zoals beschreven voor hypo- en non-responders.
C) Beleid bij onvoldoende gedocumenteerde HBV-vaccinatie in het verleden
Als er geen documentatie is van de anti-HBs titer na vaccinatie in het verleden moet anti-HBs bepaald worden. Als vaccinatie langer dan een jaar geleden plaats vond is anti-HBs misschien weggezakt en moet 1 (booster)dosis HBV-vaccin toegediend worden, met anti-HBs controle 4-8 weken later en moet schema 2.9 doorlopen worden alsof vaccinatie recent is afgerond.
2.7 Beleid ten aanzien van risicovormende non-responders
Een ‘non-responder’ is een persoon die na volledige HBV-vaccinatie een anti-HBs respons vertoont lager dan 10 IE/L. Een non-responder kan geïnfecteerd zijn met HBV (21), aanvullende serologie moet plaatsvinden conform het stroomschema (2.9):
- Als de non-responder HBV-geïnfecteerd blijkt te zijn (HBsAg positief): zie 2.4.
- Een HBsAg negatieve en anti-HBcore negatieve non-responder mag risicohandelingen verrichten, mits hij of zij elk kwartaal getest wordt op HBsAg en op anti-HBcore, waarbij beide testresultaten negatief moeten zijn. Bij elk ander testresultaat van het vervolgonderzoek (bijvoorbeeld als HBsAg plots positief is, maar ook als alleen anti-HBcore plots positief is) moeten onmiddellijk alle risicovormende handelingen gestaakt worden. Seroconversie van anti-HBcore antistoffen kan betekenen dat recent acute HBV-infectie is doorgemaakt.
- Voor HBsAg-negatieve non-responders, die bij controle na vaccinatie anti-HBcore-positief blijken te zijn: zie 2.8.
2.8 Beleid bij risicovormers met mogelijk of waarschijnlijk doorgemaakte, genezen HBV-infectie
Bij geïsoleerde aanwezigheid van anti-HBcore antistoffen (anti-HBcore=positief, HBsAg en anti-HBs zijn beide negatief; “anti-core only”) is er mogelijk sprake van doorgemaakte, genezen HBV-infectie met immuniteit.
Bij een eerste “anti-core only”-bevinding moet aanvullend een (immunoglobuline M) anti-HBcore-antistoftest ingezet worden, om recent geklaarde HBV-infectie uit te sluiten. Bij een positieve IgM anti-HBcore uitslag kan overlegd worden met RIVM/LCI.
Er kan ook sprake zijn van een fout-positieve anti-HBcore-test zonder doorgemaakte HBV-infectie en zonder immuniteit.
Betrokkene mag risicovormende handelingen verrichten, mits hij of zij elk kwartaal getest wordt op HBsAg, waarbij de uitslag negatief moet zijn. Als HBsAg positief blijkt, moeten onmiddellijk alle risicovormende handelingen gestaakt worden.
NB-1: hier wordt niet bedoeld een seroconversie naar positieve anti-HBcore, zie daarvoor 2.7.
NB-2: Het uitblijven van een anti-HBs response na vaccinatie van een persoon met geïsoleerd positieve anti-HBcore betekent niet dat de anti-HBcore reactiviteit ‘dus’ fout-positief is.
Bij het volgende serologische profiel is naar alle waarschijnlijkheid sprake van doorgemaakte, genezen HBV-infectie, met immuniteit: HBsAg is niet aantoonbaar, terwijl anti-HBs en anti-HBcore antistoffen beide aantoonbaar zijn. In deze situatie wordt men beschouwd als levenslang immuun en is revaccinatie niet nodig; risicovormende handelingen zijn toegestaan.
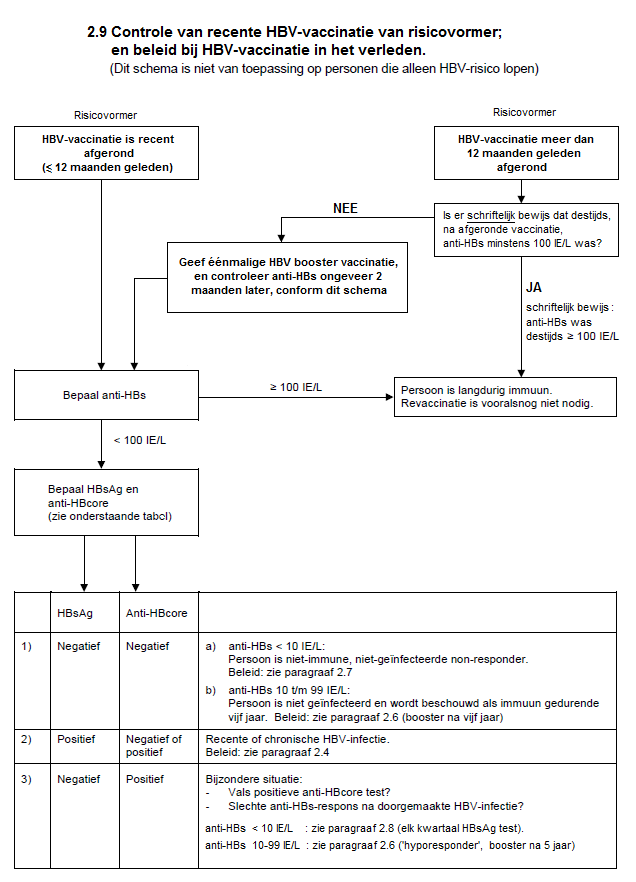
2.9 Controle van recente HBV-vaccinatie van risicovormer; en beleid bij HBV-vaccinatie in het verleden
2.10 Kwaliteitseisen en gevoeligheid bij kwantitatieve bepaling van HBV-DNA
- De afname, verwerking en verzending van een bloedmonster voor bepaling van de mate van HBV-viremie (kwantitatieve bepaling van HBV-DNA), en de rapportage van de uitslag, moeten geschieden niet door de betrokken medewerker zelf, maar onder de verantwoordelijkheid van bijvoorbeeld een bedrijfsarts, arts-microbioloog, hepatoloog of internist-infectioloog. Hierbij moet ook rekening worden gehouden met de geldende privacywetgeving . Afspraken over infectiepreventie dienen geborgd te worden in het lokale instellingsbeleid, in samenspraak met de bedrijfsarts of arbodienst.
- De HBV-DNA-bepaling dient te worden uitgevoerd in een Nederlands geaccrediteerd medisch-microbiologisch laboratorium, met behulp van een CE-gemarkeerde, commercieel verkrijgbare test. Uitvoering van de test dient uitgevoerd te worden volgens een door de verantwoordelijk leidinggevende goedgekeurde schriftelijke ‘standard operating procedure’ (‘SOP’).
- Het uitvoerend laboratorium dient minstens éénmaal per jaar deel te nemen aan blinde kwaliteitsrondzendingen van HBV-DNA en hierin goede resultaten te behalen.
- De PCR-test voor de bepaling van aan- of afwezigheid van HBV-infectie moet een minimale gevoeligheid van 20 IU/mL HBV-DNA hebben.
3. Consequenties voor HBV-geïnfecteerde risicovormers
Aanwezigheid van HBV-infectie kan gevolgen hebben voor de beroepsuitoefening. De minst vergaande consequentie is de periodieke controle bij de gezondheidszorgwerker van het HBV-DNA-gehalte. Indien initieel hoogstens 1000 IU/mL HBV-DNA werd aangetoond, kan de gezondheidszorgwerker zijn beroep blijven uitoefenen zolang de HBV-DNA load laag blijft.
Indien bij een gezondheidszorgwerker meer dan 1000 IU/mL HBV-DNA wordt aangetoond, mogen geen risicovormende handelingen meer worden verricht. Gelukkig maakt in de meeste gevallen het instellen van onderhoudstherapie met moderne antivirale middelen de hervatting van het risicovormende werk mogelijk, doordat aanzienlijk daling van HBV-DNA optreedt door de behandeling. Zonder succesvolle behandeling van een HBV-infectie kan het nodig zijn om de beroepsuitoefening te beperken of zelfs te stoppen, omdat het beroep niet uitgevoerd kan worden zonder risicohandelingen te verrichten. Een complicerende factor is dat met name private instellingen strengere eisen mogen stellen aan werknemers met betrekking tot geschiktheid voor het uitvoeren van risicohandelingen.
3.1 Beroepskeuze
De behandelmogelijkheden voor HBV-dragers zijn sterk verbeterd sinds de registratie van krachtige HBV-remmers met weinig resistentievorming. Op het eerste gezicht lijkt dit de keuze voor een beroep met risicohandelingen te vergemakkelijken voor HBV-geïnfecteerden. Hierbij is echter sprake van verschillende bezwaren.
Bij deze richtlijn is gekozen voor een benadering waarin de kans op besmetting van een patiënt door een HBV-dragende gezondheidszorgwerker minimaal maar niet nul is (zie hoofdstuk 5). Hierbij zijn de belangen van HBV-geïnfecteerde professionals meegewogen.
Met betrekking tot personen die nog een beroep moeten kiezen, is het advies een zorgvuldige afweging te maken. In geval van HBV-dragerschap past, in verband met de betrokken risico’s, terughoudendheid bij de keuze voor en toelating tot een opleiding tot een risicovormend beroep, ook indien er sprake is van lage viremie.
Lokaal kan een strenger beleid gelden dan beschreven in deze richtlijn. Bijvoorbeeld vanwege de aansprakelijkheid, kan een opleider of opleidende instelling uitgaan van een nul-risico voor de patiënt, en dus een strenger beleid toepassen. Deze richtlijn verschaft aan laag-viremische HBV-dragers niet het recht tot opleiding in een risicovormend beroep. Een medische faculteit kan echter een HBV-geïnfecteerde (kandidaat)geneeskundestudent niet weigeren vanwege de HBV-infectie, er zijn immers vele niet-risicovormende medische specialismen (zie paragraaf 3.2). Ten slotte kunnen in de toekomst nieuwe inzichten of Europese voorschriften leiden tot het van kracht worden van een strenger beleid dan beschreven in deze richtlijn.
Het uitoefenen van verloskunde, tandheelkunde, orthodontie en mondhygiëne omvat per definitie risicovolle handelingen. Deze beroepen zijn dus niet verenigbaar met hoog-viremische HBV-infectie. Personen met chronische HBV-infectie worden geadviseerd terughoudend te zijn om voor deze beroepen te kiezen. Dat geldt ook voor personen met spontane lage viremie of met lage viremie onder antivirale therapie.
3.2 Medische studenten met HBV-infectie
De HBV-status van medische studenten moet in het eerste studiejaar, na vaccinatie, worden vastgesteld. Geborgd dient te worden dat een medische student met hoog-viremische HBV-infectie tijdens de studie niet in een situatie terecht komt waarbij risicovolle handelingen verricht moeten worden. Dit is een gedeelde verantwoordelijkheid van de medische faculteit en de geïnfecteerde student. In principe moet een arts met HBV-infectie een specialisatie zonder risicovolle handelingen kiezen, ook al is er sprake van lage viremie. Er zijn veel medische specialismen zonder risicovolle handelingen. Een student met HBV-infectie moet geneeskunde kunnen studeren.
3.3 Opleidingsvoorwaarden
Voor beroepsbeoefenaren die risicovormende handelingen verrichten zijn de consequenties van de richtlijn ingrijpend, wanneer tijdens hun loopbaan blijkt dat zij HBV-drager zijn. Voor nieuw op te leiden risicovormers is het ongewenst dat zij tijdens opleiding of loopbaan met mogelijk ingrijpende consequenties geconfronteerd worden. Het lijkt juist om in deze situatie voor een nog hogere veiligheid van de patiënt te kiezen.
Voorafgaand aan elke opleiding tot een risicovormend beroep moet daarom de (documentatie van de) HBV-(immuun)status van de betrokkene gecontroleerd worden. Het is ongewenst om HBV-dragers op te leiden tot een beroep met risicohandelingen, ook al is er sprake van lage viremie. Wat betreft non-responders dient de beroepskeuze heroverwogen te worden, vanwege de mogelijkheid om geïnfecteerd te raken en de voortdurende noodzaak tot controle op HBV-infectie (zie 2.7).
4. Onderbouwing van de HBV-DNA grenswaarde van 1000 IU/mL
In dit hoofdstuk wordt aangegeven op welke basis de adviezen ter preventie van iatrogene HBV-besmetting tot stand kwamen.
Er is gekozen voor een benadering waarin de kans op besmetting van een patiënt door een HBV-dragende gezondheidszorgwerker minimaal en dus niet nul is. Een geringe mate van HBV-viremie bij risicovormers is toegestaan. Het lijkt namelijk dat vooral de mate van viremie bepalend is voor de kans op virusoverdracht. Hoe hoger de viral load, des te groter wordt de kans op overdracht. Uit de literatuur blijkt dat het merendeel van de gerapporteerde transmissies voorkomt bij hoog-viremische personen, namelijk bij zogenaamd ‘e-antigeenpositieve’ HBV-dragers en bij zeer recent geïnfecteerde personen (3,9,12). Bij e-antigeenpositieve HBV-dragers bedraagt de virus load in de regel minstens 107 HBV-DNA kopieën/mL (13-16). (Voor ‘kopieen’ HBV DNA: zie voetnoot 1).
In de voorgaande edities van deze Richtlijn was sprake van een –internationaal gezien- relatief hoge grenswaarde van HBV-viremie van 20.000 IU/mL, waarboven geen risicohandelingen verricht mochten worden. De onderbouwing hiervan was enerzijds de waarneming dat slechts hoge viremieën leidden tot transmissie naar de patient (zie voetnoot 2), en dat een lage grenswaarde tot relatief veel beroepsuitsluiting zou leiden. Inmiddels is ruime ervaring opgebouwd bij risicovormers met onderdrukking van HBV-viremie door HBV-remmers als tenofovir en entecavir.
In maart 2020 bleken alle HBV-geïnfecteerde risicovormers die werden gecontroleerd, met of zonder antivirale behandeling, een beduidend lagere viremie te vertonen dan de oude grenswaarde van 20.000 IU/mL. Men concludeerde daarop dat een verlaging van de maximaal toegestane HBV-viremie naar 1000 IU/mL de veiligheidsmarge voor patienten vergroot, zonder dat beroepsbeperkingen opgelegd moeten worden aan risicovormers. De huidige richtlijn stelt daarom de grenswaarde waarboven geen risicohandelingen mogen worden uitgevoerd op 1000 IU/mL HBV-DNA.
Voetnoot 1
In oudere publicaties wordt de mate van HBV-viremie uitgedrukt in HBV-DNA kopieen/mL, waarbij geldt dat vijf kopieën HBV-DNA ongeveer overeenkomen met 1 IU HBV-DNA.
voetnoot 2
In bijna alle beschreven gevallen van HBV-transmissie van arts naar een patiënt was de bron e-antigeen-positief (19), wat in de regel gepaard gaat met een viral load van minstens 107 HBV-DNA-kopieën/mL (13-16). Bij de ongeveer dertig beschrijvingen van HBV-transmissies van arts naar patiënt sinds 1970 was slechts in één geval sprake van een viral load lager dan 105 HBV-DNA-kopieën/mL (20.000 IU/mL), namelijk 6 x 104 HBV-DNA-kopieën/mL (17,18,20). Naar aanleiding van dit geval stelde het U.K. Department of Health destijds de grenswaarde voor het uitvoeren voor risicohandelingen op 103 HBV-DNA-kopieën/mL (200 IU/mL). Men achtte bij deze waarde, vanwege de spreiding in de meting van HBV-DNA en de variatie van de viral load in de tijd, een veiligheidsmarge van een factor 100 wenselijk.
5. Toelichting bij anti-HBs minimum ≥ 100 IU/L voor risicovormers
Het is niet algemeen bekend dat bij een significant deel van personen met chronische HBV-infectie naast het HBsAg ook anti-HBs aantoonbaar is. Een Nederlandse studie vond bij 10% aantoonbaar anti-HBs naast HBsAg (27). De anti-HBs titer bedraagt daarbij in de regel tussen 10 en 100 IU/L. Elders zijn vergelijkbare bevindingen gerapporteerd. Conform de (World Health Organization) is een persoon immuun als na een volledige HBV-vaccinatiereeks minstens 10 IU/L anti-HBs wordt gemeten. Als men bij serologische controle na HBV-vaccinatie ‘minstens 10 IU/L’ toepast als succescriterium, dan mist men de chronisch HBV-geïnfecteerden met gelijktijdige aanwezigheid van HBsAg en anti-HBs. Voor personen die alleen risico lopen is deze kleine foutkans acceptabel, omdat de gevolgen klein zijn. Voor risicovormers is de kleine foutkans niet acceptabel, omdat het tot een stroom van besmettingen kan leiden. Daarom stelt deze richtlijn als minimale anti-HBs response na HBV vaccinatie van risicovormers niet 10 maar 100 IU/L, met verplichte vervolgtest op HBsAg en anti-HBcore indien anti-HBs lager dan 100 IU/L blijkt te zijn.
6. Overleg met RIVM/LCI
RIVM/LCI is beschikbaar voor vragen over de Landelijke richtlijn preventie transmissie van hepatitis B virus van medisch personeel naar patiënten en RIVM/LCI kan advies geven bij individuele casuïstiek.
Contact via e-mail: commissiehbv@rivm.nl (maandag t/m vrijdag)
Contact via telefoon: 088 689 7000 (maandag t/m vrijdag van 8:30-17:00u en voor spoed ook buiten kantoortijden)
Literatuur
- Onderzoek naar een cluster van hepatitis B-virusbesmettingen in het St. Joseph Ziekenhuis te Veghel. Eindrapport. November 1999.
- Inspectierapportage hepatitis B-besmetting St. Joseph Ziekenhuis te Veghel (IGZ, 1999).
- Polakoff S. Acute hepatitis B in patients in Britain related to previous operations and dental treatment. Br Med J (Clin Res Ed) 1986; 293(6538):33-36.
- Welch J, Webster M, Tilzey AJ, Noah ND, Banatvala JE. Hepatitis B infections after gynaecological surgery. Lancet 1989; 1(8631):205-207.
- Prentice MB, Flower AJ, Morgan GM, Nicholson KG, Rana B, Firmin RK et al. Infection with hepatitis B virus after open heart surgery. BMJ 1992; 304(6829):761-764.
- Anonymous. Surgeons who are hepatitis B carriers. BMJ 1991; 303(6795):184-185.
- Harpaz R, Von Seidlein L, Averhoff FM, Tormey MP, Sinha SD, Kotsopoulou K et al. Transmission of hepatitis B virus to multiple patients from a surgeon without evidence of inadequate infection control. N Engl J Med 1996; 334(9):549-554.
- Lettau LA, Smith JD, Williams D, Lundquist WD, Cruz F, Sikes RK et al. Transmission of hepatitis B with resultant restriction of surgical practice. JAMA 1986; 255(7):934-937.
- Coutinho RA, Albrecht-van Lent P, Stoutjesdijk L, Meerburg-Snarenberg P, Courouce-Pauty AM, van Dijk BA et al. Hepatitis B from doctors. Lancet 1982; 1(8267):345-346.
- Carl M, Blakey DL, Francis DP, Maynard JE. Interruption of hepatitis B transmission by modification of a gynaecologist's surgical technique. Lancet 1982; 1(8274):731-733.
- Grob PJ, Bischof B, Naeff F. Cluster of hepatitis B transmitted by a physician. Lancet 1981; 2(8257):1218-1220.
- Haerem JW, Siebke JC, Ulstrup J, Geiran O, Helle I. HBsAg transmission from a cardiac surgeon incubating hepatitis B resulting in chronic antigenemia in four patiënts. Acta Med Scand 1981; 210(5):389-392.
- Bilkert-Mooiman MA, Daha TJ, Noordaa vdJ. Transmissie te lijf, vijf jaar preventie iatrogene hepatitis B. Medisch Contact 2006; 61(17).
- Corden S, Ballard AL, Ijaz S, Barbara JA, Gilbert N, Gilson RJ et al. (hepatitis B-virus) DNA levels and transmission of hepatitis B by health care workers. J Clin Virol 2003; 27(1):52-58.
- Tedder RS, Ijaz S, Gilbert N, Barbara JA, Corden SA, Gilson RJ et al. Evidence for a dynamic host-parasite relationship in e-negative hepatitis B carriers. J Med Virol 2002; 68(4):505-512.
- Corden S. HBV DNA levels in healty antenal carriers of Hepatitis B. 2000. Glasgow. Proceedings of Virology. 17-9-2000.
- Corden S, Ballard AL, Ijaz S, Barbara JA, Gilbert N, Gilson RJ et al. HBV DNA levels and transmission of hepatitis B by health care workers. J Clin Virol 2003; 27(1):52-58.
- The Incident Investigation Teams and others. Transmission of hepatitis B to patiënts from four infected surgeons without hepatitis B e antigen. N Engl J Med 1997; 336(3):178-184.
- Schalm SW, van Wijngaarden JK. Doctor-to-patiënt transmission of viral hepatitis B: is it a problem, is there a solution? J Viral Hepat 2000; 7(4):245-249.
- Gunson RN, Shouval D, Roggendorf M, Zaaijer H, Nicholas H, Holzmann H et al. Hepatitis B virus (HBV) and hepatitis C virus (HCV) infections in health care workers (HCWs): guidelines for prevention of transmission of HBV and (hepatitis C-virus) from HCW to patiënts. J Clin Virol 2003; 27(3):213-230.
- Spijkerman IJ, van Doorn LJ, Janssen MH, Wijkmans CJ, Bilkert-Mooiman MA, Coutinho RA et al. Transmission of hepatitis B virus from a surgeon to his patients during high-risk and low-risk surgical procedures during 4 years. Infect Control Hosp Epidemiol 2002; 23(6):306-312.
- Zaaijer HL, Lelie PN, Vandenbroucke-Grauls CM, Koot M. Concurrence of hepatitis B surface antibodies and surface antigen: implications for postvaccination control of health care workers. J Viral Hepat 2002; 9(2):146-148.
- Circulaire 'Vaccinatie Hepatitis B' van de Hoofdinspecteur voor de Preventieve en Curatieve Gezondheidszorg aan de directies van ziekenhuizen. 2000-03-IGZ. 8-3-2000.
- European Consensus Group on Hepatitis B Immunity. Are booster immunisations needed for lifelong hepatitis B immunity? Lancet 2000; 355(9203):561-565.
- Brief van de Secretaris van de Gezondheidsraad aan Hoofd Secretariaat van Landelijke Coördinatiestructuur Infectieziektebestrijding. 16-12-1997.
- (Landelijke Coördinatie Infectieziektebestrijding) Hepatitis B, mei 2008. In: Steenbergen JE, Timen A, Beaujean DJMA (red); LCI richtlijnen infectieziektebestrijding, Editie 2011. Bilthoven: LCI, Landelijke Coördinatiestructuur Infectieziektebestrijding, 2011. ISBN 978-90-6960-241-7.
- Zaaijer HL, Lelie PN, Vandenbroucke-Grauls CM, Koot M. Concurrence of hepatitis B surface antibodies and surface antigen: implications for postvaccination control of health care workers. J Viral Hepat 2002; 9(2):146-148.
- Daha TJ, Bilkert-Mooiman MA, Ballemans C, Frijstein G, Keeman JN, de Man RA, van Steenbergen JE, Weers-Pothoff G, Zaaijer HL. Hepatitis B virus infected health care workers in The Netherlands, 2000-2008. Eur J Clin Microbiol Infect Dis. 2009 Sep;28(9):1041-4.