Difterie Richtlijn
Samenvatting
Verwekker: Toxineproducerende stammen van Corynebacterium diphtheriae, of C. ulcerans of andere Corynebacterium species
Incubatieperiode: Meestal 2-5 dagen (spreiding 1-7 dagen)
Besmettingsweg: Via druppels uit de keel, via wondexsudaat (huiddifterie)
Besmettelijke periode: Max. 7 dagen voor eerste ziektedag tot 48 uur na start antibiotische therapie
Maatregelen: Meldingsplichtige ziekte groep B1. Doorgaans met name nodig bij infectie door C. diphtheriae
Symptomen: Pseudomembranen in luchtwegen of op een huidlaesie
Doel en doelgroep
Deze richtlijn is ontwikkeld voor zorgprofessionals werkzaam binnen de infectieziektebestrijding. De primaire doelgroepen zijn GGD- en LCI-professionals. De richtlijn beschrijft duidelijke adviezen, taken en verantwoordelijkheden en vormt een basis voor het nemen van geïnformeerde beslissingen en het maken van beleid in de praktijk. De zorgprofessional kan de richtlijn ook gebruiken voor het bijhouden en vergaren van kennis. De uitvoering van de richtlijn overstijgt institutionele en professionele domeingrenzen en is bedoeld voor het gebruik binnen diverse sectoren van de gezondheidszorg. Voor meer informatie zie Totstandkoming LCI-richtlijnen.
Versiebeheer
Richtlijn herzien door: Rob van Kessel (GGDrU/LCI), Loes Jaspers (GGDrU) en Madelief Mollers (LCI), met uitzondering van het hoofdstuk Diagnostiek en de arboparagrafen.
Vastgesteld LOI: 25 juni 2024.
Diagnostiek geschreven door: Frans Reubsaet (NVMM). Vastgesteld: 29 juni 2019.
Arboparagrafen herzien door: Herbert de Jager (LCI). Vastgesteld: januari 2023.
Wijzigingen:
- 30 juli 2024: Verduidelijkt dat meldingsplicht geldt voor de Corynebacteriumspecies die toxine-gendragend zijn. Figuur 3, 'Stroomschema meldingsplicht', en figuur 4, 'Stroomschema maatregelen' daarop o.a. aangepast.
- 12 juli 2024: Herziene richtlijn gepubliceerd (op 25 juni 2024 vastgesteld door het LOI). Nieuw en anders in deze richtlijn ten opzichte van de oude richtlijn:
- Belangrijkste inhoudelijke wijziging: de verwekkers zijn gescheiden in twee groepen: [1] species die (potentieel) van mens-op-mens overdraagbaar zijn C. diptherieae, C. belfantii en C. rouxii en [2] zoönotische species met als voornaamste verwekker C. ulcerans.
- Bij difterie veroorzaakt door zoönotische verwekkers zoals C. ulcerans zijn nauwelijks maatregelen nodig. Informatie over difterie veroorzaakt door deze groep verwekkers is opgenomen in bijlage 1, inclusief onderbouwing. Bijlage 1 vervangt daarmee tevens de eerdere onderbouwingsbijlage. De wetenschappelijke onderbouwing van het beperken van maatregelen bij de zoönotische species is aan de bijlage toegevoegd.
- De informatie van de paragrafen profylaxe en behandeling is bijgewerkt. Met name is veel informatie over difterie-antitoxine toegevoegd.
- De inhoudelijke informatie uit het draaiboek Difterie is verwerkt in de richtlijn. Het hoofdstuk over ‘Maatregelen’ is door het verplaatsen (en bijwerken) van informatie uit het draaiboek uitgebreider geworden. Het draaiboek Difterie is per 12 juli 2024 opgeheven.
Ziekte & Besmettelijkheid
Verwekker
Klinische difterie wordt veroorzaakt door toxineproducerende Corynebacterium diphtheriae of C. ulcerans, en heel af en toe door andere toxineproducerende Corynebacterium-species.
Tenzij nadrukkelijk anders vermeld heeft alle informatie hieronder betrekking op C. diphtheriae en andere toxineproducerende, van mens-op-mens overdraagbare Corynebacterium-species (C. belfantii of C. rouxii). Bij infecties veroorzaakt door exclusief zoönotische Corynebacterium-species C. ulcerans (en C. pseudotuberculosis en C. sylvaticum) zijn slechts zeer beperkt maatregelen nodig; hiervoor wordt verwezen naar bijlage 1.
Corynebacterium diphtheriae is een grampositieve, niet-beweeglijke staafvormige bacterie die aan één uiteinde een verdikking heeft, waardoor het beeld van een knots ontstaat (Grieks: korunè = knots). Er zijn vier biotypen (gravis, mitis, minimus of intermedius; deze typering is niet van belang voor maatregelen in de publieke gezondheid, maar helpt om stammen te onderscheiden). Alleen als de bacterie is geïnfecteerd door een bacteriofaag die het toxinegen bevat kan de bacterie het difterie-exotoxine produceren.
Definities
[1] een toxigene stam (ook wel toxinogene stam genoemd) is iedere stam die beschikt over het gen dat codeert voor het difterie-exotoxine, waarbij de stam al dan niet daadwerkelijk exotoxine produceert. In de wetenschappelijke literatuur wordt de term ‘toxigenic’ helaas op verschillende manieren gebruikt, wat tot verwarring kan leiden.
[2] een NTTB-stam is een stam die wel beschikt over het gen dat codeert voor het exotoxine, maar waarbij het gen niet tot expressie komt en waarbij de ELEK-test (toont daadwerkelijke productie van exotoxine aan) negatief is. Sommige stammen bevatten ook genen die de toxineproductie onderdrukken De Engelse afkorting NTTB staat voor: Non-Toxigenic Toxin gene-Bearing (Billard-Pomares 2017).
Pathogenese
C. diphtheriae dringt gewoonlijk alleen door in de oppervlakkige lagen van de nasofarynx en in huidlaesies. Met name het exotoxine is de oorzaak van ernstige ziekteverschijnselen. Productie van het exotoxine is afhankelijk van de aanwezigheid van een lysogene bacteriofaag die het gen draagt dat codeert voor het toxine. Het toxine remt al in zeer lage dosering de eiwitsynthese van alle eukaryotische cellen op ribosomaal niveau, wat tot celsterfte leidt. Lokaal, in de keel, bevordert het toxine necrose van het respiratoire slijmvlies met vorming van de kenmerkende pseudomembranen (in de vervolgtekst als ‘membraan’ aangeduid). De membranen bestaan uit leukocyten, celdebris, bacteriën en fibrine. Het toxine diffundeert tevens naar de bloed- en lymfebanen en bereikt zo alle weefsels en organen. De hartspier, zenuwen en niertubuli zijn het meest gevoelig voor het toxine. Stammen van C. diphtheriae die geen exotoxine produceren kunnen wel lokale ziekteverschijnselen veroorzaken, inclusief het op pseudomembranen lijkende beslag, maar geven geen afwijkingen op afstand (myocarditis, neuritis, acute tubulusnecrose).
Incubatieperiode
De incubatieperiode duurt meestal 2-5 dagen (spreiding: 1 tot 7 dagen). Truelove (Truelove 2020) schat op basis van systematisch literatuuronderzoek het mediane tijdsinterval tussen besmetting en het begin van prodromale verschijnselen op 1,4 dagen (95%-betrouwbaarheidsinterval: 1,0–1,9).
Ziekteverschijnselen
Na besmetting volgt asymptomatisch dragerschap of een infectie met een variabel klinisch verloop, variërend van subklinisch tot een snel fatale afloop. Difterie is een acuut ziektebeeld dat vooral klachten en verschijnselen veroorzaakt in de farynx en omringende structuren, of de huid en, alleen in zeldzame gevallen, op andere locaties. Er kan dan ook onderscheid gemaakt worden in respiratoire difterie, cutane difterie en andere vormen. Op de CDC-website is beeldmateriaal van zowel cutane als respiratoire difterie beschikbaar.
Respiratoire difterie
Neusdifterie
Begint meestal unilateraal met eerst dun, later purulent, bloederig slijm uit de neus. Soms zijn witte membranen zichtbaar, voornamelijk op het neustussenschot. Excoriaties op de neusvleugels en de bovenlip kunnen optreden. Het verloop is meestal mild, zonder koorts of complicaties door het toxine.
Keeldifterie
Dit is de meest voorkomende uiting van de ziekte en deze begint vaak abrupt met forse keelpijn, hangerigheid en een lichte temperatuurverhoging (38ºC). Bij inspectie in de keel is een milde tonsillitis, uni- of bilateraal, met daarop een vanaf de tweede dag beginnend grijs-wit vastzittend beslag (pseudomembraan) zichtbaar. Na een paar dagen wordt het beslag donkergrijs met groene of zwarte necrotische plekken en kan het foetor ex ore veroorzaken. Het pseudomembraan kan niet zonder bloeden verwijderd worden. Verdere uitbreiding naar zachte verhemelte en uvula is mogelijk, wat gepaard gaat met toename van malaise en lokale klachten. Door oedeem in het nek-halsgebied en lokale lymfeklierzwelling ontstaat de zogenaamde ‘burgemeestersnek’ met een ernstige inspiratoire stridor.
Larynxdifterie (“kroep”)
De keeldifterie kan zich uitbreiden naar de larynx, leidend tot heesheid, benauwdheid en een inspiratoire stridor. De patiënt heeft een rode oedemateuze farynx en is algemeen ziek met cyanose, sufheid en delirium. Dit ziektebeeld komt vooral voor bij kinderen onder de leeftijd van 4 jaar. De patiënt is angstig en gebruikt de hulpademhalingsspieren. Intubatie en verwijdering van het membraan zijn essentieel voor overleving.
Cutane difterie (huiddifterie)
De bacterie kan de intacte huid niet binnendringen. Na binnendringen door de beschadigde huid ontstaan typische laesies in de vorm van ronde, diep uitgeponste ulcera (van een halve tot meerdere centimeters doorsnede), bedekt met een grijsgeel tot grijsbruin membraan. Bij cutane difterie door stammen die het exotoxine produceren treden slechts zelden toxische verschijnselen op (en dan meestal neuritis). Cutane difterie kan voorkomen bij volledig gevaccineerde personen.
Andere lokalisaties
Infecties van conjunctiva, oor (acute of chronische otitis media) of genitalia komen zelden voor.
Complicaties
Bij difterie kan men twee typen complicaties onderscheiden: lokale complicaties door membranen en oedeem en systemische complicaties als gevolg van het toxine. Toxische cardiomyopathie treedt 7-14 dagen na het begin van de ademhalingssymptomen bij 10%-25% van de patiënten op en is verantwoordelijk voor 20-25% van de sterfgevallen. Neurologische aandoeningen, zoals hypo-esthesie, polyneuropathie en craniale neuropathieën, ontwikkelen zich weken tot maanden later en komen voor in 20-25% van de onbehandelde gevallen en zijn verantwoordelijk voor maximaal 15% van de sterfgevallen (Truelove 2020).
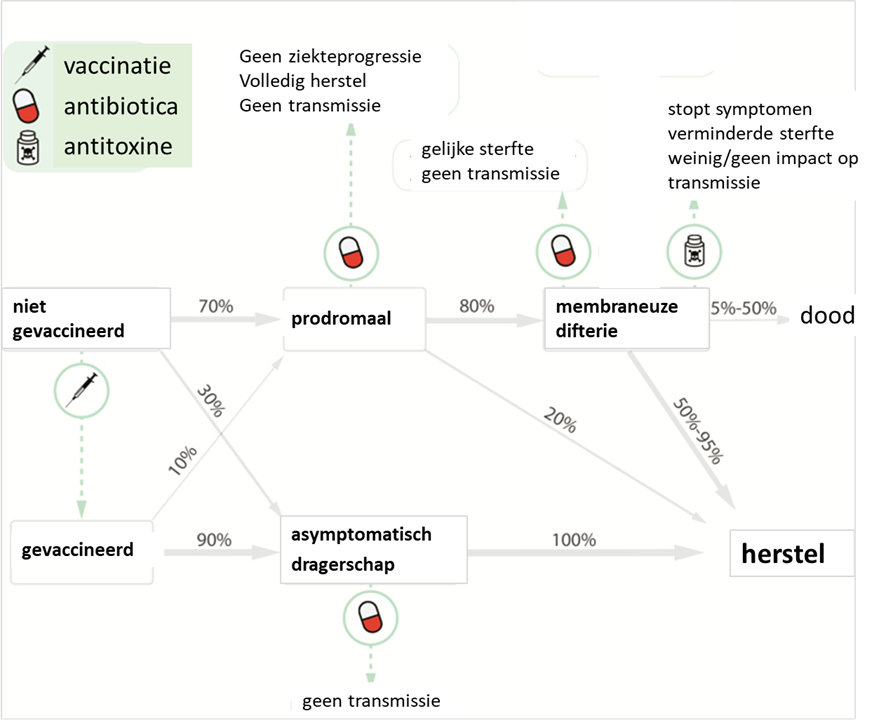
Figuur 1. Natuurlijk verloop van difterie met de effecten van preventieve en behandelingsinterventies (ontleend aan Truelove (Truelove 2020)).
Arbo
Ziekteverschijnselen in relatie tot arbeid
Bij klinische respiratoire difterie is iemand doorgaans te ziek om te werken. Bij cutane difterie is de patiënt doorgaans veel minder ziek en zou iemand in veel gevallen kunnen werken. Er zijn echter wél beperkingen op grond van de besmettelijkheid voor derden (zie onder Maatregelen).
Natuurlijke immuniteit
De belangrijkste afweer bestaat uit aanwezigheid van antistoffen (hoofdzakelijk IgG) in het bloed tegen het toxine (antitoxine). De verschillende corynebacteriën produceren een identiek toxine. Door het (ook asymptomatisch) doormaken van de infectie (keel of huid) of via vaccinatie met toxoïd ontstaat meestal immuniteit. Een natuurlijke infectie leidt niet altijd tot het ontstaan van antitoxine en geeft dus niet altijd blijvende immuniteit. Antitoxische immuniteit beschermt tegen de systemische verschijnselen, maar niet tegen lokale kolonisatie of infectie.
Zwangerschap
Natuurlijke immuniteit bij zuigelingen
Een pasgeborene is, afhankelijk van de immuunstatus van de moeder, uiterlijk tot de leeftijd van 6 maanden beschermd door transplacentaire overdracht van antistoffen en in geringe mate door secretoir IgA in moedermelk.
Reservoir
Het reservoir van C. diphtheriae is uitsluitend de mens. In endemische gebieden (zie eventueel: https://immunizationdata.who.int/) heeft 3-5% van de bevolking de bacterie periodiek in de keel of op de huid. In landen waar de vaccinatiegraad hoog is, zoals in Nederland, is dit percentage vermoedelijk vrijwel nihil.
Besmettingsweg
Direct
C. diphtheriae is van mens op mens overdraagbaar. De bacterie verspreidt zich via druppeltjes uit de neus-keelholte, zoals bij hoesten en niezen, via direct contact (bijv. zoenen) of via direct contact met wondexsudaat. Het contact met de bron moet op korte afstand plaatsvinden (enkele meters) en herhaaldelijk optredend contact, zoals in gezinnen en instellingen, of langdurig contact (slaapkamer) verhoogt de kans op besmetting.
Indirect
Besmetting via voorwerpen komt soms voor als gevolg van contaminatie van de omgeving van de patiënt door ingedroogde druppeltjes of wondexsudaat (Harnisch 1989).
Zwangerschap
Relevante transmissieroutes bij zwangeren
Het is niet bekend of het toxine de placenta kan passeren.
Besmettelijke periode
Een patiënt is in ieder geval besmettelijk vanaf het begin van de klachten. Besmettelijkheid is circa 48 uur na starten van een werkzame antibiotische behandeling verdwenen. Onbehandeld kunnen bij patiënten nog enkele weken infectieuze bacteriën aangetoond worden. Asymptomatische dragers spelen ook een rol bij de verspreiding van C. diphtheriae, maar overdracht is effectiever bij symptomatische patiënten.
Besmettelijkheid
De schaarse wetenschappelijke informatie over de besmettelijkheid van difterie stamt vooral uit de jaren ’60 en ’70 van de 20e eeuw, waarin de ziekte ook in westerse landen nog regelmatig voorkwam. C. diphtheriae wordt gedood door verhitting op 58oC gedurende 10 minuten alsmede door de meeste desinfectantia. De bacterie is betrekkelijk goed bestand tegen uitdroging en kan wekenlang – nog infectieus – in de directe leefomgeving van de patiënt worden geïsoleerd (Christie 1987).
Bij een analyse van 23 difterie-uitbraken varieerde het effectieve reproductiegetal R tijdens de initiële groeifase van de uitbraken van 1,1 tot 3,2 (Truelove 2020). Het basale reproductiegetal R0 varieerde in deze studie van 1,7 tot 4,3 (mediaan, 2,6). De onderzoekers schatten dat het seriële interval voor difterie (dwz de tijd tussen het begin van de symptomen in opeenvolgende gevallen van overdracht) op 7,8 dagen (95% CI, 6,3-9,7 dagen) met 5% van de intervallen <0,8 dagen en 5% langer dan 21 dagen (Truelove 2020). In een studie onder ziekenhuiscontacten van patiënten met difterie werd in 533 swabs bij 328 personen geen enkele positieve kweek van C. diphtheriae gevonden (Larsson 1987).
Diagnostiek
Met medewerking van de NVMM. Vastgesteld 29 juni 2019.
Microbiologische diagnostiek
| Het is noodzakelijk vóór inzending het laboratorium op de hoogte te stellen, omdat materiaal bij voorkeur op speciale platen moeten worden geënt, die over het algemeen niet bij laboratoria standaard aanwezig zijn. Zie bijlage Laboratoriumonderzoek voor de juiste procedure voor afname en opsturen van diagnostisch materiaal. |
Directe diagnostiek
De verwekkers van difterie groeien op zich goed op niet-selectieve voedingsbodems, zoals bloed- en chocolade-agars, maar zijn soms tussen commensale flora lastig te herkennen. Voor primaire isolatie kan gebruik gemaakt worden van selectieve, telluriethoudende media, zoals Hoyle’s medium, Clauberg-plaat en/of Tinsdale-medium (cysteine-telluriet). C. diphtheriae-kolonies zijn grijs-zwart van kleur, en op de Tinsdale-agar vertonen zij een bruine halo. De platen kunnen worden afgelezen na 18-24 uur incubatie bij 37°C. Een atmosfeer van 5-10% CO2 bevordert de groei, maar remt de halovorming.
C. diphtheriae kan goed geïdentificeerd worden met maldi-tof. C. ulcerans en C. pseudotuberculosis zijn met maldi-tof en 16S rRNA gen sequencen niet goed van elkaar te onderscheiden. Daarvoor zijn aanvullende biochemische testen nodig.
Toxinebepaling
Het is van belang om na isolatie van Corynebacterium-stammen vast te stellen of ze het difterietoxine produceren. Daartoe kunnen kweken voor confirmatie en aantonen van toxinevorming worden gestuurd naar het RIVM. Stuur bij voorkeur een originele plaat in of een afenting van meerdere kolonies (zie bijlage Laboratoriumonderzoek voor de juiste procedure).
Het RIVM heeft een PCR beschikbaar, waarmee het toxinegen kan worden aangetoond. Deze uitslag kan binnen 1 dag bekend zijn. Of de stam daadwerkelijk toxine produceert wordt vervolgens getest met behulp van immunodiffusie en precipitatie in agar (Elektest). Deze test duurt een paar dagen en is niet altijd conclusief, wanneer de controles geen eenduidig resultaat geven. Als een stam wel het toxinegen bevat, maar geen aantoonbaar toxine produceert, wordt dit aangeduid met NTTB (non-toxigenic toxin gene bearing) (zie Maatregelen).
Indirecte diagnostiek
Bij het RIVM CIb-IDS kunnen antistoffen tegen het toxine bepaald worden in serum voor het vaststellen van de immuunstatus. De test is niet gevalideerd om de diagnose difterie te stellen. Naar WHO-criteria worden toxine-antistofconcentraties onder 0,01 IU/ml beschouwd als niet beschermend; antistofconcentraties vanaf 0,01 IU/ml geven enige bescherming; concentraties vanaf 0,1 IU/ml worden als volledig beschermend beschouwd.
Typering voor bron- en contactonderzoek
n.v.t.
Risicogroepen
Verhoogde kans op infectie
Niet- of onvolledig gevaccineerde personen lopen een verhoogde kans op een infectie met C. diphtheriae als zij reizen naar of afkomstig zijn uit gebieden waar difterie endemisch of epidemisch voorkomt.
Arbo
Arbeidsgerelateerde risicogroepen
Werkgebonden overdracht is mogelijk bij de volgende beroepsgroepen:
- Laboratoriumpersoneel en onderzoekers die gericht werken met de bacterie of besmet materiaal (Wright 2009);
- Gezondheidzorgwerkers die een patiënt onderzoeken/verzorgen/verplegen;
- Werknemers die in aanraking komen met mensen die afkomstig zijn uit landen waar difterie endemisch of epidemisch voorkomt. Hetzij in de Nederland (zoals vluchtelingen (ECDC 2022)), hetzij in het buitenland.
Verhoogde kans op ernstig beloop
De letaliteit is hoger bij kinderen onder de leeftijd van 5 jaar (Truelove 2020) en bij niet of onvolledig gevaccineerde personen.
Zwangerschap
Verhoogd risico bij zwangerschap
Hierover is in de literatuur geen specifieke informatie beschikbaar.
Epidemiologie
Verspreiding in de wereld
Difterie komt over de hele wereld voor als kinderziekte. In landen waar de vaccinatiegraad tegen difterie (onderdeel van het Expanded Programme on Immunisation, EPI) hoog is, is difterie hoofdzakelijk een importziekte die niet tot verdere verspreiding leidt (Galazka 2000, 2000). Aangenomen wordt dat een vaccinatiegraad van ten minste 70% onder kinderen nodig is om clusters van difterie te voorkómen; groepsimmuniteit ontstaat bij een vaccinatiegraad boven de 80-85%. In ontwikkelingslanden met lagere vaccinatiegraad zouden huidinfecties met C. diphtheriae een rol spelen bij het ontwikkelen van een natuurlijke bescherming tegen respiratoire difterie (Galazka 2000).
In 1990 ontstond een grote epidemie in het Gemenebest van Onafhankelijke Staten (GOS, het huidige Rusland en omringende landen) en de Baltische Staten, die in 1994-1995 haar hoogtepunt bereikte. In 1995 waren in het gehele gebied 50.425 ziektegevallen geregistreerd, veelal volwassenen, met een gemiddelde incidentie van 17/100.000 (Dittmann 2000). De belangrijkste oorzaken van deze epidemie waren een afgenomen vaccinatiegraad onder kinderen en een verminderde bescherming onder volwassenen door gebrek aan natuurlijke boostering in de jaren ervoor. Deze epidemie leidde in de jaren ‘90 tot meerdere importgevallen in West-Europese landen (niet in Nederland), maar zonder significante verdere verspreiding. In de periode 2016-2020 werden in de EU/EEA in totaal 128 gevallen van difterie door infectie met C. diphtheriae gerapporteerd (variërend van 15-39 gevallen per jaar) (ECDC 2022). Tussen 2000 en 2021 werden jaarlijks gemiddeld ruim 8000 difteriegevallen gemeld aan de WHO (door C. diphtheriae en andere Corynebacterium-species; onderscheid is hier niet mogelijk), waarvan ongeveer tweederde afkomstig van Zuidoost-Aziatische landen (WHO 2022). Recente difterie-uitbraken werden voornamelijk gezien in de context van humanitaire crises: in Bangladesh, Jemen en Venezuela. Sinds 2022 is in meerdere Europese landen sprake van een toename van het aantal difteriegevallen onder migranten (ECDC 2022).
Voorkomen in Nederland
De laatste epidemieën hebben zich in Nederland eind jaren ’30 en in de Tweede Wereldoorlog voorgedaan. In 1952-1953 werd begonnen met een landelijk systematische vaccinatie van zuigelingen tegen difterie (en kinkhoest). Tegenwoordig komt difterie door toxigene C. diphtheriae sporadisch voor als importziekte na blootstelling in landen waar difterie nog endemisch is, of door besmetting met toxigene C. ulcerans via (huis)dieren. Tussen 2011-2021 werden in totaal 18 difteriegevallen gemeld, met een jaarlijkse range van 0-4 en waarvan de helft een besmetting met toxigene C. ulcerans betrof (Elsinga 2023). Het ging met name om cutane difterie (17/18). In 2022 zijn in totaal 7 C. diphtheriae-gevallen gemeld, waarvan 5 bij immigranten. In 2023 zijn in totaal 14 meldingen gedaan, waarvan 13 immigranten. De vaccinatiestatus van de immigranten is onbekend. Niet-toxigene C. diphtheriae-infecties doen zich met enige regelmaat voor. Tussen 2000-2021 ontving het CIb/IDS respectievelijk 31 en 89 humane C. ulcerans- en C. diphtheriae-isolaten om te testen voor de aanwezigheid van het toxigeniciteitsgen. Hiervan werden 18 isolaten positief getest (Elsinga 2023).
Arbo
Meldingen van beroepsgerelateerde infecties
In 2015 is 1 melding van difterie als beroepsgerelateerd geregistreerd bij het RIVM (Osiris). Dit was ook de enige melding aan het Nederlands Centrum voor Beroepsziekten in de periode 1997-2023.
Preventie
Immunisatie
Actieve immunisatie
De belangrijkste pijler van preventie van difterie is bescherming tegen de gevolgen van het toxine is de actieve immunisatie via het Rijksvaccinatieprogramma: door voldoende hoge immuniteit in de bevolking wordt de verspreiding van toxigene stammen voorkomen. Immunisatie geschiedt met toxoïdvaccin. Vaccinatie tegen difterie wordt sinds 1953 aangeboden en is sinds 1957 onderdeel van het Rijksvaccinatieprogramma. Rekruten kregen sinds 1959 toxoïd bij opkomst voor militaire dienst.
Aangezien het toxine van C. ulcerans vrijwel identiek is aan het toxine van C. diphtheriae, wordt ervan uitgegaan dat vaccinatie tegen difterie ook bescherming biedt tegen het toxine van C. ulcerans-infecties.
In een sero-epidemiologische studie (Swart 2016) had 91% van de geteste populatie (N=6383) antilichaamniveaus tegen het toxine van meer dan 0,01 IE/ml vergeleken met 88% in 1995/1996 (p<0,05). De groepsimmuniteit neemt af met de leeftijd (figuur 2) Door het grote bereik van het RVP in Nederland (Lier 2023) is een voldoende grote groepsimmuniteit ontstaan, waardoor import van toxineproducerende stammen uit het buitenland in principe niet tot verspreiding leidt.
Voor meer informatie over de (combi)vaccins en hun specificaties: zie Rijksvaccinatieprogramma. Op de website van LCR is voor abonnees via ‘Mijn LCR’ het LCR-protocol ‘Difterie, Tetanus, Poliomyelitis, Kinkhoest’ beschikbaar. De publiekswebsite van LCR geeft slechts beperkte informatie.
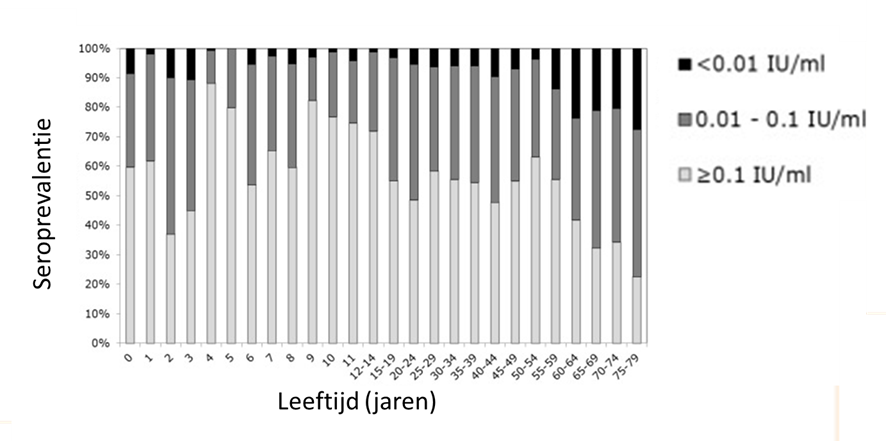
Figuur 2. Gewogen leeftijdsspecifieke seroprevalenties (%) van difterie-antistoffen in een nationale steekproef in de PIENTER-serosurvey van 2006/2007 (n = 6383) (Swart 2016).
Passieve immunisatie
Passieve immunisatie wordt alleen therapeutisch toegepast. Vanuit het oogpunt van preventie is er geen indicatie voor passieve immunisatie. Zie verder bij Behandeling.
Arbo
Vaccinatie voor werknemers
De beschermingsgraad voor difterie is in Nederland relatief hoog: 88% (Melker 2001). Werknemers die voor het uitoefenen van hun werkzaamheden nauw en intensief contact hebben met bezoekers/patiënten/cliënten uit endemische of epidemische gebieden lopen, indien niet of onvoldoende of langer dan 10 jaar geleden gevaccineerd, risico. Aan hen dient (re)vaccinatie te worden aangeboden (Gezondheidsraad 2014). Vaccinatie is ook geadviseerd bij gericht werken met C. diphtheriae. Zakelijke reizigers en expats die regelmatig of gedurende een langere periode verblijven in endemische landen wordt 10-jaarlijkse revaccinatie aanbevolen.
Algemene preventieve maatregelen
Preventieve maatregelen bij difterie zijn erop gericht verspreiding van toxigene stammen van de bacterie tegen te gaan, en nieuwe ziektegevallen (bij ongevaccineerden) te voorkomen. Er kan hier worden verwezen naar algemene adviezen ter preventie van luchtweginfecties. In het geval van respiratoire difterie wordt geadviseerd om bij verpleging of afname van een keelkweek een ademhalingsbeschermingsmasker (chirurgisch mondmasker IIR), een spatbril en handschoenen te dragen (tot 48 uur na laatste antibiotica). In het geval van cutane difterie is het advies om bij wondverzorging contactisolatie toe te passen: handhygiëne, handschoenen en halterschort; verder de wond afdekken met absorberend verband ter voorkoming van lekkage. Mocht er kleding / handdoeken in aanraking zijn geweest met wondvocht is een aanbeveling om dit te wassen op 60 graden.
Zwangerschap
Preventieve maatregelen bij zwangeren
Geen specifieke maatregelen.
Preventieve maatregelen op het werk
Het geven van periodieke, eenduidige voorlichting over het besmettingsrisico, de transmissieweg en het belang van consequente toepassing van de geldende hygiëne- en beschermende maatregelen. Daarnaast dient toezicht te zijn op het juist toepassen van de voorgeschreven maatregelen.
Het vastleggen van de vaccinatiestatus van werknemers in risicoberoepen dient bij voorkeur centraal te gebeuren. Het aanbieden van (re)vaccinatie wanneer geïndiceerd (afhankelijk van risico op blootstelling en beschermingsduur van het vaccin). Indien er sprake is van onbeschermd nauw contact dan dient de werknemer de gebruikelijke acties, die bij bron- en contactonderzoek horen, te volgen.
Desinfectie
Conform de richtlijn Standaardmethoden reiniging, desinfectie en sterilisatie in de openbare gezondheidszorg.
Maatregelen
Meldingsplicht
Difterie is een meldingsplichtige ziekte groep B1. De meldingsplicht geldt voor alle Corynebacterium-species die toxine-gendragend zijn (ook de zoönotische species).
Difterie moet worden gemeld:
- Bij vermoeden van difterie volgens onderstaande criteria.
- Na vaststelling van difterie volgens onderstaande criteria.
Het laboratorium waar de desbetreffende ziekteverwekker is vastgesteld en de behandelend arts dienen dit binnen 24 uur te melden aan de GGD (dus ook in het weekend). De GGD meldt binnen 24 uur anoniem via Osiris aan het CIb. Daarnaast neemt de GGD bij respiratoire difterie binnen 24 uur telefonisch contact op met LCI (dus ook in het weekend).
Difterie is de enige infectieziekte uit groep B van de Wet publieke gezondheid (Wpg) die reeds bij vermoeden moet worden gemeld. Een vermoedelijk geval kan worden gedefinieerd als een persoon met een passend klinisch beeld zoals bedoeld onder [1] of [2] hieronder EN een epidemiologische link (bijvoorbeeld voorafgaand bezoek aan een endemisch gebied) door mens-op-menstransmissie, maar (nog) zonder laboratoriumbevestiging van bacterie of toxigeniteit van C. diphtheriae of een van de andere de mens-op-mens overdraagbare Corynebacterium-species.
Als zich een (vermoedelijk) geval van respiratoire difterie voordoet in een populatie met lage vaccinatiegraad, dan neemt de GGD onverwijld telefonisch contact op met de LCI. Alleen in een dergelijke populatie is er een klein maar reëel risico op een uitbraak. Omdat een dergelijke uitbraak zich over meerdere GGD-werkgebieden kan (gaan) uitstrekken ligt de coördinatie van de bestrijding bij de LCI.
Voor niet-toxigene stammen geldt geen meldingsplicht en er zijn ook geen maatregelen op het gebied van de publieke gezondheid nodig.

Figuur 3. Stroomschema meldingsplicht
Meldingscriterium
[1] Elke persoon, met of zonder klachten bij wie in het laboratorium de aanwezigheid van Corynebacterium sp. is vastgesteld EN de PCR bij de gevonden Corynebacterium sp. positief is voor het toxinegen.
[2] Elke persoon met een epidemiologische link met een persoon uit groep [1] EN ten minste één van de volgende klinische beelden:
Respiratoire difterie
Ziekte van de bovenste luchtwegen met koorts en tenminste één van de volgende symptomen:
- Een pseudomembraan op ten minste één van de volgende locaties: tonsillen, farynx en/of neus.
- Laryngotracheobronchitis (kroep)
- Uni- of bilaterale bloederige afscheiding uit de neus.
Difterie van de huid of van slijmvliezen (anders dan in de luchtwegen)
Tenminste één van de volgende symptomen:
- Huidlaesie (zie het hoofdstuk over klinische verschijnselen).
- Laesie van conjunctiva of andere slijmvliezen buiten de luchtwegen.
N.B. Omdat de antitoxinebepaling (antistoffen) bij het RIVM niet geschikt is voor aantonen van een difterie-infectie (zie hoofdstuk Diagnostiek) is vaststellen van een ten minste viervoudige stijging van de serumantitoxinetiter ongeschikt als criterium voor melding. Daarbij komt nog dat wachten op de uitslag van de tweede bepaling van het serumpaar tot ongewenst uitstel van de behandeling en de bestrijding kan leiden.
N.B. De maatregelen zoals hieronder beschreven hebben betrekking op alle Corynebacterium-species die van mens op mens kunnen worden overgedragen. Waar C. diphtheriae staat worden tevens de andere species met deze transmissieroute bedoeld (zie: Verwekker).
Bij difterie op een andere locatie in het lichaam dan de luchtwegen doet de GGD onderzoek bij de patiënt naar de aanwezigheid van dragerschap in de keel. Dit is van belang voor de te nemen maatregelen.
De GGD neemt bij een sporadische melding van difterie pas actief maatregelen als de PCR voor het toxinegen positief is. In gevallen waarbij de PCR niet kan worden uitgevoerd, of als er mogelijk sprake is van een uitbraak overlegt de GGD met LCI over het te voeren beleid.
Voor gevallen van difterie die zich voordoen bij asielzoekers wordt verwezen naar de aparte bijlage over dit onderwerp. In deze setting zijn extra maatregelen nodig die zijn toegesneden op de setting.
Alle maatregelen die hieronder worden beschreven hebben uitsluitend betrekking op infecties die worden veroorzaakt door de mens-op-mens overdraagbare Corynebacterium species: C. diphtheriae, C. belfantii of C. rouxii. Voor de (zeer beperkte) maatregelen bij difterie veroorzaakt door C. ulcerans en andere zoönotische, toxineproducerende Corynebacterium-species wordt verwezen naar bijlage 1.
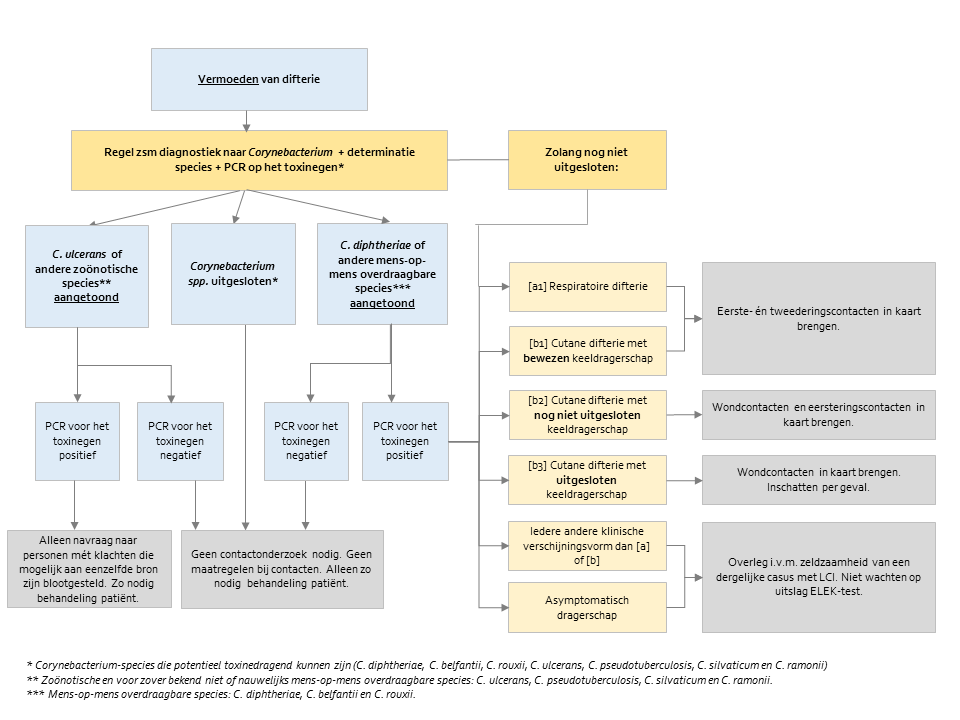
Figuur 4: Stroomschema maatregelen
Bronopsporing
De GGD inventariseert mogelijke bronnen. Voor C. diphtheriae en andere mens- op mens overdraagbare Corynebacterium-species zijn dat:
- Verblijf in een endemisch gebied in het buitenland.
- Contact in Nederland met bezoekers/ migranten uit endemische gebieden.
- Contact met een bevestigde patiënt.
Contactonderzoek
De GGD brengt de contacten van de index in kaart.
[1] Contactonderzoek bij respiratoire difterie en/of bij aangetoond keeldragerschap, indien veroorzaakt door C. diphtheriae
Bij respiratoire difterie (inclusief cutane difterie met bewezen keeldragerschap), doet de GGD contactonderzoek in de eerste en tweede ring: personen die 7 dagen vóór de eerste ziektedag van de index tot 48 uur na het starten van diens antibiotische behandeling contact met de index hebben gehad.
De eerste ring bestaat uit de volgende groepen:
- Huisgenoten (gezinsleden en anderen die gezamenlijk met de index een huishouden deelden) in de 7 dagen voor het ziek worden van de index tot 48 uur na het starten van diens antibiotische behandeling;
- Nauwe contacten. Dit zijn personen die gedurende 7 dagen voor het ziek worden van de index tot 48 uur na het starten van diens antibiotische behandeling:
- Eén of meerdere keren hebben geslapen in dezelfde ruimte als de index of
- In totaal langer dan 4 uur intensief contact hebben gehad met de index in hetzelfde huishouden. Voorbeelden hiervan zijn mensen die leven of slapen in hetzelfde huishouden als de index, zoals een oppas of logerende vriend(innet)jes. Maar ook personen die een slaapzaal/slaapcabine van een tent deelden met de index;
- Personen met zoen- en/of seksuele contacten met de indexpatiënt. - Personeel dat betrokken is bij de verzorging en behandeling van het indexgeval én onbeschermd blootgesteld is aan orofaryngeaal secreet van de patiënt;
- Opgenomen patiënten in een ziekenhuis/instelling die in dezelfde ruimte liggen als het indexgeval, of gelegen hebben. De GGD treedt in overleg met de deskundige infectiepreventie voor afstemming met de intramurale infectieziektebestrijding.
De tweede ring kan onder meer bestaan uit de volgende groepen:
Hieronder worden enkele mogelijke groepen genoemd om een indicatie te geven waaraan gedacht kan worden. De precieze bepaling van de contacten in de tweede ring in een concrete casus gebeurt in overleg tussen GGD en LCI.
- kinderen en onderwijzend personeel die dagelijks 4 uur of langer bij het indexgeval in hetzelfde lokaal verblijven (idem voor een kinderdagverblijf);
- collega's op het werk die dagelijks 4 uur of langer in dezelfde ruimte doorbrengen;
- regelmatige bezoekers van het gezin (ten minste 4 uur of langer in dezelfde ruimte als de index);
- (een selectie van) leden van een reisgezelschap, vereniging etc.
[2] Contactonderzoek bij cutane difterie door C. diphtheriae
Bij cutane difterie zonder aangetoond keeldragerschap gaat het om alle contacten die vanaf het ontstaan van de wond mogelijk in contact zijn geweest met wondexsudaat (wondcontacten). De aard van de relatie tussen patiënt en contact is hier niet relevant, maar alleen de kans dat iemand in contact is geweest met de wond, met gebruikt verbandmateriaal of met wondexsudaat. Loop voor beoordeling daarvan samen met de patiënt de sociale contacten langs (thuis, school, kindercentrum, sport, werk). Wondzorg: voor kleding is een volledig wasprogramma voldoende. Mocht er kleding / handdoeken in aanraking zijn geweest met wondvocht is een aanbeveling om dit te wassen op 60 graden.
Per geval moet een inschatting gemaakt worden van de kans op overdracht. Overleg met de LCI op basis van de aard, omvang, lokalisatie en wijze van behandelen, wie er daadwerkelijk als wondcontacten beschouwd moeten worden en hoe lang er terug in de tijd naar contacten gezocht moet worden.
Indien bij een patiënt met cutane difterie keeldragerschap nog niet is uitgesloten worden de contacten uit de eerste ring (met name de huisgenoten) ook in het contactonderzoek betrokken. Bij hen wordt in afwachting van de uitslag van de diagnostiek bij de index de vaccinatiestatus op peil gebracht.
Maatregelen bij de contacten
Maatregelen voor contacten uit de eerste ring
Onderstaande maatregelen voor de eerste ring zijn geïndiceerd bij:
- Eersteringscontacten van een index met een respiratoire difterie.
- Eersteringscontacten van een index met bewezen keeldragerschap bij cutane difterie.
- Wondcontacten van een patiënt met cutane difterie.
Maatregelen:
- Afnemen van een keelswab om dragerschap aan te tonen dan wel uit te sluiten, voor de start van antibioticaprofylaxe.
- Starten met antibioticaprofylaxe (ongeacht de vaccinatiestatus) na afname keelswab, maar voor uitslag van keelswab bekend is.
- Eenmalig vaccineren tegen difterie indien het laatste vaccin meer dan 10 jaar geleden is gegeven. Als het contact geen volledige basisserie heeft ontvangen of als de vaccinatiestatus onbekend is, wordt daarnaast geadviseerd om de basisserie af te ronden. Personen tot 18 jaar die niet basisimmuun zijn, kunnen vanuit het RVP gevaccineerd worden (zie ook de RVP-richtlijn).
- Monitoren van klachten tot 7 dagen na het laatste onbeschermde contact met de index op symptomen passend bij difterie.
Quarantaine van asymptomatische contacten is niet nodig.
Als contactpersonen van een patiënt met cutane difterie een positieve keelkweek hebben, moeten zij behandeld worden. Alsde afgenomen keelswab bij een contact positief blijkt, moetbij dit contact gehandeld worden als bij een nieuwe index, en moet deze nieuwe index worden gemeld.
Maatregelen voor contacten uit de tweede ring
Bij een indexpatiënt met respiratoire difterie of met bewezen keeldragerschap bij cutane difterie wordt bij contacten uit de tweede ring de vaccinatiestatus op peil gebracht.
De GGD overlegt met LCI of bij (bepaalde) ongevaccineerde contacten in de tweede ring dezelfde maatregelen moeten worden getroffen als bij contacten in de eerste ring.
Maatregelen bij de patiënt
Literatuuronderzoek over de afgelopen 30 jaar naar studies over de effectiviteit van maatregelen bij difterie leverde alleen casuïstisch materiaal op. De onderstaande maatregelen zijn gebaseerd op buitenlandse richtlijnen, expertopinie en consensus.
C. diphtheriae (en mogelijk/theoretisch ook C. belfantii of C. rouxii) is een exclusief humaan pathogeen met potentie voor het veroorzaken van uitbraken in populaties met een lage vaccinatiegraad (zoals de Nederlandse ‘Biblebelt’ of een asielzoekerscentrum).
Bij bewezen niet-toxinevormende stammen (PCR op toxinegen negatief, of PCR positief maar ELEK-test negatief) zijn geen verdere maatregelen nodig.
Als het gaat om een stam die (mogelijk) toxine vormt:
[1] Bacterie gedetermineerd als een C. diphtheriae, C. belfantii of C. rouxii maar PCR op het toxinegen nog niet gedaan of uitslag daarvan nog niet bekend: alvast maatregelen voorbereiden, nagaan dat de stam naar RIVM-IDS is verzonden. De uitslag is binnen 24 uur na inzetten bekend. Niet wachten op de uitslag van de ELEK-test.
[2] Bacterie gedetermineerd als een C. diphtheriae, C. belfantii of C. rouxii, en PCR positief: start uitvoering van de maatregelen; als de ELEK-test later negatief blijkt kunnen de maatregelen worden gestaakt. Bij een toxinogene stam met inconclusieve ELEK-test wordt gehandeld als bij een positieve ELEK-test..
[3] Bacterie gedetermineerd als een C. diphtheriae, C. belfantii of C. rouxii maar PCR niet (meer) mogelijk (stam zoek, geen goed materiaal voor de test, enz.): handelen als bij positieve PCR.
[1] Patiënt met waarschijnlijke of bevestigde respiratoire difterie of met cutane difterie met aangetoond of nog niet uitgesloten keeldragerschap
[1a] Patiënt met waarschijnlijke of bevestigde respiratoire difterie
Ernstig zieke difteriepatiënten worden in isolatie opgenomen in een ziekenhuis. Hier kan antitoxinebehandeling worden uitgevoerd en intensieve zorg worden verleend. In het ziekenhuis wordt de difteriepatiënt in druppelisolatie verpleegd totdat de behandeling met antibiotica is voltooid en twee kweken die met een tussenpoos van ten minste 24 uur zijn afgenomen, negatief zijn. De behandelaar neemt serum af (controle vaccinatiestatus) en neemt materialen voor microbiologisch onderzoek af (nasofarynx- en keeluitstrijk), indien mogelijk vóór de start van antibiotische therapie.
Licht zieke difteriepatiënten die volgens de behandelend arts geen antitoxinebehandeling nodig hebben, kunnen thuis in druppelisolatie worden verzorgd. De huisarts is verantwoordelijk voor de medische zorg, de GGD voor de organisatie van de infectiepreventie. Bezoeken van niet-huisgenoten moeten worden vermeden totdat de antibioticakuur is voltooid en twee kweken met een tussenpoos van ten minste 24 uur negatief zijn.
Ontslag uit isolatie (ziekenhuis, thuissituatie) vindt plaats na twee negatieve controlekweken (nasofarynx- en keeluitstrijk). De eerste kweek wordt afgenomen 48 uur na het staken van de antibiotische therapie; met een interval van minstens 24 uur volgt de tweede kweek.
[1b] Patiënt met cutane difterie met aangetoond of nog niet uitgesloten keeldragerschap
(Mogelijke) asymptomatische respiratoire dragers kunnen thuis behandeld worden met antimicrobiële middelen. Zij dienen in druppelisolatie te verblijven tot 48 uur na start van de antimicrobiële therapie.
De GGD is verantwoordelijk voor monitoring in de thuissituatie en ziet erop toe dat niet-gevaccineerde patiënten na volledig herstel gevaccineerd worden met toxoïd (bij voorkeur met DTP-vaccin).
Nacontrole dragerschap
Bij respiratoire difterie dient twee weken na beëindiging van behandeling een derde controlekweek te worden afgenomen. (Er bestaat een kans dat personen met een positieve kweek, na aanvankelijk negatief te zijn geweest na behandeling, toch weer positief worden). Indien weer positief maatregelen nemen als eerder vermeld.
[2] Patiënt met waarschijnlijke of bevestigde toxineproducerende cutane difterie zonder keeldragerschap
Bij cutane difterie is een kweek van keel geïndiceerd om dragerschap in de bovenste luchtwegen uit te sluiten. De patiënt dient thuis of eventueel in het ziekenhuis in contact-druppelisolatie te verblijven totdat keeldragerschap is uitgesloten óf tot 48 uur na start van de antimicrobiële therapie (zie WIP-richtlijn Druppelisolatie) verblijven totdat keeldragerschap is uitgesloten Bij cutane difterie zonder keeldragerschap is alleen contactisolatie (zie WIP-richtlijn Contactisolatie) van toepassing tot 48 uur na start antimicrobiële therapie.
Bij cutane difterie zonder keeldragerschap zijn controlekweken na antibiotische behandeling niet aangewezen. Men dient zorgvuldig om te gaan met verbandmateriaal. Het betreft afval met infectierisico, dat echter in afgesloten zakken met het gewone huisafval kan worden afgevoerd. Buiten instellingen kan het verband bij het huishoudelijk afval, maar afvalzakken moeten zorgvuldig afgesloten worden.
[3] Infectie (respiratoir, cutaan of op een andere plaats in het lichaam) veroorzaakt door een niet-toxigene of een NTTB C. diphtheriae.
Personen met een stam van C. diphtheriae die geen toxine produceert kunnen indien klinisch geïndiceerd behandeld worden met antibiotica (zie behandeling) en indien nodig worden gevaccineerd (zie bij Immunisatie). Controlekweken zijn hier niet nodig.
Zwangerschap
Maatregelen ten aanzien van zwangeren
Er zijn geen bijzondere maatregelen voor zwangeren.
Arbo
Melden als beroepsziekte
Indien de ziekte (waarschijnlijk) is opgelopen tijdens de beroepsuitoefening moet dit door een geregistreerd bedrijfsarts worden gemeld bij het Nederlands Centrum voor Beroepsziekten (NCvB): http://www.beroepsziekten.nl. C. diphtheriae valt onder risicoklasse 2 van de biologische agentia. Sinds 1997 zijn er geen meldingen van difterie bij het NCvB als beroepsziekte gedaan (info NCvB).
Wering van werk, school, kinderdagverblijf of consultatiebureau
Kinderen met respiratoire difterie of kinderen met cutane difterie met mogelijk keeldragerschap worden geweerd van school, kinderdagverblijf of consultatiebureau. De GGD beoordeelt of een kind met cutane difterie zonder keeldragerschap al dan niet wordt geweerd op basis van de specifieke situatie (bijvoorbeeld leeftijd van het kind, plaats van de laesie op het lichaam).
Arbo
Wering van werk
De bedrijfsarts beoordeelt of wering van werk, werkaanpassing en/of aanvullende maatregelen noodzakelijk zijn. Bij een cutane vorm zonder respiratoire component is wering van werk niet nodig. Dek de wond goed af, om verspreiding te voorkomen.
Profylaxe & Behandeling
Profylaxe
Onafhankelijk van de vaccinatiestatus van betrokkenen wordt in de eerste ring bij ieder bewezen geval van difterie door C. diphtheriae altijd profylaxe aangeboden, met als doelen:
- bij recent blootgestelde contacten de (mogelijke) infectie al behandelen tijdens de incubatieperiode.
- dragerschap elimineren om het risico op blootstelling van andere kwetsbare contacten te verkleinen.
De aanbevolen postexpositieprofylaxe is aangepast conform de recent vernieuwde adviezen van de UK Health Security Agency.
Postexpositieprofylaxe
| Antibioticum | Dosering en toedieningsweg |
|---|---|
| 1e keuze | |
| Claritromycine* | Volwassenen: 500 mg 2dd po voor 14 dagen Kinderen: zie Kinderformularium |
| 2e keuze | |
| Azitromycine* | Volwassenen: 1000 mg eenmalig, waarna 500 mg 1dd po, totaal 5 dagen Kinderen: zie Kinderformularium |
| Benzathine-benzylpenicilline** | <30 kg: 0,6 miljoen IE eenmalig im ≥30 kg: 1,2 miljoen IE eenmalig im |
* Voor zwangeren wordt als 1e keuze azitromycine geadviseerd en als 2e keuze erytromycine (voor dosering zie UK Health Security Agency). Hierbij wordt afgeweken van de UK Health Security Agency richtlijn in verband met afdoende veiligheidsdata over azitromycine tijdens de zwangerschap (voor meer informatie zie Overige overwegingen onder Uitgangsvraag 2 in de onderbouwing van de LCI-richtlijn Groep A-streptokokkeninfecties).
**Benzathinebenzylpenicilline kan overwogen worden als orale therapie niet wordt verdragen of als er twijfel is over de therapietrouw. Benzathinebenzylpenicilline mag niet intraveneus worden toegediend, alleen intramusculair.
Als de controlekweek positief blijkt en eliminatie niet is bereikt, verleng de chemoprofylaxe in overleg met een arts-microbioloog.
Op basis van beschikbare data uit ISIS-AR (2008 t/m 2017) zijn er geen aanwijzingen voor verminderde gevoeligheid voor macroliden onder stammen van C. diphtheriae die in Nederland geïsoleerd zijn. Er zijn momenteel echter geen EUCAST-breekpunten voor resistentiebepalingen. EUCAST heeft in juli 2022 een document uitgebracht ter consultatie over breekpunten op basis van epidemiologische wildtypeverdeling (ECOFF).
Behandeling
Antibiotica
Bij een hoge verdenking van difterie dient begonnen te worden met antibiotische therapie, zie onderstaande tabel. De adviezen zijn aangepast conform de recent vernieuwde adviezen van de UK Health Security Agency. Bij milde ziekte wordt claritromycine of erythromycine als eerste keus geadviseerd wegens een goede gevoeligheid en beschikbare klinische data (Kadirova 2000, Kneen 1998, Wilson 1995). Wegens het ontbreken van klinische data en beperkte microbiologische data wordt de voorkeur gegeven aan claritromycine boven azitromycine.
Antibiotische therapie milde ziekte* of ambulante behandeling
| Antibioticum | Dosering en toedieningsweg |
|---|---|
| 1e keuze | |
| Claritromycine | Volwassenen: 500 mg 2dd po voor 14 dagen Kinderen: zie Kinderformularium |
| Erythromycine | Volwassenen: 500 mg 4dd po voor 14 dagen Kinderen: zie Kinderformularium |
| 2e keuze | |
| Azitromycine | Volwassenen: 1000 mg eenmalig, waarna 500 mg 1dd po, totaal 10 dagen Kinderen: zie Kinderformularium |
Antibiotische therapie: ernstige ziekte of ziekenhuisopname
| Antibioticum | Dosering en toedieningsweg |
|---|---|
| Benzylpenicilline** + macrolide |
Volwassenen: penicilline 1 miljoen IE 6 dd iv; Kinderen: zie Kinderformularium |
| Voeg vancomycine toe indien ernstig ziek*** | Dosering in overleg met een arts-microbioloog |
* Milde ziekte: bijvoorbeeld kleine cutane laesies zonder aanwijzingen voor systemische toxiciteit.
** Voor penicilline lijkt er regelmatig een verminderde gevoeligheid te zijn, vooral bij de C. ulcerans, zodat dit alleen moet worden gebruikt indien de gevoeligheid is aangetoond.
*** Indien een patiënt ernstig systemisch ziek is, voeg een derde middel zoals vancomycine toe indien de gevoeligheid bekend is.
Difterie-antitoxine (DAT)
Voor behandeling van patiënten met difterie is antitoxine beschikbaar bij Dienst Vaccinvoorziening en Preventieprogramma’s (DVP) van het RIVM . Uitlevering van DAT gebeurt na overleg met de LCI.
De dosering is afhankelijk van de lokalisatie en uitbreiding van de difterie, evenals de duur van de ziekte. Antitoxine van humaan serum is niet meer leverbaar, daarom wordt uitgeweken naar paardenantiserum. Difterie-antitoxine is in Nederland niet geregistreerd, en alleen verkrijgbaar bij DVP, dat een ontheffing heeft van het gebruik van artsenverklaringen. Uiteraard dient de patiënt door de behandelaar geïnformeerd te worden over de toepassing van een niet in Nederland geregistreerd middel.
Indicatie
DAT bindt alleen aan ongebonden difterietoxine, dus aan difterietoxine dat nog niet weefselgebonden is. Bij een waarschijnlijk of bevestigd symptomatisch geval van respiratoire, toxigene difterie, dient de patiënt daarom zo snel mogelijk behandeld te worden met difterieantitoxine. Of een Corynebacterium diphtheriae dat het toxinegen heeft ook daadwerkelijk toxines produceert, is op grond van klinische symptomen vaak lastig vast te stellen. Schade van de toxines kunnen namelijk ook pas later tot uiting komen, bijvoorbeeld in de vorm van een myocarditis die acuut maar ook vanaf 10 dagen na de 1e ziektedag kan ontstaan (Bennet 2020, geraadpleegd 13-3-2024). Neurologische complicaties ontstaan nog later, meestal tussen de 3 en 8 weken na de 1e ziektedag (Farrar 2024, geraadpleegd 13-3-2024). Antitoxine wordt bij huiddifterie in principe niet toegediend. Alleen een casus waarbij toxigene C. diphteriae wordt geïsoleerd uit een laesie op non-respiratoire locatie en er tekenen zijn van systemische toxiciteit (zoals koorts, myocarditis of neuropathie) is hierop een uitzondering (CDC). Er is in principe geen indicatie voor difterie-antitoxine bij asymptomatisch dragerschap van toxigene C. diphtheriae, of als postexpositieprofylaxe.
Dosering
De dosering van difterie-antitoxine is niet gestandaardiseerd in de mondiale medische praktijk, zodat er meerdere doseringen of soms een range van een dosering worden aanbevolen in de diverse richtlijnen. In deze Nederlandse richtlijn zijn de doseringen van het behandeladvies van februari 2024 van de WHO als uitgangspunt genomen. Deze doseringen zijn, ook in het grootste retrospectieve onderzoek met DAT, gebruikt met goede uitkomsten (Eisenberg 2020). De aangegeven doseringen zijn de minimumdoseringen bij de verschillende stadia van difterie. Indien in de bijsluiter van DAT een andere dosis wordt geadviseerd, houd dan als maximale dosis de bovengrens aan van de range zoals die wordt geadviseerd door CDC. Betrek ook de dosering per verpakking van het voorhanden zijnde DAT-preparaat; de dienstdoende arts van de LCI beschikt over deze informatie. De doseringen zijn niet leeftijd- of gewichtafhankelijk. DAT dient bij klinische verdenking zo snel mogelijk te worden toegediend.
| Difterie stadium | Dosering DAT (IU) |
|---|---|
|
Laryngitis of faryngitis En Duur <48 uur |
20.000 |
|
Nasofaryngeaal (uitgebreid pseudomembraan) En Duur <48 uur |
40.000 |
|
Duur >48 uur Diffuse zwelling van de nek Ernstige ziekte (respiratoire nood, shock) |
80.000 |
Bijwerkingen
DAT zoals op dit moment beschikbaar bij DVP zijn immuunglobulines verkregen uit equine serum (paardenserum). In de klinische praktijk bleek dit bij 3% van de gevallen ernstige overgevoeligheidsreacties te veroorzaken, waarvoor behandeling nodig is (Eisenberg 2020). Daarom is alleen toediening in een ziekenhuis mogelijk, om deze mogelijk ernstige overgevoeligheidsreacties snel te kunnen behandelen. Mensen die eerder een allergische reactie hebben gehad na behandeling met dierlijke immuunglobulines hebben een verhoogd risico op een allergische reactie.
Vanwege dit risico wordt in sommige richtlijnen en bijsluiters daarom geadviseerd voorafgaand aan toediening van DAT een overgevoeligheidstest (=huidtest) te doen en/of iedereen voorafgaand aan toediening medicatie (antihistaminica en/of corticosteroiden) toe te dienen. Over het gebruik van premedicatie is geen consensus. De WHO raadt af om een overgevoeligheidstest voorafgaand aan toediening van DAT te doen: deze huidtest is niet voldoende voorspellend voor eventuele allergische reacties of kan op zichzelf al zo’n reactie uitlokken. Daarnaast moet DAT zo snel mogelijk worden toegediend om schade door toxine te voorkomen en de tijd die besteed wordt aan de overgevoeligheidstest kan hierbij klinisch nadelig gevolgen hebben. Bovendien is een eerdere allergische reactie bij de patiënt voor het product geen contra-indicatie voor toediening. Daarom is het advies om DAT in een ziekenhuis te geven waar ernstige allergische reacties snel en adequaat behandeld kunnen worden.
Historie
Hoewel waarschijnlijk Hippocrates de ziekte reeds kende, kreeg ze pas in 1821 een naam. Tijdens een epidemie in het zuiden van Frankrijk gaf de Fransman Bretonneau de ziekte de naam ‘difterie’, vanwege de kenmerkende membranen in de keelholte (lederen lap, vel). De eerste onderkende pandemie vond plaats tussen 1858 en 1860 (ook in Nederland). In 1883 toonde Klebs de verwekker aan in een microscopisch preparaat van het difteriemembraan; het jaar daarna isoleerde Loeffler de bacterie met behulp van zelf samengestelde media. Roux en Iresine ontdekten het toxine in 1888, waarna Behring aantoonde dat dieren, zoals paarden, antitoxine aanmaken wanneer zij met difterietoxine worden ingespoten. Behring ontving in 1901 de eerste Nobelprijs voor de Geneeskunde voor de ontdekking dat serum met antistoffen (‘antiserum’) gebruikt kan worden voor de preventie en behandeling van difterie. Roux paste deze behandeling in 1894 voor het eerst toe bij patiënten met difterie en halveerde daarmee de letaliteit onder Parijse vondelingen van 51% naar 24%.
In 1923 ontdekte Ramon dat expositie van het toxine aan formaldehyde en hitte het toxine inactiveert met behoud van het vermogen een antistofrespons op te wekken. Dit ‘toxoïd’ werd kort daarop in gebruik genomen als vaccin. Ondanks actieve immunisatie en massale toepassing van antitoxine bleef difterie tussen de twee wereldoorlogen, zowel in Europa als in Amerika, de belangrijkste doodsoorzaak in de leeftijdsgroep van 4-10 jaar. Inmiddels is difterie in de Westerse wereld zeldzaam geworden en wordt daardoor mogelijk (te) laat herkend, gediagnosticeerd en behandeld.
Literatuur
- Billard-Pomares T, Rouyer C, Walewski V, Badell-Ocando E, Dumas M, Zumelzu C, et al. Diagnosis in France of a Non-Toxigenic tox Gene-Bearing Strain of Corynebacterium diphtheriae in a Young Male Back From Senegal. Open Forum Infect Dis. 2017;4(1):ofw271. https://doi.org/10.1093/ofid/ofw271
- CDC. Expanded Access Investigational New Drug (IND) Application Protocol: Use of Diphtheria Antitoxin (DAT) for Possible Diphtheria Cases2023 [cited 2024. Available from: https://www.cdc.gov/diphtheria/downloads/protocol.pdf.
- Christie AB. Infectious diseases: Epidemiology and Clinical Practice. Edinburgh: Churchill Livingstone; 1987.
- Dittmann S, Wharton M, Vitek C, Ciotti M, Galazka A, Guichard S, et al. Successful control of epidemic diphtheria in the states of the Former Union of Soviet Socialist Republics: lessons learned. J Infect Dis. 2000;181 Suppl 1:S10-22. https://doi.org/10.1086/315534
- ECDC. Increase of reported diphtheria cases among migrants in Europe due to Corynebacterium diphtheriae, 2022 Stockholm: ECDC; 2022.
- Eisenberg N, Panunzi I, Wolz A, Burzio C, Cilliers A, Islam MA, et al. Diphtheria Antitoxin Administration, Outcomes, and Safety: Response to a Diphtheria Outbreak in Cox's Bazar, Bangladesh. Clin Infect Dis. 2021;73(7):e1713-e8. https://doi.org/10.1093/cid/ciaa1718
- Elsinga J, van Meijeren D, Reubsaet F. Surveillance of diphtheria in the Netherlands between 2000-2021: cutaneous diphtheria supersedes the respiratory form. BMC Infect Dis. 2023;23(1):420. https://doi.org/10.1186/s12879-023-08388-5
- Farrar J, Hotez PJ, Junghanss T, Kang G, Lalloo D, White NJ, Garcia PJ. Manson’s tropical diseases: Elsevier; 2023 13-03-2024].
- Galazka A. The changing epidemiology of diphtheria in the vaccine era. J Infect Dis. 2000;181 Suppl 1:S2-9. https://doi.org/10.1086/315533
- Galazka A. Implications of the diphtheria epidemic in the Former Soviet Union for immunization programs. J Infect Dis. 2000;181 Suppl 1:S244-8. https://doi.org/10.1086/315570
- Gezondheidsraad. Werknemers en infectieziekten - Criteria voor vaccinatie. Den Haag; 2014.
- Harnisch JP, Tronca E, Nolan CM, Turck M, Holmes KK. Diphtheria among alcoholic urban adults. A decade of experience in Seattle. Ann Intern Med. 1989;111(1):71-82. https://doi.org/10.7326/0003-4819-111-1-71
- Kadirova R, Kartoglu HU, Strebel PM. Clinical characteristics and management of 676 hospitalized diphtheria cases, Kyrgyz Republic, 1995. J Infect Dis. 2000;181 Suppl 1:S110-5. https://doi.org/10.1086/315549
- Kneen R, Pham NG, Solomon T, Tran TM, Nguyen TT, Tran BL, et al. Penicillin vs. erythromycin in the treatment of diphtheria. Clin Infect Dis. 1998;27(4):845-50. https://doi.org/10.1086/514959
- Larsson P, Brinkhoff B, Larsson L. Corynebacterium diphtheriae in the environment of carriers and patients. J Hosp Infect. 1987;10(3):282-6. https://doi.org/10.1016/0195-6701(87)90010-7
- Lier Ev, Hament J-M, Knijff M, Westra M, Ernst A, Giesbers H, et al. Vaccinatiegraad en jaarverslag Rijksvaccinatieprogramma Nederland 2022. Vaccination coverage and annual report of the National Immunisation Programme in the Netherlands, 2022: Rijksinstituut voor Volksgezondheid en Milieu RIVM; 2023.
- Melker Hd, Hof Svd, Berbers G, Bondt PV-d, Spaendonck MC-v. Difterie en tetanus in Nederland. Infectieziekten Bulletin. 2001(2001; 12:182-6).
- Swart EM, van Gageldonk PG, de Melker HE, van der Klis FR, Berbers GA, Mollema L. Long-Term Protection against Diphtheria in the Netherlands after 50 Years of Vaccination: Results from a Seroepidemiological Study. PLoS One. 2016;11(2):e0148605. https://doi.org/10.1371/journal.pone.0148605
- Truelove SA, Keegan LT, Moss WJ, Chaisson LH, Macher E, Azman AS, Lessler J. Clinical and Epidemiological Aspects of Diphtheria: A Systematic Review and Pooled Analysis. Clin Infect Dis. 2020;71(1):89-97. https://doi.org/10.1093/cid/ciz808
- WHO. Diphtheria - number of reported cases. In: Organization WH, editor. 2022.
- WHO. Clinical management of diphtheria: guideline. World Health Organization; 2024.
- Wilson AP. Treatment of infection caused by toxigenic and non-toxigenic strains of Corynebacterium diphtheriae. J Antimicrob Chemother. 1995;35(6):717-20. https://doi.org/10.1093/jac/35.6.717
- Wright W, E. Couturier's Occupational and Environmental Infectious Diseases: Oem Health Information Inc; 2009.







